
REAÇÕES ADVERSAS CLORIDRATO DE SIBUTRAMINA MONOIDRATADO
REAÇÕES DURANTE ESTUDOS CLÍNICOS: A MAIOR PART E DOS EFEITOS COLATERAIS1 RELATADOS OCORREU NO INÍCIO DO TRATAMENTO COM SIBUTRAMINA (DURANTE AS PRIMEIRAS QUATRO SEMANAS). SUA GRAVIDADE E FREQÜÊNCIA DIMINUÍRAM NO DECORRER DO TEMPO. OS EFEITOS, EM GERAL, NÃO FORAM GRAVES, NÃO LEVARAM À DESCONTINUAÇÃO DO TRATAMENTO E FORAM REVERSÍVEIS.
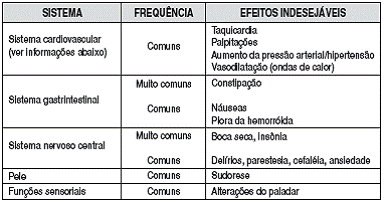
OS EFEITOS COLATERAIS1 OBSERVADOS NOS ESTUDOS CLÍNICOS DE FASE II/III SÃO RELACIONADOS A SEGUIR POR ÓRGÃO/SISTEMA (MUITO COMUNS > 1/10; COMUNS ≤ 1/10 E > 1/100).
HIPERTENSÃO2 E AUMENTO DA FREQÜÊNCIA CARDÍACA EM ESTUDOS CLÍNICOS: FORAM OBSERVADOS AUMENTOS DA PRESSÃO ARTERIAL SISTÓLICA3 E DIASTÓLICA DE REPOUSO NA VARIAÇÃO ENTE 1-3 MM HG, E AUMENTOS DA FREQÜÊNCIA CARDÍACA DE 3-5 BATIMENTOS POR MINUTO. EM RELAÇÃO AO PLACEBO4, UM PEQUENO NÚMERO DE PACIENTES APRESENTOU AUMENTOS CONSTANTES DA PRESSÃO ART ERIAL E DA FREQUÊNCIA CARDÍACA EM REPOUSO.
NOS ESTUDOS CONTROLADOS COM PLACEBO4, EVENTOS ADVERSOS CLINICAMENTE RELEVANTES QUE FORAM ASSOCIADOS COM OS AUM ENTOS DA PRESSÃO ARTERIAL5 E DA FREQÜÊNCIA CARDÍACA FORAM RAROS NO GRUPO TRATADO COM CLORIDRATO DE SIBUTRAMINA MONOIDRATADO E OCORRERAM COM A MESMA INCIDÊNCIA6 DAQUELA OBSERVADA NO GRUPO TRATADO COM PLACEBO4.
REAÇÕES OBSERVADAS NOS ESTUDOS DE FASE IV OU NA FARMACOVIGILÂNCIA PÓS-COMERCIALIZAÇÃO: OS EVENTOS ADVERSOS OBSERVADOS ESTÃO RELACIONADOS A SEGUIR POR ÓRGÃO/ SISTEMA:
SISTEMA HEMATOLÓGICO: TROMBOCITOPENIA7.
SISTEMA IMU NOLÓGICO: FORAM RELATADAS REAÇÕES DE HIP ERSENSIBILID ADE ALÉRGICA VARI ANDO DESDE LEVES ERUPÇÕES CUTÂNEAS8 E URTICÁRIA9 ATÉ ANGIOEDEMA10 E ANAFILAXIA11.
TRANSTORNOS PSIQUIÁTRICOS: RARAMENTE FORAM RELATADOS CASOS DE DEPRESSÃO, IDÉIAS SUICIDAS E SUICÍDI O EM PACIENTES TRATADOS COM SIBUTRAMINA. ENTRETANTO, A RELAÇÃO CAUSAL NÃO FOI ESTABELECID A ENTRE A OCORRÊNCIA DESSAS REAÇÕES E O USO DE SIBUTRAMINA.
SE OCORRER DEPRESSÃO DURANTE O TRATAMENTO COM SIBUTRAMINA, É NECESSÁRIA UMA AVALIAÇÃO DO PACIENTE.
SISTEMA NERVOSO12: CONVULSÕES.
DISTÚRBIOS OCULARES: VISÃO13 BORRADA.
SISTEMA GASTRINTESTINAL: DIARRÉIA14 E VÔMITOS15.
PELE E TECIDO SUBCUTÂNEO16: ERUPÇÕES CUTÂNEAS8, URTICÁRIA9.
RINS17/ALTERAÇÕES URINÁRIAS: RETENÇÃO URINÁRIA18.
SISTEMA REPRODUTOR: EJACULAÇÃO19 ANORMAL (ORGASMO), IMPOTÊNCIA20, DISTÚRBIOS DO CICLO MENSTRUAL, METRORRAGIA21.
ALTERAÇÕES LABORATORIAIS: AUMENTOS REVERSÍVEIS DAS ENZIMAS HEPÁTICAS22. OUTROS EVENTOS ADVERSOS NOTÁVEIS:
CONVULSÕES: EM ESTUDOS CLÍNICOS FORAM RELATADAS CONVULSÕES COMO REAÇÃO ADVERSA EM TRÊS DOS 2068 (0,1%) PACIENTES TRATADOS COM CLORIDRATO DE SIBUTRAMINA MONO IDRATADO E EM NENHUM DOS 884 PACIENTES TRATADOS COM PLACEBO4. DOIS DOS TRÊS PACIENTES COM CONVULSÃO23 APRESENTAVAM FATORES PREDISPONENTES: UM TINHA HISTÓRIA PREGRESSA DE EPILEPSIA24; UM TEVE UM DIAGNÓSTICO25 SUBSEQÜENTE DE TUMOR26 CEREBRAL. A INCIDÊNCIA6 EM TODOS OS INDIVÍDUOS QUE FORAM TRATADOS COM CLORIDRATO DE SIBUTRAMINA MONOIDRATADO (TRÊS DE 4.588 PACIENTES) FOI MENOS DE 0,1%.
DISTÚRBIOS DO SANGRAMENTO/EQUIMOSES27: EM ESTUDOS CONTROLADOS COM PLACEBO4 FORAM RELATADAS EQUIMOSES27 EM 0,7% DOS PACIENTES TRATADOS COM CLORIDRATO DE SIBUTRAMINA E EM 0,2% DOS TRATADOS COM PLACEBO4. CLORIDRATO DE SIBUTRAMINA MONOIDRATADO PODE APRESENTAR UM EFEITO SOBRE A FUNÇÃO PL AQUETÁRIA DEVIDO A SEUS EFEITOS SOBRE A CAPTAÇÃO DE SEROTONINA.
NEFRITE28 INTERSTICIAL29: FOI RELATADO UM CASO DE NEFRITE28 INTERSTICIAL29 AGUDA, CONFIRMADA POR BIÓPSIA30, EM UM PACIENTE OBESO. DEPOIS DA DESCONTINUAÇÃO DO TRATAMENTO, FORAM ADMINISTRADOS CORTICOSTERÓIDES E REALIZADA DIÁLISE31, COM A QUAL A FUNÇÃO RENAL32 NORMALIZOU. O PACIENTE SE RECUPEROU COMPLETAMENTE.
ALTERAÇÕES LABORATORIAIS: FORAM RELATADAS ALTERAÇÕES DOS TESTES DE FUNÇÃO HEPÁTICA33, INCLUINDO AUMENTO DE AST, ALT, GAMA-GT, FOSFATASE ALCALINA34 E BILIRRU BINAS, COMO EVENTOS ADVERSOS EM 1,6% DOS PACIENTES TRATADOS COM CLORIDRATO DE SIBUTRAMINA MONOIDRATADO, EM COMPARAÇÃO COM 0,8% DOS PACIENTES TRATADOS COM PLACEBO4. NESSES ESTUDOS OS VALORES CONSIDERADOS CLINICAMENTE RELEVANTES (QUE SÃO: BILIRRUBINAS35 ≥ 2MG/DL; ALT, AST, GAMA-GT, LDH, OU FOSFATASE ALCALINA34 ≥ 3 VEZES O LIMITE SUPERIOR DE NORMALIDADE) OCORRERAM EM 0% (COM RELAÇÃO À FOSFATASE ALCALINA34) A 0,6% (ALT ) DOS PACIENTES TRATADOS COM CLORIDRATO DE SIBUTRAMINA MONOIDRATADO E EM NENHUM DOS TR ATADOS COM PL ACEBO. OS VALORES ANORMAIS APRESENTARAM UM A TENDÊNCIA A SEREM ESPORÁDICOS, FREQUENTEMENTE DIMINUÍRAM MESMO SEM A DESCONTINUAÇÃO DO TRATAMENTO, E NÃO APRESENTARAM UMA CLARA RELAÇÃO DOSE-RESPOSTA.
- POSOLOGIA E ADMINISTRAÇÃO:
A dose inicial recomendada é de 1 cápsula de 10 mg por dia, pela manhã, com ou sem alimentação.
Se o paciente não perder pelo menos 2 kg nas primeiras 4 semanas de tratamento, o médico deve considerar a reavaliação do tratamento, que pode incluir um aumento da dose para 15 mg ou a descontinuação da sibutramina. No caso de titulação da dose, devem-se levar em consideração os índices de variação da freqüência cardíaca e da pressão arterial5.
Doses acima de 15 mg ao dia não são recomendadas.
O uso da sibutramina demonstrou ser seguro e efetivo por até 24 meses em estudos duplo-cego placebo4 controlados.


