
REAÇÕES ADVERSAS TORLÓS
Em estudos clínicos controlados de hipertensão1, verificou-se que a losartana potássica, em geral, é bem tolerada; os efeitos adversos foram em geral de natureza leve e transitória e não requereram a descontinuação do tratamento. A incidência2 geral de efeitos colaterais3 relatados com a losartana potássica foi comparável à do placebo4. Em estudos clínicos controlados de hipertensão1 essencial, tontura5 foi o único efeito adverso relatado como relacionado à medicação com incidência2 superior à do placebo4, em 1% ou mais dos pacientes tratados com losartana potássica. Além disso, efeitos ortostáticos relacionados à dose foram observados em menos de 1% dos pacientes. Raramente foi relatada erupção6 cutânea7, embora a incidência2 em estudos clínicos controlados tenha sido menor do que a do placebo4.
Nesses estudos clínicos duplo-cegos e controlados sobre hipertensão1 essencial, as seguintes experiências adversas relatadas com a losartana potássica ocorreram em 1% dos pacientes, independentemente da relação com a medicação:

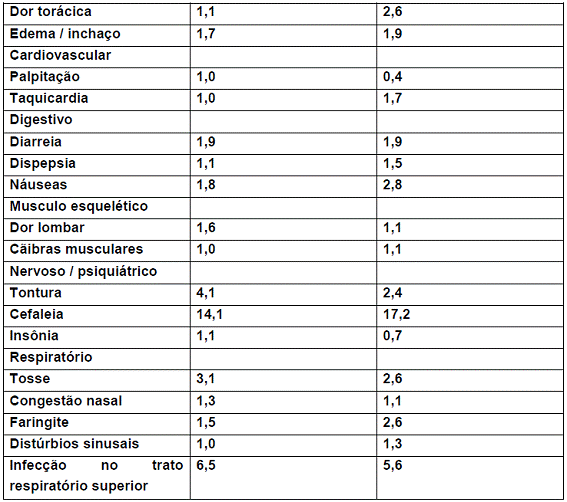
A losartana potássica foi geralmente bem tolerada em estudos clínicos controlados sobre insuficiência cardíaca8. Os efeitos adversos mais comuns relacionados à medicação foram tontura5 e hipotensão9.
A losartana potássica foi geralmente bem tolerada em um estudo clínico que envolveu pacientes com hipertrofia10 ventricular esquerda. As reações adversas relacionadas à medicação mais comuns foram tontura5, astenia11/fadiga12 e vertigem13.
No estudo LIFE (Losartan Intervention For Endpoint reduction in hypertension), dentre os pacientes sem diabetes14 no período basal, a incidência2 de novos casos de diabetes mellitus15 com a losartana potássica foi mais baixa quando comparada àquela observada com o atenolol (242 pacientes versus 320 pacientes, respectivamente, p<0,001). Como não foi incluído no estudo um grupo com placebo4, não se sabe se isso representa efeito benéfico da losartana potássica ou reação adversa ao atenolol.
A losartana potássica foi geralmente bem tolerada em um estudo clínico controlado que envolveu pacientes com diabetes tipo 216 e proteinúria17. As reações adversas relacionadas à medicação mais comuns foram astenia11/fadiga12, tontura5, hipotensão9 e hipercalemia18 (vide “Hipotensão e Desequilíbrio hidroeletrolítico” em “Precauções e Advertências”).
Após a comercialização da losartana potássica, foram relatados os seguintes efeitos adversos: - Hipersensibilidade: reações anafiláticas19, angioedema20, incluindo edema21 de laringe22 e glote23, com obstrução das vias aéreas e/ou edema21 de face24, lábios, faringe25 e/ou língua26, foram relatados raramente em pacientes tratados com losartana; alguns desses pacientes apresentaram anteriormente angioedema20 com outros medicamentos, entre eles os inibidores da ECA. Vasculite27, incluindo púrpura28 de Henoch-Schoenlein, foi raramente relatada.
- Gastrintestinais: anormalidades da função hepática29, hepatite30 (relatada raramente).
- Hematológico: anemia31.
- Musculoesquelético: mialgia32.
- Sistemas nervoso/psiquiátrico: enxaqueca33.
- Respiratório: tosse.
- Pele34: urticária35, prurido36.
Alterações em exames laboratoriais: em estudos clínicos controlados sobre hipertensão1 essencial, alterações clinicamente importantes dos parâmetros laboratoriais-padrão foram raramente associadas com a administração de losartana potássica. Hipercalemia18 (potássio sérico >5,5 mEq/L) ocorreu em 1,5% dos pacientes nos estudos clínicos sobre hipertensão1. Em um estudo clínico conduzido em pacientes com diabetes tipo 216 e proteinúria17, 9,9% dos pacientes tratados com a losartana potássica e 3,4% dos pacientes que receberam placebo4 desenvolveram hipercalemia18 (vide “Hipotensão e Desequilíbrio hidroeletrolítico” em “Precauções e Advertências”). Raramente ocorreram aumentos de ALT que, em geral, desapareceram com a descontinuação do tratamento.


