
ADVERTÊNCIAS E PRECAUÇÕES ACTOS
Estudos clínicos e dados epidemiológicos disponíveis sugerem um pequeno aumento do risco de câncer1 de bexiga2 em pacientes diabéticos tratados com pioglitazona, em particular em pacientes em tratamento por longos períodos. Portanto, a terapia não deve ser iniciada em pacientes com câncer1 ativo de bexiga2, e deve ser usado com precaução em pacientes com histórico de câncer1 de bexiga2. Os pacientes devem ser aconselhados a procurar seu médico imediatamente se hematúria3 macroscópica ou outros sintomas4, como de urgência5 miccional, desenvolverem-se durante o tratamento.
Retenção de fluidos e insuficiência cardíaca6: A pioglitazona, como outras tiazolidinedionas, podem causar retenção de fluidos, o que pode exacerbar ou precipitar uma insuficiência cardíaca6. Pacientes com insuficiência cardíaca6 devem ser monitorados por seus sinais7 e sintomas4, e a descontinuação do tratamento com pioglitazona deve ser considerado se qualquer deterioração do estado cardíaco ocorrer. Em um estudo clínico de pioglitazona e insulina8, placebo9-controlado, duplo-cego com 566 pacientes, dois pacientes que receberam pioglitazona 15mg e insulina8 (1,1%) e dois pacientes que receberam pioglitazona 30mg mais insulina8 (1,1%) desenvolveram insuficiência cardíaca congestiva10 (ICC) em comparação com nenhum dos pacientes que receberam somente insulina8. Em outro estudo dose-controlada de pioglitazona co-administrado com insulina8, 0,3% (1/345) dos pacientes tratados com 30mg e 0,9% (3/345) dos pacientes tratados com 45mg reportaram ICC como um evento adverso grave. Nestes estudos, não foi identificado nenhum fator específico que poderia prever um risco aumentado de ICC em terapia combinada11 com insulina8.
Um estudo de segurança pós-comercialização comparou a pioglitazona (n = 262) e a glibenclamida (n = 256) em pacientes diabéticos não controlados com insuficiência cardíaca6 NYHA classe II e III e fração de ejeção menor que 40%.
Internação hospitalar noturna devido a ICC foi relatada em 9,9% dos pacientes tratados com pioglitazona em comparação com 4,7% dos pacientes tratados com glibenclamida. Não houve diferença na mortalidade12 cardiovascular entre os grupos de tratamento. No estudo PROactive (estudo clínico prospectivo13 de pioglitazona em eventos macrovasculares), 5.238 pacientes com diabetes mellitus14 tipo II e uma história prévia de doença macrovascular15 foram tratados com pioglitazona (n = 2.605), titulação forçada até 45 mg ao dia, ou placebo9 (n = 2,633), além do atendimento padrão. Quase todos os indivíduos (95%) estavam recebendo medicamentos cardiovasculares (beta-bloqueadores, inibidores da ECA, BRAs, bloqueadores dos canais de cálcio, nitratos, diuréticos16, aspirina, estatinas, fibratos). Os pacientes tinham uma idade média de 61,8 anos, duração média do diabetes17 de 9,5 anos e HbA1c18 média de 8,1%. A duração média de acompanhamento foi de 34,5 meses. A primeira variável de eficácia foi o tempo para a primeira ocorrência de qualquer evento no desfecho cardiovascular composto que inclui mortalidade12 por todas as causas, infarto19 miocardial não-fatal (IM), incluindo IM silencioso, acidente vascular cerebral20, síndrome21 coronariana aguda, intervenção cardíaca, incluindo cirurgia de revascularização miocárdica ou intervenção percutânea, amputação22 da perna acima do tornozelo23, e revascularização da perna.
Um total de 514 (19,7%) dos pacientes tratados com pioglitazona e 572 (21,7%) dos pacientes tratados com placebo9 apresentaram pelo menos um evento do desfecho primário composto (hazard ratio 0,90; Intervalo de confiança 95%: 0,80, 1,02, p = 0,10). Embora não haja diferença estatisticamente significativa entre a pioglitazona e o placebo9 para a incidência24 de um primeiro evento dentro deste composto em 3 anos, não houve aumento na mortalidade12 nem no número total de eventos macrovasculares com pioglitazona (ver Tabela 11 abaixo). A porcentagem de pacientes que tiveram um caso de insuficiência cardíaca6 grave foi maior entre os pacientes tratados com pioglitazona (5,7% , n = 149) do que para os pacientes tratados com placebo9 (4,1% , n = 108) . A incidência24 de morte na sequência de um relato de insuficiência cardíaca6 grave foi de 1,5% (n = 40) em pacientes tratados com pioglitazona e 1,4% (n = 37) em pacientes tratados com placebo9. Em pacientes tratados com um regime contendo insulina8 no início do estudo, a incidência24 de insuficiência cardíaca6 grave foi de 6,3% (n = 54/864 ) com pioglitazona e 5,2% (n = 47/896 ) com placebo9. Para aqueles tratados com um regime contendo sulfonilureia no início do estudo, a incidência24 de insuficiência cardíaca6 grave foi de 5,8% (n = 94 /1,624) com pioglitazona e 4,4% ( n = 71 /1,626) com placebo9.
A pioglitazona deve ser iniciada com a menor dose aprovada em pacientes com diabetes17 tipo II e insuficiência cardíaca6 sistólica (NYHA classes I e II). Se o escalonamento de dose subsequente for necessário, a dose deve ser aumentada gradualmente somente depois de vários meses de tratamento com monitorização cuidadosa de ganho de peso, edema25 ou exacerbação da ICC.

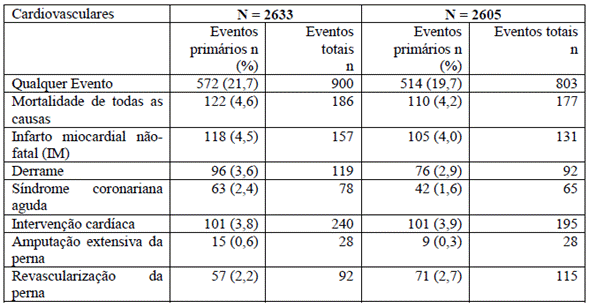
CRM = cirurgia de revascularização miocárdica; IP = intervenção percutânea
Câncer1 de bexiga2: casos de câncer1 de bexiga2 foram reportados mais frequentemente em uma meta-análise de estudos clínicos controlados com pioglitazona (19 casos em 12.506 pacientes, 0,15%) do que em grupos de controle (7 casos em 10.212 pacientes, 0,07%) HR-2,64 (IC 95% 1,11 – 6,31, P = 0,029). Após a exclusão de pacientes cuja exposição ao medicamento em estudo foi inferior a um ano no momento do diagnóstico26 de câncer1 de bexiga2, houve 7 (0,06%) casos relatados com o uso de pioglitazona e 2 casos (0,02%) nos grupos de controle. A análise interina de 5 anos de um estudo de coorte27 observacional em andamento com duração de 10 anos demonstrou um aumento não significativo no risco de câncer1 de bexiga2 em pessoas expostas a ACTOS, quando comparado com pessoas nunca expostas a ACTOS® (HR 1,2 [IC 95% 0,9-1,5]). Quando comparada com a ausência de exposição, a duração do tratamento com ACTOS superior a 12 meses foi associada a um aumento no risco (HR 1,4 [IC 95% 0,9-2,1]),
atingindo significância estatística com uso de ACTOS superior a 24 meses (HR 1,4 [IC 95% 1,03-2,0]).
Monitoramento da função do fígado28: foram recebidos raros relatos pós-comercialização de disfunção hepática29. Os pacientes tratados com pioglitazona devem, portanto, submeter-se a monitorização das enzimas hepáticas30 antes do início do tratamento e depois periodicamente. O tratamento com pioglitazona não deve ser iniciado em pacientes com aumento dos níveis das enzimas hepáticas30 (TGP > 2,5 vezes o limite superior da normalidade) ou com qualquer outra evidência de doença hepática29. O tratamento existente com pioglitazona deve ser interrompido se os níveis de TGP forem persistentemente 3x mais elevados do que o limite superior da normalidade, e os sintomas4 sugestivos de disfunção hepática29 devem fazer com que as enzimas do fígado28 sejam verificadas. Enquanto se aguardam os resultados dos exames laboratoriais, a decisão se o tratamento com pioglitazona deve continuar deve ser baseada no julgamento clínico; na presença de icterícia31, o tratamento deve ser descontinuado.
Ganho de peso: foi observado ganho de peso em estudos clínicos com pioglitazona e em experiência pós-comercialização, então o peso do paciente deve ser monitorado de perto.
Como parte do tratamento de diabetes17 inclui o controle da dieta, os pacientes devem aderir rigorosamente a uma dieta com controle de calorias32.
Hematologia: em estudos clínicos controlados e comparativos sobre o tratamento com pioglitazona, houve uma pequena redução na hemoglobina33 média (redução relativa de 4%) e hematócrito34 (redução relativa de 4,1%), consistentes com hemodiluição. Alterações semelhantes foram vistas com metformina35 (reduções relativas de hemoglobina33 3 - 4% e hematócrito34 3,6 – 4,1%) e em uma extensão menor com sulfonilureia (reduções relativas de hemoglobina33 1 - 2% e hematócrito34 1 – 3,2%).
Ovulação36: Pacientes com síndrome21 do ovário37 policístico podem retomar a ovulação36 após o tratamento com pioglitazona, como conseqüência de uma maior ação da insulina8. As pacientes devem, portanto, estar conscientes do risco de gravidez38; se a paciente deseja engravidar ou se ocorrer gravidez38, o tratamento deve ser interrompido.
Outros: ACTOS contém lactose39 monodratada e, dessa forma, não deve ser administrada em pacientes com problemas hereditários raros de intolerância a galactose40, deficiência de lactase de Lapp ou má-absorção de glucose-galactose40.
ACTOS exerce seu efeito anti-hiperglicêmico somente na presença de insulina8 e por isso, não deve ser usado em pacientes com diabetes17 tipo I ou para o tratamento de cetoacidose diabética41.
Efeitos na habilidade de dirigir ou operar máquinas: Nenhum. Pioglitazona não tem nenhum efeito ou efeito insignificante na habilidade de dirigir ou operar máquinas. Entretanto, pacientes que apresentarem distúrbios visuais devem ser cautelosos ao dirigir ou operar máquinas.
Gravidez38: este produto não deve ser usado durante a gravidez38 exceto quando os benefícios percebidos superem os potenciais riscos.
Não existem dados adequados e humanos que demonstrem a segurança de ACTOS, usado isoladamente ou em combinação com metformina35 ou glimepirida42, durante a gravidez38.
Em estudos com animais, foram observados atraso no parto e embriotoxicidade em ratos com doses de 40 mg/kg/dia (aproximadamente 10 vezes a dose humana máxima recomendada baseada em mg/m2) e em coelhos com 160mg/kg por via oral (aproximadamente 40 vezes a dose humana máxima recomendada com base em mg/m2). Porém, a pioglitazona não foi teratogênica43 em ratos com doses orais até 80mg/kg, nem em coelhos com doses até 160mg/kg durante a organogênese (17 vezes e 40 vezes a dose humana máxima recomendada em mg/m2, respectivamente). Foi observada restrição do crescimento fetal, o que foi atribuída à ação de pioglitazona ao diminuir a hiperinsulinemia44 materna normal já que o aumento da resistência à insulina45 causada pela gravidez38 é necessária para o crescimento fetal.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Categoria de risco: C
Lactação46: este produto não deve ser administrado em mulheres em fase de amamentação47, ou a amamentação47 deve ser descontinuada se o uso deste produto for considerado essencial.
A pioglitazona está presente no leite de ratas durante o período de lactação46 que estavam sob tratamento, apesar de não se saber se esta é secretada no leite humano. A pioglitazona não deve ser administrada em mulheres durante o período de amamentação47.
- 6. INTERAÇÕES MEDICAMENTOSAS
Hipoglicemia48 pode ocorrer quando pioglitazona é administrada com sulfonilureia ou insulina8 – Um inibidor de CYP2C8 (como genfibrozila) pode elevar a ASC de pioglitazona e um indutor de CYP2C8 (como rifampicina) pode reduzir a ASC de piglitazona.
Foi relatado que a co-administração de pioglitazona com genfibrozila resulta em um aumento de três vezes na ASC de pioglitazona. Uma vez que a pioglitazona apresenta um potencial para efeitos adversos relacionados com a dose, uma diminuição da dose de pioglitazona pode ser necessária quando genfibrozila for administrado concomitantemente.
Foi relatado que a co-administração de pioglitazona com rifampicina resulta em uma diminuição de 54% na ASC de pioglitazona. Pode ser necessário aumentar a dose de pioglitazona em função da resposta clínica quando a rifampicina é administrada concomitantemente.
Estudos de interação demonstraram que a pioglitazona não afeta a farmacocinética ou farmacodinâmica da digoxina, varfarina, femprocumona ou metformina35, e em coadministração com sulfonilureias49 não parece afetar a farmacocinética da sulfonilureia. Estudos em humanos não mostram indução dos principais citocromos induzidos P450, 1A, 2C8/9 e 3A4. Estudos in vitro não demonstraram inibição de qualquer subtipo dos citocromos P450; interações com substâncias metabolizados por estas enzimas, por exemplo, contraceptivos orais, ciclosporina, bloqueadores do canal de cálcio e os inibidores de reductase HMGCoA não são esperados.
Os pacientes que receberam pioglitazona em combinação com insulina8 ou hipoglicemiantes orais50 podem correr risco de desenvolverem hipoglicemia48.


