
POSOLOGIA E MODO DE USAR ACTOS
A dose inicial recomendada de ACTOS (cloridrato de pioglitazona) é 15mg ou 30mg, e a faixa de dose aprovada é de 15 a 45mg. O medicamento deve ser administrado uma vez por dia, por via oral, independentemente da alimentação.
Resumo de observações especiais da posologia em populações específicas
Pacientes idosos
Nenhum ajuste de dose é necessário para pacientes1 idosos. Deve-se iniciar o tratamento com a menor dose disponível e aumentar a dose gradualmente, particularmente quando o medicamento é usado em combinação com insulina2.
Pacientes pediátricos
A segurança e eficácia de ACTOS (cloridrato de pioglitazona) em pacientes pediátricos ainda não foi estabelecida.
Insuficiência renal3
Nenhum ajuste de dose é necessário para pacientes1 com insuficiência renal3. Não há informação disponível sobre pacientes em diálise4; desta forma, ACTOS® (cloridrato de pioglitazona) não deve ser utilizado nestes pacientes.
Insuficiência hepática5
Não se deve iniciar o tratamento em pacientes com doença hepática6 ativa ou TGP aumentado (maior que 2,5 vezes o limite da normalidade).
Insuficiência cardíaca7
Em pacientes com Insuficiência Cardíaca Congestiva8 (classes I ou II pela New York Heart Association - NYHA), a dose inicial recomendada é 15mg. Não inicie em pacienties com Insuficiência Cardíaca Congestiva8 (classes III ou IV pela NYHA).
- 9. REAÇÕES ADVERSAS
Edema9
Aumento de peso corporal
Reduz níveis de hemoglobina10 e hematócrito11
Aumento (ou elevação) da creatina quinase (creatinafosfoquinase) – insuficiência cardíaca7 Disfunção hepatocelular*
Edema macular12*
Fratura13 ósseas em mulheres*
*Eventos pós-comercialização
Cardiovasculares: Em ensaios clínicos14 controlados com placebo15, que excluíram pacientes com insuficiência cardíaca7 NYHA classes III e IV, a incidência16 de eventos adversos cardíacos graves relacionados com a expansão de volume não foi aumentada em pacientes tratados com pioglitazona como monoterapia ou em combinação com sulfoniluréias17 ou metformina18 versus pacientes tratados com placebo15. Em estudos de combinação com insulina2, um pequeno número de pacientes com doença cardíaca previamente existente desenvolveram insuficiência cardíaca congestiva8 quando tratados com pioglitazona em combinação com insulina2 (para detalhes, ver item 5. ADVERTÊNCIAS E PRECAUÇÕES). Os pacientes com insuficiência cardíaca7 NYHA classes III e IV não foram estudados nestes ensaios clínicos14.
Na experiência pós-comercialização com pioglitazona, os casos de insuficiência cardíaca congestiva8 têm sido relatados em pacientes com e sem doença cardíaca previamente conhecida.
Edema9: Em ensaios clínicos14, o edema9 foi relatado mais freqüentemente em pacientes tratados com pioglitazona do que nos pacientes tratados com placebo15 e parece estar relacionado com a dose. Também foram recebidos relatos pós-comercialização de início ou agravamento do edema9.
Ganho de peso: O ganho de peso relacionado com a dose foi observado com a pioglitazona isoladamente e em combinação com outros agentes hipoglicêmicos. O mecanismo de ganho de peso não é claro, mas é considerado ser uma combinação de retenção de líquidos e acúmulo de gordura subcutânea19, que é menos metabolicamente ativa do que a gordura20 intestinal. O ganho de peso nos estudos clínicos foi na faixa de 3 - 5 kg, e diminuiu após os primeiros 6 meses de tratamento.
Ovulação21: A terapia com pioglitazona, como outras tiazolidinedionas, pode resultar em ovulação21 em algumas mulheres pré-menopausadas, anovulatórias. Como resultado, estes pacientes podem apresentar um risco maior de gravidez22 ao tomar pioglitazona (ver item 5. ADVERTÊNCIAS E PRECAUÇÕES). Assim, a contracepção23 adequada em mulheres na pré-menopausa24 é recomendada. A freqüência de ocorrência desse efeito não é conhecida, uma vez que não foi investigado em estudos clínicos.
Hematologia: A pioglitazona pode causar reduções nos níveis de hemoglobina10 e hematócrito11 (ver também item 5. ADVERTÊNCIAS E PRECAUÇÕES). Em estudos clínicos, essas alterações ocorreram principalmente nas primeiras 4 - 12 semanas de tratamento e se manteve relativamente constante a partir daí. Acredita-se estar relacionada com o aumento do volume do plasma25 e têm sido raramente associada a qualquer causa hematológica significativa clínica.
Efeitos hepáticos: Em estudos clínicos controlados com placebo15 pré-aprovação, 4 de 1526 (0,26%) dos pacientes tratados com pioglitazona e 2 de 793 (0,25%) pacientes tratados com placebo15 tinham níveis de TGP 3 vezes maiores que o limite superior da normalidade. As elevações de TGP com pioglitazona foram reversíveis e não foram claramente relacionadas com a administração de pioglitazona.
Foram recebidos relatos pós-comercialização de aumento de 3 ou mais vezes de casos de hepatite26 e de elevação de enzimas hepáticas27 acima do limite superior da normalidade. Muito raramente, estes relatos têm envolvido insuficiência hepática5 com e sem desfecho fatal, apesar da causalidade não ter sido estabelecida.
Recomenda-se que os pacientes tratados com pioglitazona façam uma monitorização periódica das enzimas hepáticas27. Para o gerenciamento do tratamento com pioglitazona em relação à função hepática6, ver item 5. ADVERTÊNCIAS E PRECAUÇÕES.
Fraturas ósseas em mulheres: O papel dos agonistas de PPARγ no metabolismo28 ósseo humano não está claro. Estudos toxicológicos pré-clínicos de pioglitazona não indicam qualquer efeito sobre os ossos em estudos com uma duração de até um ou dois anos em ratos, cães ou macacos - estudos de longo prazo com ratos mostraram efeitos ósseos, mas são de difícil interpretação porque há crescimento de ossos ao longo da vida nestas espécies.
Em estudos clínicos controlados, uma taxa de notificação de fraturas mais elevada foi reportada em mulheres tratadas com pioglitazona (2,6%) em comparação com as mulheres tratadas com outros agentes anti-diabéticos ou placebo15 (1,7%).
Além disso, uma taxa de notificação de fraturas ligeiramente maior foi observada em indivíduos com 65 anos ou mais, e uma incidência16 maior de fraturas foi observada após a exposição entre 1 a 2 anos à pioglitazona, embora a exposição à pioglitazona por mais de 2 anos não foi claramente associada a um aumento na incidência16 de fraturas.
Em um estudo randomizado29 (PROactive) em pacientes com diabetes30 tipo II (9,5 anos de duração média da diabetes30), um aumento na incidência16 de fraturas ósseas foi observado em pacientes do sexo feminino sob tratamento com pioglitazona. Durante um follow-up médio de 34,5 meses, a incidência16 de fraturas ósseas nas mulheres foi de 5,1% para a pioglitazona contra 2,5% para o placebo15. Esta diferença foi observada após o primeiro ano de tratamento e se manteve durante o decurso do estudo . A maioria das fraturas observadas em pacientes do sexo feminino foram as fraturas não-vertebrais, incluindo o membro inferior e membro superior distal31. Não foi observado aumento das taxas de fraturas em homens tratados com pioglitazona (1,7%) versus placebo15 (2,1%).
O risco de fratura13 deve ser considerado no tratamento de pacientes, principalmente em pacientes do sexo feminino tratadas com pioglitazona, e deve ser dada atenção à avaliação e manutenção da saúde32 óssea de acordo com padrões atuais de tratamento.
Edema macular12: Relatos pós-comercialização de nova ocorrência ou agravamento de edema macular12 diabético com diminuição da acuidade visual33 com o uso de tiazolidinedionas, incluindo pioglitazona, foram relatados muito raramente. Uma associação direta entre a pioglitazona e o edema macular12 é desconhecida. Os médicos devem considerar a possibilidade de edema macular12 se o paciente relatar diminuição da acuidade visual33.
A fim de elucidar esta questão, Bartsch et al. (2007, dados não publicados) conduziram um estudo prospectivo34 de segurança de 19 indivíduos (os olhos35 de 37 foram examinados, 17 no grupo de tratamento ativo e 20 no grupo placebo15), que foram submetidos a um tratamento duplo-cego placebo15-controlado com pioglitazona para o diabetes30.A dose foi administrada com insulina2 mais placebo15 e insulina2 mais pioglitazona, a qual foi administrada a 30mg por dia durante duas semanas, seguida de 45mg por dia durante 10 semanas. A acuidade visual33 foi monitorada no início do estudo e após três meses. A visão36 foi monitorada utilizando tabela ETDRS a 4m e o volume da retina37 foi avaliado com a tomografia de coerência óptica (Stratus OCT) usando o mapa macular rápido e protocolos de mapa macular. A medida do volume OCT mostrou um aumento nos olhos35 de 7 e de 11 indivíduos para os grupos ativo e placebo15, respectivamente. A diminuição do volume foi medida nos olhos35 de 9 e 5 indivíduos para os grupos ativo e placebo15, respectivamente. Os olhos35 de um indivíduo no grupo de tratamento não mostrou nenhuma mudança no volume macular. A análise de visão36 ETDRS não foi alterada nos olhos35 de 4 e 9 indivíduos para os grupos ativo e placebo15, respectivamente. A análise de visão36 ETDRS se mostrou aumentada nos olhos35 de 6 indivíduos, em ambos os grupos e diminuiu nos olhos35 de 7 e 5 indivíduos para os grupos ativo e placebo15, respectivamente.
Nenhum dos olhos35 dos indivíduos apresentou aumento de volume macular maior que 10%.
Alterações da visão36 e do volume macular OCT foram correlacionados nos olhos35 de 11 indivíduos e inversamente correlacionados em olhos35 de 11 indivíduos, enquanto nos olhos35 de 12 indivíduos não mostrou nenhuma correlação.
Concluiu-se que o estudo não observou um aumento significativo no volume macular medida com OCT, que as exacerbações induzidas por glitazona em edema macular12 diabético são eventos raros e idiossincráticos e que um estudo maior foi indicado para determinar sua prevalência38.
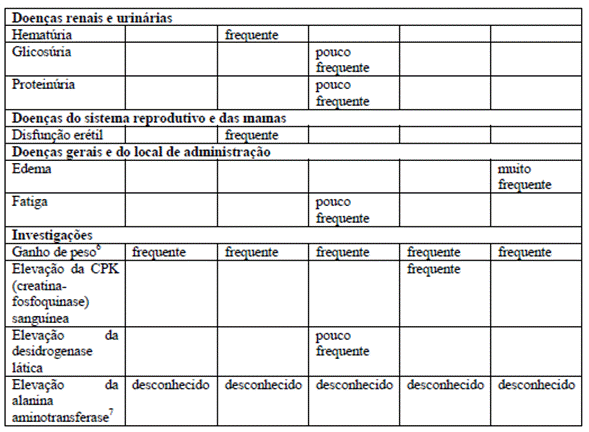
As reações adversas relatadas em excesso (> 0,5%) de placebo15 e como mais do que um caso isolado em pacientes que receberam pioglitazona em estudos duplo-cego estão listadas abaixo de acordo com os termos MedDRA por sistema de órgãos e frequência absoluta. As frequências são definidas como: muito frequentes (≥ 1/10); frequentes (≥ 1/100 a <1/10); pouco frequentes (≥ 1/1 000, <1/100); raros (≥ 1/10 000, <1/1, 000); muito raros (<1/10, 000); desconhecidos (não podem ser calculados a partir dos dados disponíveis). Dentro de cada grupo de frequência, as reações adversas são apresentadas por ordem decrescente de incidência16 e seriedade.


1 Casos pós-comercialização de reações de hipersensibilidade em pacientes tratados com a pioglitazona foram relatados. Estas reações incluem anafilaxia39, angioedema40, e urticária41.
2 Perturbação visual tem sido relatada principalmente no início do tratamento e está relacionada a alterações na glicemia42, devido a alteração temporária na turgescência e índice de refração da lente, como é visto com outros tratamentos de hipoglicemia43.
3 Edema9 foi relatado em 6-9% dos pacientes tratados com a pioglitazona por mais de um ano, em ensaios clínicos14 controlados. As taxas de edema9 nos grupos comparadores (sulfonilureia, metformina18) foram 2-5%. Os relatos de edema9 foram geralmente leves a moderados e usualmente não requiseram a interrupção do tratamento.
4 Em ensaios clínicos14 controlados, a incidência16 de relatos de insuficiência cardíaca7 com pioglitazona foi o mesmo que nos grupos de tratamento com placebo15, metformina18 e sulfonilureias17, mas foi aumentada quando utilizado em terapia combinada44 com insulina2. Em um estudo de evolução de pacientes com doença macrovascular45 grave pré-existente, a incidência16 de insuficiência cardíaca7 grave foi 1,6% mais elevada com pioglitazona do que com placebo15, quando adicionada à terapia que incluía insulina2. No entanto, isto não levou a um aumento da mortalidade46 neste estudo. A insuficiência cardíaca7 tem sido raramente relatada com o uso comercial de pioglitazona, mas com maior frequência quando a pioglitazona foi utilizada em combinação com insulina2 ou em pacientes com história de insuficiência cardíaca7.
5 Foi realizada uma análise conjunta de reações adversas de fraturas ósseas, de estudos clínicos randomizados, duplo-cego, controlados com comparador, em mais de 8.100 pacientes nos grupos tratados com pioglitazona e 7.400 pacientes nos grupos tratados com comparador em até 3,5 anos de duração. A maior taxa de fraturas foi observada em mulheres que tomaram pioglitazona (2,6%) versus o comparador (1,7%). Não foi observado aumento das taxas de fraturas em homens tratados com pioglitazona (1,3%) versus o comparador (1,5%).
No estudo PROactive de 3,5 anos, 44/870 (5,1%) dos pacientes do sexo feminino tratadas com pioglitazona apresentaram fraturas em comparação com 23/905 (2,5%) de pacientes do sexo feminino tratadas com comparador. Não foi observado aumento das taxas de fraturas em homens tratados com pioglitazona (1,7%) versus o comparador (2,1%).
6 Em ensaios controlados com comparador ativo, a média do ganho de peso com pioglitazona administrada como monoterapia foi de 2-3 kg durante um ano. Este valor é semelhante ao observado no grupo de sulfonilureia como comparador ativo. Em ensaios clínicos14 de terapia combinada44 de pioglitazona adicionada à metformina18 resultou em ganho de peso médio ao longo de um ano de 1,5 kg e adicionada à sulfonilureia, de 2,8 kg. Nos grupos comparadores a adição de sulfonilureia à metformina18 resultou em um ganho de peso médio de 1,3 kg e a adição de metformina18 à sulfonilureia uma perda média de peso de 1,0 kg.
7 Em ensaios clínicos14 com pioglitazona, a incidência16 de elevações de TGP maior do que três vezes o limite superior da normalidade foi igual ao placebo15, mas inferior ao verificado com grupos comparadores de metformina18 ou sulfonilureia. Os níveis médios de enzimas hepáticas27 diminuíram com o tratamento com pioglitazona. Casos raros de elevação das enzimas hepáticas27 e disfunção hepatocelular ocorreram na experiência pós-comercialização. Embora em casos muito raros, tenham sido notificados resultados fatais, nenhuma relação causal foi estabelecida.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em http://www.anvisa.gov.br/ hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.


