
CARACTERÍSTICAS FARMACOLÓGICAS KLARICID IV
Claritromina é um antibiótico macrolídeo semi-sintético obtido pela substituição do grupo CH3O pelo hidroxilo (OH) na posição 6 do anel lactônico da eritromicina. Especialmente para a claritromicina é a 6-O-metil-eritromicina. A claritromicina é um pó branco ou esbranquiçado, amargo e praticamente sem cheiro, insolúvel em água, levemente solúvel em metanol, etanol e acetonitrila, e praticamente insolúvel em água. O peso molecular é 747,96.
Microbiologia
A claritromicina exerce sua ação antibacteriana através de sua ligação às subunidades ribossômicas 50S dos agentes patogênicos sensíveis, suprimindo-lhes a síntese protéica.
A claritromicina apresenta excelente atividade in vitro tanto contra cepas1 padronizadas de bactérias quanto de bactérias isoladas na clínica. A claritromicina é altamente potente contra uma grande variedade de organismos Gram-positivos e Gram-negativos aeróbios e anaeróbios. As concentrações inibitórias mínimas (CIMs) da claritromicina geralmente são uma diluição log2 mais potentes do que as CIMs da eritromicina.
Os dados in vitro também indicam que a claritromicina apresenta uma excelente atividade contra Legionella pneumophila, Mycoplasma pneumoniae e Helicobacter pylori. Esta atividade é maior em pH neutro do que em pH ácido. Dados in vitro e in vivo mostram que este antibiótico apresenta atividade contra espécies de micobactérias clinicamente significantes. Os dados in vitro indicam que espécies de Enterobacteriaceae e de pseudomonas e outros bacilos Gram-negativos não fermentadores de lactose2 não são sensíveis a claritromicina.
A claritromicina tem se mostrado ativa contra a maioria das cepas1 dos seguintes microorganismos, tanto in vitro quanto em infecções3 clínicas:
Micro-organismos Gram-positivos aeróbios: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Listeria monocytogenes.
Micro-organismos Gram-negativos aeróbios: Haemophilus influenzae, Haemophilus parainfluenzae, Moraxella catarrhalis, Neisseria gonorrhoeae, Legionella pneumophila.
Outros micro-organismos: Mycoplasma pneumoniae, Chlamydia pneumoniae (TWAR).
Micobactérias: Mycobacterium leprae, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium avium complex (MAC) consistindo de: Mycobacterium avium e Mycobacterium intracellulare.
A produção de betalactamase não deve apresentar efeitos sobre a atividade da claritromicina. NOTA: a maioria das cepas1 de estafilococos resistentes à meticilina e à oxacilina são resistentes à claritromicina.
Helicobacter: Helicobacter pylori. Em culturas realizadas antes do tratamento, o H. pylori foi isolado e as CIMs da claritromicina foram determinadas em 104 pacientes. Destes, quatro pacientes apresentavam cepas1 resistentes, dois apresentavam cepas1 com sensibilidade intermediária e 98 apresentavam cepas1 sensíveis.
Os seguintes dados in vitro estão disponíveis, mas seu significado clínico é desconhecido. A claritromicina apresenta atividade in vitro contra a maioria das cepas1 dos seguintes microorganismos; entretanto, a segurança e eficácia da claritromicina no tratamento de infecções3 clínicas devidas a esses microorganismos ainda não foram estabelecidas em estudos clínicos adequados e bem controlados.
Micro-organismos Gram-positivos aeróbios: Streptococcus agalactiae, Streptococci (Grupos C, F e G), Streptococcus viridans.
Micro-organismos Gram-negativos aeróbios: Bordetella pertussis, Pasteurella multocida.
Micro-organismos Gram-positivos anaeróbios: Propionibacterium acnes, Clostridium perfringens, Peptococcus niger.
Micro-organismos Gram-negativos anaeróbios: Bacteroides melaninogenicus.
Espiroquetas: Borrelia burgdorferi, Treponema pallidum.
Campilobacter: Campylobacter jejuni.
O principal metabólito4 da claritromicina em humanos e outros primatas é o metabólito4 microbiologicamente ativo 14-OH-claritromicina.
Este metabólito4 é tão ativo quanto, ou 1 a 2 vezes menos ativo do que a substância-mãe para a maioria dos microorganismos, exceto contra o H. influenzae contra o qual é duas vezes mais ativo. A substância-mãe e o metabólito4 14-OH exercem tanto atividade aditiva quanto efeito sinérgico sobre o H. influenzae in vitro e in vivo, dependendo da cepa5 bacteriana.
A claritromicina se mostrou duas a dez vezes mais ativa do que a eritromicina em vários modelos experimentais em animais. Foi demonstrado, por exemplo, que ela é mais ativa do que a eritromicina em infecções3 sistêmicas, em abscessos6 subcutâneos e infecções3 do trato respiratório em camundongos, causadas por S. pneumoniae, S. aureus, S. pyogenes e H. influenzae. Em cobaias com infecção7 por Legionella este efeito foi mais pronunciado; uma dose intraperitoneal de 1,6 mg/kg/dia de claritromicina foi mais efetiva do que 50 mg/kg/dia de eritromicina.
Testes de Sensibilidade
Os métodos quantitativos que requerem medida dos diâmetros das zonas fornecem estimativas mais precisas da sensibilidade antibiótica.
Um procedimento recomendado utiliza discos impregnados com 15 mcg de claritromicina para testar a sensibilidade (teste de difusão de Kirby-Bauer); as interpretações correlacionam o diâmetro das zonas do disco de teste com os valores das CIMs para a claritromicina. As CIMs são determinadas pelo método de diluição em caldo ou ágar. Com este procedimento, um relatório do laboratório de “sensível” indica que o organismo infectante provavelmente responderá ao tratamento. Um relatório de “resistente” indica que o organismo infectante provavelmente não responderá ao tratamento. Um relatório de “sensibilidade intermediária” sugere que o efeito terapêutico da substância pode ser duvidoso ou que o organismo poderia ser sensível se fossem utilizadas doses maiores (este último também é referido como “moderadamente sensível”).
Propriedades Farmacocinéticas
Distribuição, Biotransformação e Eliminação
Em um estudo clínico de dose única em voluntários, a claritromicina foi administrada por via intravenosa nas doses de 75 mg, 125 mg, 250 mg e 500 mg, em volumes de 100 mL infundidos durante 30 minutos, e 500 mg, 750 mg ou 1000 mg, em volumes de 250 Ml infundidos durante 60 minutos. Os picos de concentração média (Cmax) da substância-mãe variaram de 5,16 mcg/mL após 500 mg, a 9,40 mcg/mL após 1000 mg (60 minutos de infusão). O pico da concentração média (Cmax) do metabólito4 14-OH-claritromicina variou de 0,66 mcg/mL após a dose de 500 mg até 1,06 mcg/mL após a dose de 1000 mg (infusão em 60 minutos).
A meia-vida sérica média, na fase terminal, da substância-mãe foi dose-dependente, variando de 3,8 horas após 500 mg a 4,5 horas após 1000 mg (60 minutos de infusão). A meia-vida plasmática média estimada para o metabólito4 14-hidroxilado apresentou alguns aumentos dependentes da dose com as doses mais elevadas e variou de 7,3 horas após a dose de 500 mg até 9,3 horas após a dose de 1000 mg (infusão em 60 minutos). A média da área sob a curva concentração vs tempo (ASC) apresentou um aumento não linear dependente da dose para a substância-mãe de 22,29 h.mcg/mL após a dose de 500 mg, para 53,26 h.mcg/mL após a dose de 1000 mg. A média da área
sob a curva concentração vs tempo (ASC) para o metabólito4 14-hidroxilado variou de 8,16 h.mcg/mL após a dose de 500 mg para 14,76 h.mcg/mL após a dose de 1000 mg (infusão em 60 minutos).
Em um estudo clínico de doses múltiplas no período de 7 dias, pacientes receberam infusões de 125 mg e 250 mg de claritromicina por via intravenosa, em volumes de 100 mL durante 30 minutos, ou 500 mg e 750 mg, em volumes de 250 mL durante 60 minutos; as doses foram administradas com intervalos de 12 horas.
Nesse estudo, os picos médios de concentração de claritromicina (Cmax) no “steady-state” aumentaram de 5,5 mcg/mL com doses de 500 mg para 8,6 mcg/mL com doses de 750 mg. A meia-vida aparente terminal foi de 5,3 horas após a infusão da dose de 500 mg durante 60 minutos e 4,8 horas após a infusão da dose de 750 mg durante 60 minutos.
A Cmax no “steady-state” observada para o metabólito4 14-hidroxi aumentou de 1,02 mcg/mL com a dose de 500 mg para 1,37 mcg/mL com a dose de 750 mg. As meias-vidas da fase terminal para este metabólito4 foram de 7,9 horas e 5,4 horas para os grupos das doses de 500 mg e 750 mg, respectivamente. Não se evidenciou nenhuma tendência relacionada com a dose.
A claritromicina administrada em doses orais de 250 mg a cada 12 horas, apresenta picos de concentração plasmática em 2 a 3 dias com média de 1 mcg/mL de claritromicina e 0,6 mcg/mL para o seu metabólito4 14-OH-claritromicina, enquanto que a meia-vida de eliminação foi de 3 a 4 horas para a claritromicina e 5 a 6 horas para o seu metabólito4 14-OH. Quando a administração é em doses de 500 mg a cada 12 horas, a Cmax no steady-state da claritromicina e seu metabólito4 hidroxilado foi atingida a partir da quinta dose. Após a quinta e sétima doses, a Cmax no “steady-state” alcançada foi de 2,7 e 2,9 mcg/mL; seu metabólito4 hidroxilado atingiu 0,88 e 0,83 mcg/mL, respectivamente. A meia-vida da claritromicina na dose de 500 mg é de 4,5 a 4,8 horas e a do seu metabólito4 14-OH é de 6,9 a 8,7 horas. A concentração de 14-OH-claritromicina não aumenta proporcionalmente com a dose de claritromicina, e aparentemente a meia-vida das duas substâncias tendem a ser mais longas com doses maiores. Esse comportamento farmacocinético não linear da claritromicina, associado com o decréscimo global na formação dos produtos 14-hidroxilados e N-dimetilados com doses maiores, indicam que o metabolismo8 da claritromicina aproxima-se da saturação com altas doses.
O principal metabólito4 encontrado no plasma9 humano é a 14-OH-claritromicina, com níveis de pico de 0,5 mcg/mL e 1,2 mcg/mL após doses orais de 250 mg e 1200 mg, respectivamente. Em humanos recebendo doses orais únicas de 250 mg ou 1200 mg de claritromicina, a excreção urinária atingiu 37,9% da menor dose e 46,0% da dose mais elevada. A eliminação fecal contribuiu com 40,2% e 29,1% (esta incluiu um indivíduo com apenas uma amostra de fezes contendo 14,1%) dessas respectivas doses.
Pacientes
A claritromicina e seu metabólito4 14-OH são facilmente distribuídos nos tecidos e fluidos corporais. A concentração nos tecidos é normalmente maior que a concentração sérica. Exemplos de concentrações séricas nos tecidos e fluídos corporais são apresentados abaixo:

Pacientes com infecções3 por micobactérias
Apesar de não haver dados disponíveis relacionados ao uso de claritromicina por via intravenosa em infecções3 por micobactérias, há dados farmacocinéticos do uso de claritromicina comprimidos nessas infecções3.
As concentrações no “steady-state” da claritromicina e da 14-OH-claritromicina observadas após administração das doses usuais de claritromicina a pacientes adultos infectados pelo HIV10 foram semelhantes àquelas observadas em indivíduos normais. Entretanto, com as doses mais elevadas que podem ser requeridas para tratar infecções3 por micobactérias, as concentrações de claritromicina foram muito superiores àquelas observadas com as doses usuais. As meias-vidas de eliminação pareceram ser aumentadas nestas doses elevadas, quando comparadas com aquelas observadas com as doses usuais em indivíduos normais. As concentrações maiores de claritromicina e as vidas médias de eliminação da substância observadas com essas doses são consistentes com a conhecida não linearidade da farmacocinética da claritromicina.
Dados pré-clínicos de segurança:
Toxicidade11 aguda: claritromicina foi administrada por via intravenosa em camundongos, em dois estudos separados, e a DL50 encontrada foi de 184 mg/kg e 227 mg/kg. Estes valores são várias vezes maiores que a DL50 encontrada em ratos (64 mg base/kg) e são menores que os obtidos após administração em camundongos por outras vias. Os sinais12 de toxicidade11 em ambas espécies foram: diminuição da atividade e do reflexo, ataxia13, tremores, dispneia14 e convulsões.
A autópsia15 e os exames histopatológicos realizados nos camundongos sobreviventes do estudo cuja DL50 encontrada foi de 184 mg/kg não mostraram alterações associadas à administração intravenosa da claritromicina. Entretanto, no outro estudo com camundongos e no estudo com ratos foram encontrados nos animais que tiveram morte aguda, alterações sugestivas de edema pulmonar16, juntamente com pequenas áreas de descoloração vermelho-escuras difusas dos lóbulos dos pulmões17. Embora similares, os efeitos produzidos foram mais tóxicos em ratos do que em camundongos. O modo exato de toxicidade11 não foi determinado. Embora os sinais12 de toxicidade11 aguda tenham sugerido efeitos sobre o sistema nervoso central18, as necrópsias revelaram alterações pulmonares em alguns camundongos e ratos.
A toxicidade11 intravenosa aguda dos vários metabólitos19 foram avaliado em ratos e estão resumidos abaixo:
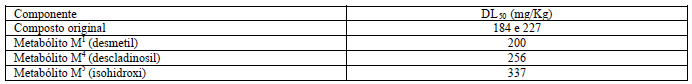
Sinais12 de toxicidade11 incluem inibição do movimento, dificuldade respiratória e convulsão20 clônica. É aparente que a toxicidade11 destes metabólitos19 são comparáveis aos da claritromicina em qualidade e grau.
Irritação venosa aguda: as soluções intravenosas de claritromicina foram avaliadas para irritação na veia periférica da orelha21 de coelhos. Esse estudo demonstrou que administração de dose única em altas concentrações (7,5 mg a 30 mg/mL) apresentou irritação discreta.
Toxicidade11 subaguda22: os estudos tiveram a duração de um mês, empregando-se doses de 15, 50 e 160 mg/kg/dia em ratos e 5, 15 e 40 mg/kg/dia em macacos. As doses mais elevadas testadas na determinação da dose em ratos (entre 20 e 640 mg/kg/dia) e em macacos (entre 5 e 80 mg/kg/dia) se mostraram tóxicas para o fígado23, sistema biliar e rins24, o que foi coerente com os encontrados em órgãos alvos em estudos com administração oral de claritromicina.
A ocorrência de irritação venosa grave nos estudos com duração de um mês, com as doses de 160 mg/kg/dia e 40 mg/kg/dia em ratos e macacos, respectivamente, impediram o estudo de doses elevadas para demonstrar a toxicidade11 nos órgãos alvo. Isso ocorreu apesar dos esforços para maximizar a dose, aumentando o volume de infusão e diminuindo o ritmo de infusão.
As doses sem efeito em ratos e macacos determinadas por estudos subagudos de um mês, foram de 50 e 15 mg/kg/dia, respectivamente, devido a irritação venosa com as doses mais elevadas.
Embriotoxicidade em ratos: Foram administradas doses de 15, 50 e 160 mg base/Kg/dia de claritromicina intravenosa na veia da cauda de ratos. Significantes sinais12 de toxicidade11 materna foram manifestados na dose de 160 mg/Kg/dia (diminuição do consumo de alimentos e do ganho de peso) e 50 mg/Kg/dia (diminuição do consumo de alimentos). Efeitos locais no local de aplicação da dose dos animais, tais como inchaço25, ferida e necrose26 para as doses elevadas. Não foram notados efeitos sobre a incidência27 média de efeitos nos locais de aplicação28 ou reabsorção. Nenhuma alteração visceral ou esquelética foram notadas devido à aplicação de claritromicina, exceto de uma tendência relacionada com a dose na proporção de fetos do sexo masculino com a ausência de um testículo29. Apesar na toxicidade11 materna significante manifestada como irritação das veias30, diminuição do consumo de alimentos e ganho de peso, não há evidência de embriotoxicidade ou teratoxicidade em ambas as doses.
Embriotoxicidade em coelhos: foram administradas doses de 3, 10 e 30 mg base/Kg/dia de claritromicina intravenosa em grupos de ceolhos. Uma coeolha prenha tratada com 3 mg/Kg/dia morreu no dia 29 da gestação.Irritação venosa foi observada tanto no grupo controle quanto no grupo tratado com a droga. A incidência27 e severidade da irritação estiveram diretamente relacionadas à concentração da droga na formulação. Sinais12 de toxicidade11 materna foram observado com 30 mg/Kg/dia (redução do peso e do consumo de alimentos). A incidência27 de aborto no grupo tratado com 30 mg/Kg/dia foi significante maior quando comparado ao grupo controle, mas todos os fetos abortadas eram normais, quando grosseiramente analisados. Nenhum efeitos nos níveis maternos e de toxicidade11 fetal quando 10 e 30 mg/Kg/dia foram administrados, respectivamente.
Embriotoxicidade em macacos: Claritromicina mostrou produzir menor perda embrionária em macacos quando administrada em doses até 10 vezes maiores que a maior estipulada (500 mg duas vezes ao dia) diariamente para humanos, iniciando no dia 20 da gestação.
Estes efeitos foram atribuídos à toxicidade11 materna da driga em doses muito altas. Um estudo adicional em macacos gestantes com dosagem de aproximadamente 2,5 a 5 vezes maiores que a dose usualmente utilizada (500 mg duas vezes ao dia) não produziram perigo exclusivo para o feto31.
Mutagenicidade: foram realizados estudos para avaliar o potencial mutagênico de claritromicina através de sistemas de testes com microssomas hepáticos ativados e não ativados de ratos (teste de Ames). Resultados desses estudos não evidenciaram potencial mutagênico para concentrações iguais ou menores que 25 mcg de claritromicina, por placas32 de Petri. Numa concentração de 50 mcg, a droga foi tóxica para todas as cepas1 testadas.
- 4. CONTRAINDICAÇÕES
KLARICID I.V. é contraindicado para o uso por pacientes com conhecida hipersensibilidade aos antibióticos macrolídeos e a qualquer componente da fórmula.
A administração concomitante de claritromicina com astemizol, cisaprida, pimozida e terfenadina está contraindicada, pois pode resultar em prolongamento QT e arritmias33 cardíacas incluindo taquicardia34 ventricular, fibrilação ventricular e torsades de pointes.
A administração concomitante de claritromicina com alcalóides de ergot (ex: ergotamina ou diidroergotamina) é contraindicada pois, pode resultar em toxicidade11 por ergot.
A coadministração de claritromicina e midazolam oral é contraindicada (ver Interações Medicamentosas).
A claritromicina não deve ser administrada a pacientes com histórico de prolongamento do intervalo QT ou arritmia35 ventricular cardíaca, incluindo torsades de pointes (ver Advertências e Precauções e Interações medicamentosas).
Claritromicina não deve ser indicada para pacientes36 com hipocalemia37 (risco de prolongamento do intervalo QT).
Claritromicina não deve ser usada em pacientes que sofrem de insuficiência hepática38 grave em combinação com insuficiência renal39.
A claritromicina não deve ser utilizada concomitantemente com inibidores da HMG-CoA redutase (estatinas) que são extensivamente metabolizados pela CYP3A4 (lovastatina ou sinvastatina), devido a um aumento no risco de miopatia40, incluindo rabdomiólise41 (ver Advertências e Precauções).
Claritromicina (e outros inibidores fortes de CYP3A4) não deve ser utilizada em combinação com colchicina (ver Advertências e Precauções e Interações Medicamentosas).
A administração concomitante com ticagrelor ou ranolazina é contraindicada.
Gravidez42: Categoria de risco: C


