INDICAÇÕES DACARB
DACARB® (dacarbazina) é indicada no tratamento de melanoma1 maligno metastático. Além disto, DACARB® (dacarbazina) é indicada na doença de Hodgkin2, como uma terapia de segunda linha, quando em combinação com outros agentes eficazes.
- 2. RESULTADOS DE EFICÁCIA:
- Melanoma1 maligno:
A eficácia da dacarbazina no tratamento do melanoma1 metastático foi avaliada em vários estudos clínicos. Segundo a revisão de Serrone e cols1, a monoterapia com dacarbazina determina uma taxa de resposta objetiva de aproximadamente 20%, com uma duração de resposta mediana de 5 (cinco) a 6 (seis) meses e taxas de resposta completa de 5%.
No estudo de Middleton e cols.2, a dacarbazina na dose inicial de 250 mg/m2/dia durante 5 (cinco) dias a cada 21 (vinte e um) dias foi administrada a 149 (cento e quarenta e nove) pacientes ≥ 18 (dezoito) anos de idade portadores de melanoma1 metastático avançado cirurgicamente irresecável. Os pacientes deveriam ter doença mensurável e performance status (OMS) 2. Foram excluídos pacientes que já haviam recebido tratamento prévio para doença metastática3 (exceto radioterapia4 local), ou que apresentavam metástases5 em sistema nervoso central6 (SNC7). Na população com intenção de tratamento (ITT), o tempo de sobrevida8 mediano foi de 6,4 meses e o tempo de sobrevida8 livre de progressão mediano foi de 1,5 meses. Resposta completa (RC), parcial (RP) e estabilização da doença foram observadas, respectivamente, em 2,7%, 9,4% e 15,8% dos pacientes tratados. Dentre os pacientes respondedores (RC e RP), o tempo de sobrevida8 global mediano foi de 20 (vinte) meses.
Vários estudos avaliaram regimes de quimioterapia9, ou bioquimioterapia, contendo dacarbazina. Legha e cols.3 analisaram a atividade antitumoral e a toxicidade10 do regime, contendo cisplatina (20 mg/m2/d por 4 (quatro) dias), vimblastina (1,6 mg/m2/d por 4 (quatro) dias) e dacarbazina (800 mg/m2 IV no dia 1 (um)) em combinação com interferon alfa (5 x 106 U/m2/d SC por 5 dias) e interleucina-2 (9 x 106 UI/m2/d IV por infusão contínua, por 4 (quatro) dias), repetidos a intervalos de 21 (vinte e um) dias, em 53 (cinquenta e três) pacientes portadores de melanoma1 metastático com lesões11 mensuráveis, performance status (ECOG) 2 e sem metástases5 sintomáticas em SNC7. A resposta foi avaliada após dois ciclos, e os pacientes que responderam continuaram o tratamento até um total de seis ciclos. Onze pacientes (21%) alcançaram RC e 23 (vinte e três) pacientes (43%) alcançaram RP, totalizando 64% de resposta objetiva global, a qual teve duração mediana de 6,5 meses. Considerando-se todos os pacientes, o tempo mediano para progressão da doença foi de 5 (cinco) meses e a sobrevida8 mediana foi de 11,8 meses.
Eton e cols.4 realizaram um estudo clínico de fase III para comparar os efeitos da quimioterapia9 com cisplatina, na dose de 20 mg/m2, nos dias 1- 4 e 22-25, vimblastina na dose de 2 mg/m2 nos dias 1-4 e 22-25 e dacarbazina 800 mg/m2 nos dias 1 e 22 (CVD), com aqueles da bioquimioterapia sequencial, que consistia no regime CVD (com vimblastina na dose de 1,5 mg/m2) mais interleucina-2 administrada como infusão contínua em 24 (vinte e quatro) horas, na dose de 9 MUI/m2, nos dias 5-8, 17-20 e 26-29 e interferon alfa-2b, na dose de 5 MU/m2 SC, nos dias 5-9, 17-21 e 26-30. Cada curso de tratamento consistia de dois ciclos de 21 (vinte e um) dias de quimioterapia9 dados em um período de 6 (seis) semanas. Os pacientes foram avaliados a cada 6 (seis) semanas e aqueles com evidência de redução tumoral repetiam o tratamento. Dentre os 190 (cento e noventa) pacientes incluídos, 91 (noventa e um) foram avaliáveis para o regime de bioquimioterapia e 92 (noventa e dois) para o regime de quimioterapia9. As taxas de resposta foram de 48% para a bioquimioterapia e 25% para a quimioterapia9 (p=0,001), enquanto o tempo para progressão mediano foi de 4,9 e 2,4 meses, e a sobrevida8 mediana foi de 11,9 e 9,2 meses, respectivamente. Naqueles pacientes que apresentaram RC ou RP ao tratamento, a sobrevida8 mediana foi de 18,7 meses no grupo que recebeu bioquimioterapia e 15,4 meses no grupo que recebeu quimioterapia9.
Atkins e cols.5 randomizaram 395 (trezentos e noventa e cinco) pacientes portadores de melanoma1 metastático progressivo com doença mensurável e com performance status (ECOG) < 2 para receber o regime CVD (cisplatina 20 mg/m2/d nos dias 1-4; vimblastina 1,2 mg/m2/d nos dias 1-4; dacarbazina 800 mg/m2 no dia 1; n=195) isoladamente, ou em combinação com interleucina-2 (9 MUI/m2 nos dias 1-4) e interferon alfa-2b (5 MU/m2 nos dias 1-5, 8, 10 e 12; n=200) a cada 21 (vinte e um) dias por um máximo de quatro ciclos. A resposta tumoral foi avaliada após os ciclos 2 (dois) e 4 (quatro) e, a seguir, a cada 3 (três) meses. A taxa de resposta foi de 19,5% no grupo que recebeu bioquimioterapia, e 13,8% no grupo CVD (p =0,140). A sobrevida8 livre de progressão mediana foi significativamente mais longa com o regime de bioquimioterapia que com o regime CVD (4,8 versus 2,9 meses; p = 0,015), embora isso não tenha se traduzido em vantagem na sobrevida8 global mediana (9,0 versus 8,7 meses), ou na porcentagem de pacientes vivos após 1 (um) ano (41% versus 36,9%).
- Doença de Hodgkin2:
A eficácia da dacarbazina, como parte do regime ABVD, foi avaliada em vários estudos clínicos, no tratamento da Doença de Hodgkin2. Duggan e cols6 compararam o regime que alterna os esquemas MOPP (mecloretamina, vincristina, procarbazina e prednisona) e ABV (MOPP/ABV) com o regime ABVD (doxorrubicina 25 mg/m2, bleomicina 10 mg/m2, vimblastina 6 mg/m2 e dacarbazina 375 mg/m2 nos dias 1 e 15) isoladamente em portadores de Doença de Hodgkin2 avançada. Um total de 856 (oitocentos e cinqüenta e seis) pacientes com doença histologicamente confirmada nos estádios III2A, IIIB, ou IV, ou que haviam experimentado recidiva12 após radioterapia4 foram randomizados para uma das duas modalidades de tratamento. As taxas de remissão completa (76% versus 80%), sobrevida8 livre de falência em 5 (cinco) anos (63% versus 66%) e sobrevida8 global em 5 (cinco) anos (82% versus 81%) foram semelhantes entre os grupos ABVD e MOPP/ABV, respectivamente. Uma vez que o regime MOPP/ABV foi associado com maior incidência13 de toxicidade10 aguda pulmonar e hematológica (efeitos adversos de outras drogas antineoplásicas), síndrome14 mielodisplásica e leucemia15, os autores concluíram que o regime ABVD deveria ser considerado o regime padrão no tratamento da doença de Hodgkin2 avançada.
Straus e cols7 tiveram como objetivo determinar se a combinação de quimioterapia9 e radioterapia4 (terapia combinada16) era superior à quimioterapia9 isoladamente em portadores de Doença de Hodgkin2 nos estádios IA, IB, IIA, IIB e IIIA sem massa tumoral. Os pacientes foram randomizados para receber seis ciclos do regime ABVD a cada 28 (vinte e oito) dias isoladamente ou seguido de radioterapia4 (3600 cGy). Dos 69 (sessenta e nove) pacientes avaliáveis em cada grupo, 94% alcançaram remissão completa. Em 60 (sessenta) meses, a duração da remissão completa e sobrevida8 global no grupo de terapia combinada16 versus ABVD isoladamente foram 91% versus 87% e 97% versus 90%, respectivamente, não se evidenciando diferenças estatisticamente significativas entre as duas modalidades de tratamento.
Bonadonna e cols8 compararam o tratamento com quatro ciclos do regime ABVD seguido por irradiação nodal subtotal, ou por radioterapia4 da área envolvida em 136 (cento e trinta e seis) pacientes, com doença de Hodgkin2 nos estádios IA, IB e IIA. Remissão completa foi alcançada em 100% e 97% dos pacientes, e as taxas de sobrevida8 global foram de 96% e 94%, respectivamente. Os autores concluíram que o regime ABVD seguido por radioterapia4 da área envolvida pode ser considerado uma modalidade de tratamento efetiva e segura na Doença de Hodgkin2 inicial.
Engert e cols9 compararam a terapia combinada16 (dois ciclos de ABVD seguidos por radioterapia4 estendida) com a radioterapia4 estendida isoladamente em 650 (seiscentos e cinquenta) pacientes com Doença de Hodgkin2 recém-diagnosticada nos estádios IA a IIB. Após um período de observação mediano de 87 (oitenta e sete) meses, não houve diferenças entre os dois grupos de tratamento, na taxa de RC (95% e 94%, respectivamente) e na sobrevida8 global (92% e 94%, respectivamente); porém, houve mais recidivas17 nos pacientes tratados apenas com radioterapia4 (22%) em relação aos que receberam terapia combinada16 (3%), o que demonstrou que esta última é mais eficaz que a radioterapia4 isolada.
Os resultados do tratamento para Linfoma18 de Hodgkin em pediatria com esquemas quimioterápicos que incluem a dacarbazina tem se mostrado animadores.
Weiner et al10 conduziram um estudo randomizado19 empregando 8 ciclos de MOPP (mostarda nitrogenada, vincristina, procarbazina e prednisona) e ABVD (doxorrubicina, bleomicina, vimblastina e dacarbazina), associado ou não a radioterapia4 em baixas doses, em 183 crianças e adolescentes com estadio IIB, IIIA2, IIIB e IV. A remissão completa foi obtida em 90% dos casos após o término dos oito ciclos de quimioterapia9. A sobrevida8 livre de eventos e a sobrevida8 global estimadas em 5 anos foi de 79% e 92%, respectivamente. A sobrevida8 livre de eventos em 5 anos para o grupo que recebeu apenas quimioterapia9 foi de 79%, enquanto para aqueles que receberam também radioterapia4 foi de 80%, sugerindo que, com o advento da quimioterapia9 MOPP-ABVD, a radioterapia4 em baixas doses não melhora a SLE e a SG nesses pacientes.
Estudo retrospectivo20 brasileiro avaliou 69 crianças entre 2 e 18 anos (mediada de 11 anos) com doença de Hodgkin2. Até 1996, a terapia utilizada era adriamicina, bleomicina, vimblastina e dacarbazina / vincristina, procarbazina, prednisona e adriamicina (ABVD/OPPA). Após 1996, a terapia utilizada foi ABVD. A sobrevida8 global com resposta completa foi de 94,2%, a SLE foi de 87% e a duração mediana de seguimento de 82 meses (12-332 meses)14.
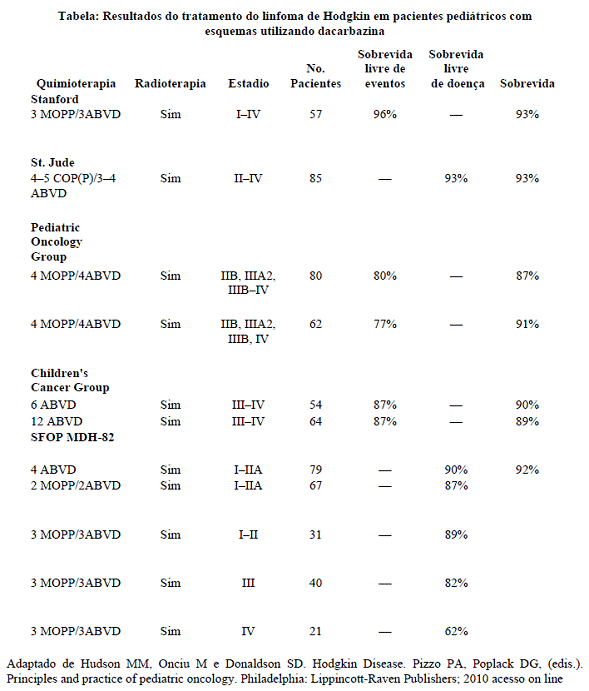
A tabela abaixo compila os resultados do tratamento do linfoma18 de Hodgkin em pacientes pediátricos com esquemas utilizando dacarbazina15.