
USO PEDIÁTRICO (ACIMA DE DOIS ANOS DE IDADE DACARB
A dosagem recomendada de dacarbazina no tratamento da Doença de Hodgkin1 na população pediátrica é de 375 mg/m2, em combinação com outras doses eficazes, nos dias 1e 15 do curso de tratamento. O tratamento deve ser repetido a cada 4 (quatro) semanas, contando a partir do dia 1 de tratamento.
- 9. REAÇÕES ADVERSAS:
As reações tóxicas mais frequentemente observadas são sintomas2 de anorexia3, náusea4 e vômito5. Mais de 90% dos pacientes são afetados com as doses iniciais. Os vômitos6 persistem por 1 (um) – 12 (doze) horas e são atenuados com fenobarbital e/ou proclorperazina. Raramente, em casos de náusea4, ou vômito5, houve necessidade de descontinuação da terapia. É muito rara a ocorrência de casos de diarreia7. Propõe-se a restrição ao paciente da ingestão de alimentos por 4 (quatro) – 6 (seis) horas, antes do tratamento. A rápida tolerância a esses sintomas2 sugere que um mecanismo do SNC8 possa estar envolvido, e geralmente estes sintomas2 diminuem após o primeiro, ou segundo dia. Alguns pacientes experimentam sintomas2 semelhantes à gripe9, com febre10 a 39°C, mialgias11 e mal-estar. Estes sintomas2 geralmente ocorrem após administração de uma dose única elevada; podem persistir por vários dias e podem acontecer com tratamentos sucessivos. Alopécia12, rubor facial e parestesia13 facial foram observados. Foram relatados poucos casos de anormalidades nos testes de função renal14 (Achado anormal de exame químico do sangue15, não especificado), ou hepática16 em seres humanos, após a administração de DACARB® (dacarbazina). Raramente, podem ocorrer reações de fotossensibilidade. Entretanto, estas anormalidades foram constatadas mais frequentemente nos estudos, em animais. Eritemas17 e exantema18 urticariforme foram observados com menor frequência, após administração de DACARB® (dacarbazina).
Os efeitos adversos da dacarbazina são apresentados em ordem de gravidade decrescente na tabela abaixo:
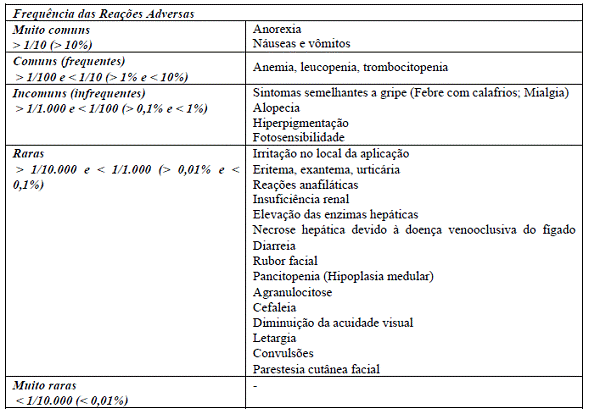
Em casos de eventos adversos, notifique ao sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
10. SUPERDOSE:
A superdose de dacarbazina caracteriza-se por sintomas2 semelhantes aos eventos adversos causados por este medicamento, porém de intensidade mais grave: reações alérgicas, depressão da medula óssea19, náuseas20 e vômitos6, diarreia7, anorexia3, alopecia12, rubor facial, parestesias21 cutâneas22. O tratamento da superdose deve ser feito com terapia de suporte e monitorização da contagem das células sanguíneas23. O tempo para ocorrência das contagens mais baixas de leucócitos24 e plaquetas25 é de 4 (quatro) semanas.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
M.S.: 1.0043.0636
Responsável Técnico: Dra. Sônia Albano Badaró – CRF-SP 19.258
EUROFARMA LABORATÓRIOS LTDA
Av. Vereador José Diniz, 3.465 - São Paulo - SP
CNPJ: 61.190.096/0001-92
Indústria Brasileira
LOGO CENTRAL DE ATENDIMENTO EUROFARMA COM TEL 0800 704 3876.
USO RESTRITO A HOSPITAIS.
VENDA SOB PRESCRIÇÃO MÉDICA.
Esta bula foi aprovada pela ANVISA em 28/06/2010.
Referências Bibliográficas:
1. Serrone L, Zeuli M, Sega FM, Cognetti F. Dacarbazine-based chemotherapy for metastatic melanoma26: thirty-year experience overview. J Exp Clin Cancer27 Res 19:21-34, 2000
2. Middleton MR, Grob JJ, Aaronson N, Fierlbeck G, Tilgen W, Seiter S, Gore M, Aamdal S, Cebon J, Coates A, Dreno B, Henz M, Schadendorf D, Kapp A, Weiss J, Fraass U, Statkevich P, Muller M, Thatcher N. Randomized Phase III Study of Temozolomide Versus Dacarbazine in the Treatment of Patients With Advanced Metastatic Malignant Melanoma26. J Clin Oncol 18:158-66, 2000
3. Legha SS, Ring S, Eton O, Bedikian A, Buzaid AC, Plager C, Papadopoulos N. Development of a Biochemotherapy Regimen With Concurrent Administration of Cisplatin, Vinblastine, Dacarbazine, Interferon Alfa, and Interleukin-2 for Patients With Metastatic Melanoma26. J Clin Oncol 16:1752-9, 1998
4. Eton O, Legha SS, Bedikian AY, Lee JJ, Buzaid AC, Hodges C, Ring SE, Papadopoulos NE, Plager C, East MJ, Zhan F, Benjamin RS. Sequential Biochemotherapy Versus Chemotherapy for Metastatic Melanoma26: Results From a Phase III Randomized Trial. J Clin Oncol 20:2045-52, 2002
5. Atkins MB, Hsu J, Lee S, Cohen GI, Flaherty LE, Sosman JA, Sondak VK,Kirkwood JM. Phase III Trial Comparing Concurrent Biochemotherapy With Cisplatin, Vinblastine, Dacarbazine, Interleukin-2, and Interferon Alfa-2b With Cisplatin, Vinblastine, and Dacarbazine Alone in Patients With Metastatic Malignant Melanoma26 (E3695): A Trial Coordinated by the Eastern Cooperative Oncology Group. J Clin Oncol 26:5748-54, 2008
6. Duggan DB, Petroni GR, Johnson JL, Glick JH, Fisher RI, Connors JM, Canellos GP, Peterson BA Randomized Comparison of ABVD and MOPP/ABV Hybrid for the Treatment of Advanced Hodgkin’s Disease: Report of an Intergroup Trial. J Clin Oncol 21:607-14, 2003
7. Straus DJ, Portlock CS, Qin J, Myers J, Zelenetz AD, Moskowitz C, Noy A, Goy A, Yahalom J. Results of a Prospective Randomized Clinical Trial of Doxorubicin, Bleomycin, Vinblastine, and Dacarbazine (ABVD) Followed by Radiation Therapy (RT) versus ABVD Alone for Stages I, II, and IIIA Nonbulky Hodgkin Disease. Blood 104:3483-9, 2004
8. Bonadonna G, Bonfante V, Viviani S, Russo AD, Villani F, Valagussa P. ABVD Plus Subtotal Nodal Versus Involved-Field Radiotherapy in Early-Stage Hodgkin’s Disease: Long-Term Results. J Clin Oncol 22:2835-41, 2004
9. Engert A, Franklin J, Eich HT, Brillant C, Sehlen S, Cartoni C, Herrmann R, Pfreundschuh M, Sieber M, Tesch H, Franke A, Koch P, de Wit M, Paulus U, Hasenclever D, Loeffler M, Muller R-P, Muller-Hermelink HK, Duhmke E, Diehl V. Two Cycles of Doxorubicin, Bleomycin, Vinblastine, and Dacarbazine Plus Extended-Field Radiotherapy Is Superior to Radiotherapy Alone in Early Favorable Hodgkin’s Lymphoma: Final Results of the GHSG HD7 Trial. J Clin Oncol 25:3495-3502, 2007
10. Weiner MA, Leventhal B, Brecher ML, et al. Randomized study of intensive MOPP-ABVD with or without low-dose total-nodal radiation therapy in the treatment of stages IIB, IIIA2, IIIB, and IV Hodgkin's disease in pediatric patients: a Pediatric Oncology Group study. J Clin Oncol. 1997;15(8):2769-79.
11. Oliveira BM, Viana MB, Cunha KCCMS. Linfoma28 de Hodgkin na infância: experiência de 16 anos em uma única instituição. J. Pediatr. 2000;76(4):281- 286
12. Kelly KM, Hutchinson RJ, Sposto R, et al. Feasibility of upfront doseintensive chemotherapy in children with advanced-stage Hodgkin's lymphoma: preliminary results from the Children's Cancer27 Group Study CCG-59704. Ann Oncol. 2002;13 Suppl 1:107-11.
13. Viani GA, Castilho MS, Novaes PE et al. Chemotherapy followed by low dose radiotherapy in childhood Hodgkin's disease: retrospective analysis of results and prognostic factors. Radiation Oncology 2006, 1:38
14. Morais A, Barros MHM, Rocio H et al. Número de áreas anatômicas envolvidas como preditor de risco no linfoma28 de Hodgkin em crianças: um estudo retrospectivo29. J Pediatr. 2009;85(3):236-242
15. Texto do Capítulo 23 (Linfoma28 de Hodgkin) – Hudson MM, Onciu M e Donaldson SD. Hodgkin Disease do livro Pizzo PA, Poplack DG, (edis.). Principles and practice of pediatric oncology. Philadelphia: Lippincott-Raven Publishers; 2010 acesso on line
16. Texto do Capítulo 10 (General Principles of Chemotherapy) – Adamson PC, Balis FM, Berg S, Blaney SM – do livro Pizzo PA, Poplack DG, (edis.). Principles and practice of pediatric oncology. Philadelphia: Lippincott-Raven Publishers; 2010 acesso on line


