
CARACTERISTICAS FARMACOLÓGICAS CIMAHER
Descrição
CIMAher (nimotuzumabe) é um anticorpo1 monoclonal (MAb) humanizado recombinante que reconhece com alta afinidade o Receptor do Fator de Crescimento Epidérmico (EGFR) humano. É obtido pela inserção das regiões hiper-variáveis ou determinantes complementares do anticorpo1 murino ior egf/r3 em marcadores de imunoglobulina2 humana, apresentando adicionalmente, as regiões constantes das cadeias leves (REI) e pesadas (Eu) de origem humana. Pertence as classe lgG 1, e tem um peso molecular aproximado de 150 Kd. CIMAher (nimotuzumabe) é produzido através do cultivo de células3 superiores não secretoras de mamíferos oriundas de um sistema de células3 hospedeiras de mieloma4 de camundongo bem caracterizado (NOS).
Farmacodinâmica
Mecanismo de Ação: O Receptor do Fator de Crescimento Epidérmico (EGFR) é uma glicoproeina de membrana de 170 Kd. Sua atividade intracelular está associada à atividade da proteína tirosina5-quinase específica e sua superexpressão pelas células3 tumorais altera a regulação do ciclo celular (aumentando sua proliferação), bloqueia a apoptose6. promove a angiogenêse, aumenta a motilidade, a adesividade e a capacidade invasiva.
ClMAher (nimotuzumabe) liga-se ao EGFR. bloqueando a ligação de seu ligante natural, e irnibindo o crescimento das células3 tumorais de origem epitelial in vitro e in vivo. Dessa forma, ClMAhera (nimo!uzumabe) possui efeito anti-angiogênico. anti-proliferativo e pró-apoptótico em tumores cque superexpressam o EGFR
Dados pré-clínicos
Citotoxicidade: Estudos avaliaram a citotoxicidade mediada por células3 anticorpo1-dependente – Antibody Dependent Cell Mediated Cytotoxictty (ADCC) - e de citotoxicidade complemento-dependentes - Complement Dependent Cytotoxicity (CDC). A capacidade de ADCC do ClMAher (nimotuzumabe) foi demonstrada numa prova de liberação de 51Cr. usando como alvo uma linhagem celular de adenocarcinoma7 de pulmão8 humano H-125. O ClMAher (nimotuzumabe) foi capaz de fixar, ativar e induzir a lise9 das células3 marcadas quando foi utilizada uma fonte de complemento humano.
Atividade antiproliferativa: ClMAher (nimotuzumabe) demonstrou ação antiproliferativa em linhagens tumorais e em células3 tumorais transplantadas em camundongos por bloqueio do EGFR. O ClMAher (nimotuzumabe) mostrou-se especialmente ativo in vitro em culturas tridimensionais.
Atividade antiangiogênica: CIMAhe, (nimotuzumabe) demonstrou propriedades antiangiogênicas pela inibiçâo da produção dos fatores de crescimento pró-angiogénicos, como VEGF. Testes in vivo avaliando a atividade antitumoral do ClMAher (nimotuzumabe) revelaram uma diminuição significativa na vascularização das amostras tratadas.
Toxicologia aguda e toxicologia subaguda10 de doses repetidas em roedores: Foram realizados estudos utilizando o ClMAher (nimotuzumabe) em doses de até 20 vezes a dose humana máxima proposta. Não foi observado qualquer sinal11 de toxicidade12 em nenhum dos estudos de dose única ou de doses repetidas.
Toxicidade12 de doses repetidas (6 meses) em primatas: Foi feito um estudo em macacos verdes
(Cercopithecus aethiops). Foram administradas doses intravenosas de 1X e 1OX a dose humana ótima. De 200mg (2,86 mglkg), e solução fisiológica13 a 3 grupos de 6 animais, cada grupo contendo 3 animais de cada sexo. A administração da substância em estudo foi feita uma vez por semana durante 26 semanas. Não foi observado qualquer efeito toxicológico que pudesse ser interpretado como sinal11 de efeitos farmacológicos secundários indesejados.
Mutagenicidade/Carcinogenicidade: Não foram realizados estudos para avaliar o potencial carcinogênico e mutagênico de ClMAher (nimotuzumabe).
Toxicidade12 reprodutiva: Não foram realizados estudos específicos em animais para avaliar o efeito de ClMAher (nimotuzumabe) sobre a fertilidade.
Reatividade cruzada: ClMAher (nimotuzumabe) foi estudado em várias amostras de criocortes de uma série de tecidos humanos e mostrou ligar-se essencialmente ao tecido epitelial14, especialmente pele15. que é incluída como controle positivo. Não há reatividade cruzada com tecidos de órgáos vitais (coração16, vasos sanguíneos17, rim18, encéfalo19 e pulmão8) e a ligação ao tecido epitelial14 normal não foi considerado um problema potencial.
Ligação Seletiva: Estudos demonstraram diferentes níveis de reação imuno-histoquímica e distribuição do ClMAher (nimotuzumabe) em diferentes tipos de tumores, dependendo do nível de expressão do receptor.
Os tumores estudados incluíram gliomas, meningeomas, histiocitoma fibroso maligno, neurofibrossarcoma e tumores de mama20, cabeça21 e pescoço22 e ginecológicos. Tumores não epiteliais não demonstraram qualquer reatividade com este anticorpo1 monoclonal.
Biodistribuição: ClMAher (nimotuzumabe) foi avaliado para sua utilização diagnóstica. O produto foi marcado com 99mTc (roedores) ou 188Re (babuínos). Alguns testes foram feitos em ratos com xenoenxertos de células3 tumorais H-125 ou A431. O ClMAher (nimotuzumabe) é depurado rapidamente da circulação23, diminuindo a captação radioativa inespecífica em tecidos normais, como fígado24, pulmões25 e rins26. Nos camundongos com implantes, o ClMAher (nimotuzumabe) marcado mostrou relações tumor27/não tumor27 fortemente positivas nos parâmetros avaliados.
Farmacocinética — Estudos Clínicos
Eliminação: No estudo clínico de fase 1 aberto, de doses crescentes, em pacientes com tumores avançados derivados do tecido epitelial14 foram obtidos parâmetros farmacocinéticos de 10 pacientes. As curvas de desaparecimento plasmático de ClMAhera (nimotuzumabe) ajustaram-se melhor por equação exponencial com meia-vida de elininação (tl/2B) de 62,91 h, 82,60 h, 302,95 h e 304.51 h para a dose de 50, 100, 200 e 400 mg, respectivamente. A área sob a curva de tempo-concentração (AUC28) foi 45 458. 145 931, 573 612 e 635 275 ng/mL.min e a concentração de atividade máxina (Cmáx) foi 27 790, 36 612. 52 713, 57 117 ng/mL para a dose de 50,100, 200 e 400 mg, respectivamente. O volume aparente do compartimento central (Vc) foi 2321,96, 2823,67, 4279,71 e 7173,99 ml e o clearance total de eliminação (Cl) foi 1,08; 0,67; 0,34 e 0,76 (mL/hlg) para a dose de 50, 100, 200 e 400 mg, respectivamenle. Não foram encontradas diferenças estatisticamente significativas no clearance para os quatro níveis de dose (P = 0,095. teste de Kruskal-Wallis).
As principais vias de eliminação em humanos são rins26, bexiga29 e trato gastrintestinal. Em 24 horas a excreção urinária média foi de cerca de 22%.
Biodistribuição: Os dados revelaram uma meia-vida efetiva de 2,93 h para o coração16, 3,94 h para o fígado24. 3,20 h para o baço30 e 4,96 h para o resto do organismo. Imagens positivas de tumor27 foram vistas em 4 de 10 pacientes. Os parâmetros laboratoriais (ames e 24 horas após a injeção31) não mostraram alterações significativas, exceto para a glicose32. que se apresentou elevada em um paciente após 24 horas. O fígado24 demonstrou ser o órgão-alvo, com pico de captação 1 h após a injeção31. Fígado24, vesícula biliar33 e baço30 apresentaram os valores mais altos de absorção.
Saturação dos recer1ores de EGFR: Desde as fases iniciais dos estudos das doses diagnósticas e terapêuticas de CIMAher (nimotuzumabe). a droga revelou perfil de segurança muito favorável em doses de até 400 mg (5.71 mg.’kg). A biodistribuição nas doses diagnósticas e nas doses terapêuticas revela os mesmos órgãos-alvo e as mesmas características farmacocinéticas. A análise farmacocinética dos estudos terapêuticos iniciais indica que a saturação dos receptores é obtida com doses iniciais acima de 200 mg e mantida com doses de 200 mg de ClMAher (nimotuzumabe).
- 2. RESULTADOS DE EFICÁCIA
Um estudo prospectivo34, de braço único. multicêntrico, foi realizado na Alemanha para avaliar a eficácia de nimotuzumabe no tratamento de glioma de alto grau. resistente à quimioterapia35 em crianças e adolescentes na faixa etária de 3 a 20 anos. Todos os pacientes apresentaram progressão da doença durante a terapia primária ou recaída comprovada.
O estudo foi planejado em duas etapas: na primeira seriam incluídos 18 pacientes e uma análise interina seria realizada quando estes 18 pacientes completassem o estudo. Se não houvesse resposta entre os 18 pacientes o estudo seria interrompido por fracasso. Se 3 ou mais dos 18 pacientes respondessem o estudo seria interrompido por comprovação da eficácia. Se um ou 2 dos 18 pacientes respondessem o estudo continuaria até que 47 pacientes fossem incluídos.
Durante o período de indução de 6 semanas todos os pacientes foram tratados com 150 mg/m2 uma vez por semana. Pacientes sem progressão da doença receberam 4 infusóes adicionais de nimotuzurnabe 150 mg/m2 de superfície corporal, uma vez a cada 3 semanas (período de consolidação).
Seis pacientes apresentavam diagnóstico36 de glioblastoma multiforme, 6 pacientes glioma de ponte intrínseco e 7 pacientes astrocitoma anaplásico37. Cinco dos 19 pacientes responderam ao tratamento (26,3%). Portanto, o objetivo primário do estudo foi atingido na primeira etapa e o estudo foi interrompido.
A tabela seguinte mostra o número e a porcentagem de resposta global por tipo de melhor resposta, com um intervalo de confiança (CI) de 95% para as porcentagens, para todos os pacientes de estudo e para o subgrupo de glioma de ponte intrínseco. Pacientes cuja melhor resposta foi progressão da doença também estão no resumo.
Resumo da melhor resposta, global e por tipo de resposta:
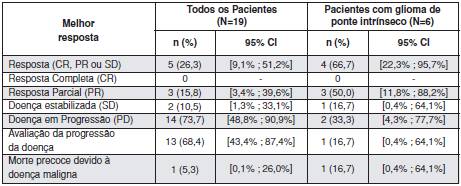
Quatro dos cincos pacientes respondedores apresentavam glioma intrínseco. Em 2 dos 3 pacientes com progressão da doença, esta foi confirmada pela segunda avaliação. Entre os respondedores, a duração média da resposta foi de 113.8 dias.
As figuras abaixo mostram a estimativa de Kaplan-Meier para a curva de sobrevida38 livre de progressão e para a curva de sobrevida38 global. O tempo médio de progressão foi de 46 dias (95% CI: [35 dias; 56dias]).
Curva de sobrevida38 livre da doença
Curva do tempo de sobrevida38 até a morte
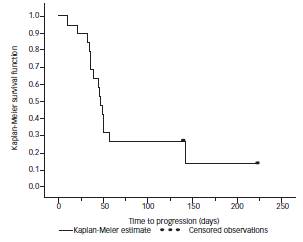
A gravidade média dos sintomas cardinais39 dos pacientes não alteraram relativamente entre a linha de base e o último valor do paciente durante o estudo na amostragem de análise completa. Entretanto, na média, uma melhora de 2,2 pontos foi observada em 5 pacientes que responderam ao tratamento, e uma piora de 0,6 pontos nos 14 pacientes que não responderam ao tratamento.
Os resultados de eficácia foram geralmente melhores no subgrupo de pacientes com glioma de ponte intrínseco porque a porcentagem de respondedores foi muito maior neste grupo.
A proporção observada de pacientes que responderam (26,3%, Cl 95%: [9,1%; 51,2%]) foi estatisticamente e significativamente maior que o esperado que era de 15%. Três dos 5 pacientes que responderam apresentaram resposta parcial e 2 pacientes estabilização da doença como melhor resposta. Os pacientes com Glioma de ponte intrínseco foram os que mais se beneficiaram do tratamento com nimotuzumabe. O tempo médio para a progressão foi de 46 dias (95% Cl: [35 dias; 56 dias]) e o tempo médio para a morte foi de 116 dias (95% Cl: [73 dias: 284 dias]).
ClMAher (nimotuzumabe) obteve 37,8% de resposta objetiva antitumoral no grupo de pacientes pediátricos tratados. A mediana de sobrevida38 foi de 8,9 meses para os pacientes que evidenciaram resposta antitumoral em comparação com 3,3 meses para os pacientes que não responderam ao tratamento (p < 0,05).
- 3.INDICAÇÕES:
ClMAher (nimotuzumabe) como monoterapia está indicado para pacientes40 pediátricos portadores de astrocitomas de alto grau recorrentes e/ou, refratários41 ao tratamento de cirurgia, à irradiação e à terapia com citostáticos42.


