
REAÇÕES ADVERSAS MENOS COMUNS ABILIFY
A Tabela 2 enumera a incidência1 combinada, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até seis semanas em esquizofrenia2 e até três semanas em mania bipolar), incluindo apenas aquelas reações que ocorreram em pelo menos 2% dos pacientes tratados com aripiprazol (doses ≥ 2 mg/dia) e cuja incidência1 em pacientes tratados com aripiprazol foi superior à incidência1 em pacientes tratados com placebo3 no conjunto de dados combinado.
Tabela 2: Reações adversas em estudos de curto prazo e controlados por placebo3 em pacientes tratados com ABILIFY

Um exame dos subgrupos de população não revelou nenhuma evidência clara de incidência1 diferencial de reação adversa com relação à idade, sexo ou raça.
Terapia adjuntiva com mania bipolar
Os achados abaixo são baseados em um estudo controlado por placebo3 em pacientes adultos com transtorno bipolar nos quais o aripiprazol foi administrado a doses de 15 mg/dia ou 30 mg/dia como terapia adjuntiva ao lítio ou valproato.
- Reações adversas associadas à descontinuação do tratamento
Em um estudo com pacientes que já toleravam lítio ou valproato como monoterapia, as taxas de descontinuação devida a reações adversas foram de 12% para pacientes4 tratados com aripiprazol em terapia adjuntiva, em comparação a 6% dos pacientes tratados com placebo3 em terapia adjuntiva.
As reações medicamentosas adversas mais comuns associadas à descontinuação em pacientes tratados com aripiprazolem terapia adjuntiva, em comparação a pacientes tratados com placeboem terapia adjuntiva, foram acatisia5 (5% e 1%, respectivamente) e tremores (2% e 1%, respectivamente).
- Reações adversas comumente observadas
As reações adversas mais frequentemente observadas associadas ao aripiprazol em terapia adjuntiva e lítio ou valproato em pacientes com mania bipolar (incidência1 de, no mínimo, 5% e incidência1 de pelo menos o dobro no placebo3 em terapia adjuntiva) foram: acatisia5, insônia e distúrbio extrapiramidal.
- Reações adversas menos comuns em pacientes sob terapia adjuntiva em mania bipolar
A Tabela 3 enumera a incidência1, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até seis semanas), incluindo apenas aquelas reações que ocorreram em, no mínimo, 2% dos pacientes tratados com aripiprazol em terapia adjuntiva (doses de 15 mg/dia ou 30 mg/dia) e lítio ou valproato, e cuja incidência1 em pacientes tratados com essa combinação foi superior à incidência1 nos pacientes tratados com placebo3 mais lítio ou valproato.
Tabela 3: Eventos adversos em estudo de curto prazo e controlado por placebo3 sobre a terapia adjuntiva em pacientes com transtorno bipolar


Reações adversas relacionadas à dose
- Esquizofrenia2
As relações de resposta à dose para a incidência1 de eventos adversos emergentes do tratamento foram avaliadas a partir de quatro estudos em pacientes adultos com esquizofrenia2 comparando doses fixas variadas (2 mg/dia, 5 mg/dia, 10 mg/dia, 15 mg/dia, 20 mg/dia e 30 mg/dia) de aripiprazol ao placebo3. Essa análise, estratificada por estudo, indicou que a única reação adversa possivelmente relacionada à dose, e mais notável apenas com 30 mg, foi sonolência [incluindo sedação6]; (incidências para o placebo3: 7,1%; 10 mg, 8,5%; 15 mg, 8,7%; 20 mg, 7,5%; 30 mg, 12,6%).
- Sintomas7 Extrapiramidais
Esquizofrenia2
Em estudos de curto prazo e controlados por placebo3 em esquizofrenia2 em adultos, a incidência1 de eventos relacionados à síndrome8 extrapiramidal relatados, exceto por eventos relacionados à acatisia5, para pacientes4 tratados com aripiprazol, foi de 13% versus 12% para placebo3. A incidência1 de eventos relacionados à acatisia5 para pacientes4 tratados com aripiprazol foi de 8% versus 4% para placebo3.
Dados coletados objetivamente a partir desses estudos foram reunidos na Escala de Classificação de Simpson Angus (para síndrome8 extrapiramidal), Escala de Acatisia5 de Barnes (para acatisia5) e nas Avaliações das Escalas de Movimento Involuntário (para discinesia). Em estudos de esquizofrenia2 em adultos, os dados coletados objetivamente não apresentaram uma diferença entre aripiprazol e placebo3, exceto pela Escala de Acatisia5 de Barnes (aripiprazol, 0,08; placebo3, -0,05).
De maneira semelhante, em um estudo de longo prazo (26 semanas), controlado por placebo3, de esquizofrenia2 em adultos, os dados coletados objetivamente na Escala de Classificação de Simpson Angus (para síndrome8 extrapiramidal), Escala de Acatisia5 de Barnes (para agitação motora) e nas Avaliações das Escalas de Movimento Involuntário (para discinesia) não apresentaram diferença entre aripiprazol e placebo3.
Mania Bipolar
Em estudos de curto prazo e controlados por placebo3 em mania bipolar em adultos, a incidência1 de eventos relacionados à síndrome8 extrapiramidal relatados, exceto por eventos relacionados à acatisia5, para pacientes4 tratados com aripiprazol em monoterapia, foi de 16% versus 8% para placebo3. A incidência1 de eventos relacionados à acatisia5 para pacientes4 tratados com aripiprazol em monoterapia foi de 13% versus 4% para placebo3. Em um estudo de seis semanas, controlado por placebo3, em mania bipolar para terapia adjuntiva com lítio ou valproato, a incidência1 de eventos relacionados à síndrome8 extrapiramidal relatados, exceto por eventos relacionados à acatisia5, para pacientes4 tratados com aripiprazol em terapia adjuntiva, foi de 15% versus 8% para placebo3 em terapia adjuntiva. A incidência1 de eventos relacionados à acatisia5 para pacientes4 tratados com aripiprazol em terapia adjuntiva foi de 19% versus 5% para placebo3 em terapia adjuntiva.
Nos estudos de monoterapia de aripiprazol em adultos com mania bipolar, a Escala de Classificação de Simpson Angus e a Escala de Acatisia5 de Barnes demonstraram uma diferença significativa entre aripiprazol e placebo3 (aripiprazol, 0,50; placebo3, -0,01 e aripiprazol, 0,21; placebo3, -0,05). As alterações nas Avaliações das Escalas de Movimento Involuntário foram semelhantes para os grupos de aripiprazol e placebo3. Em estudos de mania bipolar com aripiprazol como terapia adjuntiva com lítio ou valproato, a Escala de Classificação de Simpson Angus e a Escala de Acatisia5 de Barnes demonstraram uma diferença significativa entre aripiprazol e placebo3 em terapia adjuntiva (aripiprazol, 0,73; placebo3, 0,07 e aripiprazol, 0,30; placebo3, 0,11). As alterações nas Avaliações das Escalas de Movimento Involuntário foram semelhantes para os grupos de aripiprazol e placebo3 em terapia adjuntiva.
- Distonia9
Sintomas7 de distonia9, contrações anormais prolongadas de conjuntos de músculos10, podem ocorrer em indivíduos susceptíveis durante os primeiros dias de tratamento. Os sintomas7 da distonia9 incluem: espasmos11 nos músculos do pescoço12, algumas vezes progredindo para compressão da garganta13, dificuldade em engolir, dificuldade em respirar e/ou protrusão da língua14. Embora estes sintomas7 possam ocorrer em doses baixas, eles ocorrem mais frequentemente e com maior gravidade sob concentrações maiores e doses mais altas de drogas antipsicóticas de primeira geração. Um risco elevado de distonia9 aguda é observado em grupos de homens e indivíduos mais jovens.
- Ganho de Peso
Em estudos de quatro a seis semanas em adultos com esquizofrenia2, houve uma leve diferença no ganho de peso médio entre pacientes recebendo aripiprazol e placebo3 (+0,7 kg versus -0,05 kg, respectivamente) e também foi observada diferença na proporção de pacientes que atendiam ao critério de ganho de peso ≥7% do peso corporal [aripiprazol (8%) comparado a placebo3 (3%)]. Em estudos de três semanas de monoterapia de aripiprazol em adultos com mania, o ganho de peso médio para pacientes4 recebendo aripiprazol e placebo3 foi de 0,1 kg versus 0,0 kg, respectivamente.
A proporção de pacientes que atenderam ao critério de ganho de peso ≥ 7% do peso corporal foi de 2% com aripiprazol em comparação a 3% com placebo3. No estudo de seis semanas em Mania com aripiprazol como terapia adjuntiva com lítio ou valproato, o ganho de peso médio para os pacientes recebendo aripiprazol e placebo3 foi de 0,6 kg versus 0,2 kg, respectivamente. A proporção de pacientes que atenderam ao critério de ganho de peso ≥ 7% do peso corporal foi de 3% com aripiprazol em comparação a 4% com placebo3 em terapia adjuntiva.
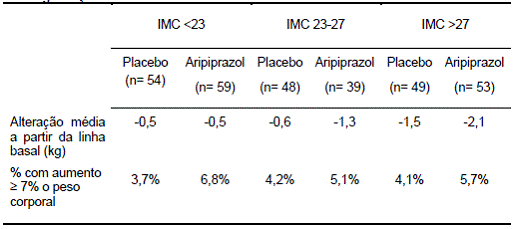
A Tabela 6 fornece os resultados na alteração de peso de um estudo de longo prazo (26 semanas), controlado por placebo3, de aripiprazol em adultos com esquizofrenia2, a alteração média a partir da linha basal e as proporções de pacientes que atenderam ao critério de ganho de peso ≥ 7% o peso corporal relativo à linha basal, categorizado pelo índice de massa corporal15 (IMC16) na linha basal. Apesar de não haver aumento no peso médio, o grupo de aripiprazol tendeu a apresentar mais pacientes com um ganho de peso ≥ 7%.
Tabela 6: Resultados na alteração de peso categorizados pelo índice de massa corporal15 na linha basal: estudo controlado por placebo3 em esquizofrenia2, amostra de segurança
A Tabela 7 fornece os resultados na alteração de peso de um estudo de longo prazo (52 semanas) de aripiprazol em adultos com esquizofrenia2, a alteração média a partir da linha basal e as proporções de pacientes que atenderam ao critério de ganho de peso ≥ 7% o peso corporal relativo à linha basal, categorizado pelo índice de massa corporal15 (IMC16) na linha basal:
Tabela 7: Resultados na alteração de peso categorizados pelo índice de massa corporal15 na linha basal: estudo controlado ativamente em esquizofrenia2, amostra de segurança

Achados adicionais observados em estudos clínicos
- Reações adversas em estudo de longo prazo, duplo-cegos e controlados por placebo3
As reações adversas relatadas em um estudo duplo-cego17 de 26 semanas, comparando ABILIFY e placebo3 em pacientes com esquizofrenia2, foram em geral consistentes com aquelas relatadas em estudos de curto prazo e controlados por placebo3, exceto por uma incidência1 maior de tremores [8% (12/153) para ABILIFY versus 2% (3/153) para placebo3]. Neste estudo, a maioria dos casos de tremores teve intensidade leve (8/12 leve e 4/12 moderada), ocorreu no início da terapia (9/12 ≤ 49 dias) e apresentou duração limitada (7/12 ≤ 10 dias). Em casos raros, os tremores levaram à descontinuação (<1%) de ABILIFY. Ademais, em um estudo de longo prazo (52 semanas), controlado por medicamento ativo, a incidência1 de tremores foi de 5% (40/859) para ABILIFY. Um perfil semelhante foi observado em um estudo de longo prazo com transtorno bipolar.
- Outras reações adversas observadas durante a avaliação pré-comercialização de aripiprazol
Abaixo pode ser encontrada uma relação dos termos do MedDRA que refletem as reações adversas como definidas em REAÇÕES ADVERSAS, relatadas por pacientes tratados com aripiprazol oral em doses múltiplas ≥ 2 mg/dia durante qualquer fase de um estudo no banco de dados de 13.543 pacientes adultos. Todos os eventos avaliados como possíveis reações adversas foram incluídos, exceto pelos eventos mais frequentes. Além disso, reações adversas médica ou clinicamente significativas, em especial aquelas provavelmente mais úteis para o médico responsável pela prescrição, ou que apresentam plausibilidade farmacológica, também foram incluídas. Eventos já listados em outras partes de REAÇÕES ADVERSAS, ou aqueles mencionados em ADVERTÊNCIAS E PRECAUÇÕES ou SUPERDOSE foram excluídos. Apesar de as reações relatadas terem ocorrido durante o tratamento com aripiprazol, elas não foram necessariamente causadas pelo medicamento.
Os eventos são, ainda, categorizados pela classe de sistemas de órgãos e listados em frequência decrescente de acordo com as definições abaixo:
Comum (frequente): ocorreram em ≥ 1/100 e < 1/10 dos pacientes (apenas aqueles ainda não listados nos resultados tabelados de estudos controlados por placebo3 aparecem nessa relação);
Incomum (infrequente): ocorreram em ≥ 1/1000 e < 1/100 dos pacientes;
Raro: ocorreram em ≥ 1/10000 e < 1/1000 dos pacientes.
Distúrbios do sistema linfático18 e sanguíneo: Incomuns – leucopenia19, neutropenia20, trombocitopenia21.
Distúrbios cardíacos: Incomuns – bradicardia22, palpitações23, insuficiência24 cardiopulmonar, infarto do miocárdio25, parada cardiorrespiratória, bloqueio atrioventricular, extrassístoles, taquicardia26 sinusal, fibrilação atrial, angina27 pectoris, isquemia28 miocárdica; Raros – flutter atrial, taquicardia26 supraventricular, taquicardia26 ventricular.
Distúrbios oculares: Incomuns – fotofobia29, diplopia30, edema31 na pálpebra, fotopsia.
Distúrbios gastrintestinais: Incomuns – diarreia32, doença do refluxo gastroesofágico33, edema31 de língua14, esofagite34; Raro – pancreatite35.
Distúrbios gerais e condições no local de administração: Comuns – astenia36, edema31 periférico, dor no peito37, pirexia38, irritabilidade; Incomuns – edema31 facial, angioedema39, sede; Raro – hipotermia40.
Distúrbios hepatobiliares41: Raros– hepatite42, icterícia43.
Distúrbios do sistema imunológico44: Incomum – hipersensibilidade.
Lesões45, intoxicação e complicações do procedimento: Comum – queda; Incomum – automutilação; Raro – insolação.
Investigações: Comuns - redução do peso, creatinofosfoquinase elevada; Incomuns – enzima46 hepática47 elevada, glicose48 sérica elevada, prolactina49 sérica elevada, ureia50 sérica elevada, prolongamento do QT no eletrocardiograma51, creatinina52 sérica elevada, bilirrubina53 sérica elevada; Raros – lactato54 desidrogenase sérico elevada, hemoglobina glicosilada55 elevada, gama glutamil transferase elevada.
Distúrbios metabólicos e nutricionais: Comum – apetite reduzido; Incomuns – hiperlipidemia56, anorexia57, diabetes mellitus58 (incluindo insulina59 sérica elevada, tolerância a carboidratos reduzida, diabetes mellitus58 não dependente de insulina59, tolerância à glicose48 prejudicada, glicosúria60, glicose48 na urina61, glicose48 presente na urina61), hiperglicemia62, hipocalemia63, hiponatremia64, hipoglicemia65, polidipsia66; Raro – cetoacidose diabética67.
Distúrbio musculoesquelético e do tecido conjuntivo68: Incomuns – rigidez muscular, fraqueza muscular, compressão muscular, mobilidade reduzida; Raro – rabdomiólise69.
Distúrbios do sistema nervoso70: Comuns – coordenação anormal, discinesia; Incomuns – distúrbio na fala, parkinsonismo, comprometimento da memória, rigidez de roda dentada, acidente vascular cerebral71, hipocinesia, discinesia tardia72, hipotonia73, mioclonia74, hipertonia75, acinesia, bradicinesia76; Raros – convulsão77 de grande mal, coreoatetose.
Transtornos psiquiátricos: comum – ideação suicida; Incomuns – agressividade, perda da libido78, tentativa de suicídio, hostilidade, libido78 elevada, raiva79, anorgasmia80, delírios, automutilação intencional, suicídio concluído, tique81, ideação homicida; Raros – catatonia, sonambulismo
Distúrbios renais e urinários: Incomuns – retenção urinária82, poliúria83, noctúria.
Distúrbios do sistema reprodutor e das mamas84: Incomuns – menstruação85 irregular, disfunção erétil, amenorreia86, dor nas mamas84; Raros – ginecomastia87, priapismo88.
Distúrbios respiratórios, torácicos e mediastinais: Comuns – congestão nasal, dispneia89, pneumonia90 por aspiração.
Distúrbios cutâneos e subcutâneos: Comuns – rash91 (incluindo rash91 eritematoso92, esfoliativo, generalizado, macular, maculopapular93, papular; dermatite94 acneiforme, alérgica, de contato, esfoliativa, seborréica, neurodermatite e erupção95 medicamentosa), hiperidrose96; Incomuns – prurido97, reação fotossensível, alopecia98, urticária99.
Distúrbios vasculares100: Comum – hipertensão101; Incomum – hipotensão102.
Experiência pós-comercialização
As reações adversas abaixo foram identificadas durante o uso após a aprovação de ABILIFY. Em razão de essas reações serem relatadas voluntariamente por uma população de tamanho indeterminado, nem sempre é possível estabelecer uma relação causal com a exposição à droga: ocorrências raras de reação alérgica103 (reação anafilática104, angioedema39, laringoespasmo, prurido97/urticária99 ou espasmo105 orofaríngeo106) e oscilação da glicose48 sérica.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.


