
POSOLOGIA E ADMINISTRAÇÃO CLORIDRATO DE CEFEPIMA
Administração
cloridrato de cefepima pode ser administrado por via intravenosa ou intramuscular. A dose e a via de administração variam de acordo com a sensibilidade do patógeno, com a gravidade da infecção1, com a função renal2 e com a condição geral do paciente.
Posologia
Adultos
Um guia para as doses de cloridrato de cefepima em adultos com função renal2 normal é apresentado na Tabela 4.
TABELA 4 - Esquema de Dose Recomendado em Adultos com Função Renal2 Normal (acima de 12 anos de idade)*
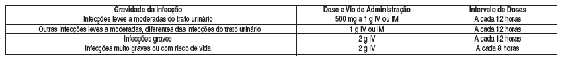
*A duração normal do tratamento é de 7 A 10 dias; entretanto, infecções3 mais graves podem necessitar de tratamento mais prolongado. Para o tratamento empírico de neutropenia4 febril, a duração prevista é de 7 dias ou até a resolução da neutropenia4.
Lactentes5 e crianças (1 mês a 12 anos de idade com função renal2 normal)
Doses comumente recomendadas.
Pneumonia6, infecções3 do trato urinário7, infecções3 da pele8 e estruturas cutâneas9
Pacientes com mais de 2 meses de idade e peso corpóreo < 40kg: 50 mg/kg a cada 12 horas durante 10 dias. Para infecções3 mais graves o intervalo entre as doses a cada 8 horas pode ser usado.
Septicemia10, meningite11 bacteriana e tratamento empírico da neutropenia4 febril
Pacientes com mais de 2 meses de idade e peso corpóreo < 40kg: 50 mg/kg a cada 8 horas durante 7 - 10 dias.
A experiência com o uso de cloridrato de cefepima em pacientes pediátricos com menos de 2 meses de idade é limitada. Embora esta experiência tenha sido alcançada usando-se a dose de 50 mg/kg, os dados farmacocinéticos obtidos em pacientes com mais de 2 meses de idade sugerem que a dose de 30 mg/kg a cada 8 horas ou a cada 12 horas podem ser consideradas para pacientes12 entre 1 e 2 meses de idade. A administração de cloridrato de cefepima nestes pacientes deverá ser cuidadosamente controlada.
Para pacientes12 pediátricos com peso corpóreo acima de 40 kg, aplicam-se as doses recomendadas para adultos (vide “TABELA 4”). Em pacientes com mais de 12 anos e peso corpóreo que não ultrapasse 40kg a dose recomendada deverá ser a utilizada para pacientes12 com ≥ 40kg. A dose recomendada para pacientes12 pediátricos não deve exceder a dose máxima recomendada para adultos (2 g a cada 8 horas). A experiência com a administração intramuscular em pacientes pediátricos é limitada.
Pacientes portadores de disfunção renal2
A dose inicial de cloridrato de cefepima é a mesma dos pacientes com função renal2 normal. As doses de manutenção recomendadas de cloridrato de cefepima para pacientes12 com insuficiência renal13 são apresentadas na TABELA 5.
TABELA 5 - Esquema de doses de manutenção recomendadas em pacientes adultos com disfunção renal2 em relação à dose normal *
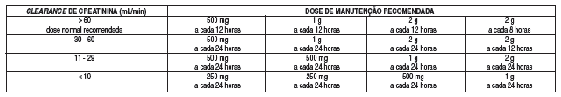
*A dose inicial é a mesma dos pacientes com função renal2 normal.
Quando somente o valor da creatinina14 sérica estiver disponível, pode-se usar a fórmula abaixo (equação de Cockcroft e Gault) para estimar o “clearance” da creatinina14. A
creatinina14 sérica deve representar um estado de equilíbrio hemodinâmico da função renal2.
Homens
“Clearance” da creatinina14 (mL/min) = peso (kg) X (140 - idade) .
72 X creatinina14 sérica (mg/dL15)
Mulheres
0,85 X valor calculado usando-se a fórmula para homens.
Pacientes submetidos à diálise16
Em pacientes submetidos à hemodiálise17, aproximadamente 68% da quantidade total de cefepima presente no organismo no início da diálise16 será removida durante um período de 3 horas de diálise16. Uma dose repetida equivalente à dose inicial deve ser administrada ao completar cada sessão de diálise16. Em pacientes submetidos à diálise peritoneal18 contínua em ambulatório, a cefepima pode ser administrada nas mesmas doses recomendadas para pacientes12 com função renal2 normal, isto é, 500 mg, 1 g ou 2 g dependendo da gravidade da infecção1, porém com intervalo entre as doses de 48 horas.
Crianças portadoras de disfunção renal2
Uma vez que a excreção urinária é a principal via de eliminação da cefepima em pacientes pediátricos (vide "Farmacologia "), o ajuste das doses de cloridrato de cefepima deve ser considerado em pacientes com menos de 12 anos de idade portadores de disfunção renal2.
A dose de 50 mg/kg em pacientes com idade entre 2 meses a 12 anos e a dose de 30 mg/kg em pacientes com 1 mês a 2 meses de idade são comparáveis à dose de 2 g em adultos. Como recomendado anteriormente na Tabela 5, os mesmos aumentos nos intervalos das doses e/ou reduções de doses devem ser usados.
Quando somente o valor da creatinina14 sérica estiver disponível, o “clearance” de creatinina14 pode ser estimado utilizando-se os seguintes métodos:
Clearance da creatinina14 (mL/min/1,73m2) = 0,55 X altura (centímetros)
creatinina14 sérica (mg/dL15)
ou Clearance da creatinina14 (mL/min/1,73m2) = 0,52 X altura (centímetros) – 3,6
creatinina14 sérica (mg/dL15)
Pacientes portadores de disfunção hepática19
Não é necessário nenhum ajuste para pacientes12 com alterações da função hepática19.
TABELA 6 - Preparo das soluções de cloridrato de cefepima
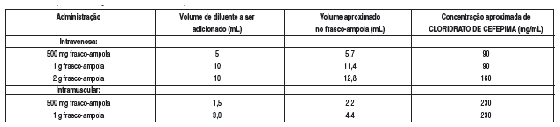
Reconstituição
Os medicamentos de uso parenteral devem ser visualmente inspecionados antes da administração com relação a partículas estranhas e não devem ser utilizados se estes estiverem presentes.
cloridrato de cefepima deve ser reconstituído utilizando-se os volumes de diluentes descritos na Tabela 6; os diluentes a serem utilizados são identificados na TABELA 7.
Administração intravenosa (IV)
É a via de administração preferível para pacientes12 com infecções3 graves ou com risco de vida, principalmente se existe a possibilidade de choque20.
Para a administração intravenosa direta, reconstituir cloridrato de cefepima com água para injeção21, solução injetável de glicose22 a 5% ou soro23 fisiológico24 a 0,9%, utilizando-se os volumes de diluente descritos na Tabela 6. A solução resultante deve ser injetada diretamente na veia em intervalos de três a cinco minutos ou injetada no tubo do equipo de administração enquanto o paciente estiver recebendo líquido intravenoso compatível (vide: “Compatibilidade e Estabilidade”).
Para infusão intravenosa, reconstituir a dose de 500 mg, 1 g ou 2 g, como descrito anteriormente para administração intravenosa direta e adicionar a quantidade apropriada da solução resultante para um recipiente com um dos líquidos intravenosos compatíveis (vide: “Compatibilidade e Estabilidade”). A solução resultante deve ser completamente administrada em um período de aproximadamente 30 minutos.
Administração intramuscular (IM)
Cloridrato de cefepima deve ser reconstituído com um dos seguintes diluentes (utilizando-se os volumes descritos na Tabela 6): água para injeção21, soro23 fisiológico24 a 0,9%, solução injetável de glicose22 a 5% ou água bacteriostática para injeção21 com parabenos ou álcool benzílico, então administrado por injeção intramuscular25 profunda em uma grande massa muscular (como o quadrante superior externo da região glútea26). Em um estudo farmacocinético, doses de 1 g (volume < 3,1 mL) foram administradas em injeção21 local única; a dose máxima intramuscular (2 g/6,2 mL) foi administrada em dois locais. Embora CLORIDRATO DE CEFEPIMA possa ser reconstituído com cloridrato de lidocaína a 0,5 ou 1,0%, esta normalmente não é necessária, pois cloridrato de cefepima causa pouca ou nenhuma dor na administração intramuscular.
Compatibilidade e Estabilidade
Como ocorre com outras cefalosporinas, a cor de cloridrato de cefepima pó e da solução reconstituída pode escurecer durante a armazenagem, porém a potência do produto não será afetada.
Intravenosa:
Cloridrato de cefepima é compatível em concentrações entre 1 e 40 mg/mL com os seguintes líquidos para infusão intravenosa: soro23 fisiológico24 a 0,9%, solução injetável de glicose22 a 5% ou 10%, injeção21 de lactato27 de sódio M/6, solução injetável de glicose22 a 5% e soro23 fisiológico24 a 0,9%, solução injetável de Ringer Lactato27 e solução injetável de glicose22 a 5%. Estas soluções são estáveis por 24 horas à temperatura ambiente (entre 15°C e 30°C) ou por 7 dias sob refrigeração (entre 2°C e 8°C).
Informações sobre a estabilidade e compatibilidade de cloridrato de cefepima em associações estão resumidas na Tabela 7.
TABELA 7 - Estabilidade de cloridrato de cefepima em associações
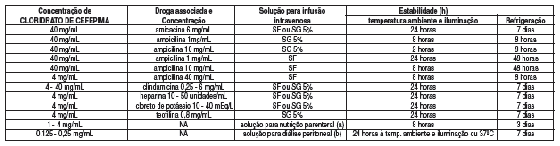
(a) = Aminosina II 4,25% em glicose22 25% com eletrólitos28 e cálcio.
(b) = Inpersol® com 4,25% de glicose22.
SF = Solução fisiológica29 a 0,9% para injeção21.
SG5% = Solução injetável de glicose22 a 5%.
NA = não aplicável.
As soluções de cloridrato de cefepima, assim como a maioria dos antibióticos betalactâmicos, não devem ser associadas com soluções de metronidazol, vancomicina, gentamicina, tobramicina ou netilmicina devido à incompatibilidade física e química. Entretanto, caso a terapia concomitante com cloridrato de cefepima for indicada, cada um desses antibióticos poderá ser administrado separadamente.
Intramuscular:
Cloridrato de cefepima reconstituído como descrito (Tabela 7) é estável por 24 horas à temperatura ambiente (entre 15°C e 30°C) ou por 7 dias sob refrigeração (2°C a 8°C) quando são usados os seguintes diluentes: água estéril para injeção21, soro23 fisilógico a 0,9%, solução injetável de glicose22 a 5%, água bacteriostática para injeção21 com parabenos ou álcool benzílico, ou cloridrato de lidocaína a 0,5 ou a 1,0%.
- SUPERDOSAGEM:
Em estudos clínicos ocorreu superdosagem com cloridrato de cefepima em um paciente com insuficiência renal13 (clearance de creatinina14 < 11 mL/min), o qual recebeu 2 g a cada 24 horas por 7 dias. O paciente apresentou convulsões, encefalopatia30 e excitabilidade neuromuscular. os pacientes que receberem superdose devem ser cuidadosamente observados e receber tratamento de suporte. Na presença de insuficiência renal13, a hemodiálise17 ajudará na remoção de cloridrato de cefepima do organismo; a diálise peritoneal18 não é indicada nestes casos. pode ocorrer superdose acidental quando doses elevadas são administradas a pacientes com função renal2 reduzida (vide “PRECAUÇÕES E ADVERTÊNCIAS”).


