
ADVERTÊNCIAS E PRECAUÇÕES DORMONID BULA PARA O PROFISSIONAL DE SAÚDE
Dormonid® injetável deve ser usado somente quando materiais de ressuscitação apropriados para o tamanho e a idade estão disponíveis, já que a administração I.V. de Dormonid® pode deprimir a contratilidade miocárdica e causar apneia1. Eventos adversos cardiorrespiratórios graves têm ocorrido em raras ocasiões. Esses eventos têm incluído depressão respiratória, apneia1, parada respiratória e/ou parada cardíaca.
A ocorrência de tais incidentes2 de risco de vida é mais provável em adultos acima de 60 anos, naqueles com insuficiência respiratória3 preexistente ou comprometimento da função cardíaca, e pacientes pediátricos com instabilidade cardiovascular, particularmente quando a injeção4 é administrada muito rapidamente ou quando é administrada uma alta dose.
Quando Dormonid® injetável é administrado parenteralmente, cuidados especiais devem ser observados em pacientes representantes de grupos de alto risco:
· adultos acima de 60 anos;
· pacientes cronicamente doentes ou debilitados;
· pacientes com insuficiência respiratória crônica5;
· pacientes com insuficiência renal6 crônica, insuficiência hepática7 ou com insuficiência cardíaca congestiva8;
· pacientes pediátricos com instabilidade cardiovascular.
Esses pacientes de alto risco precisam de doses menores (vide “Posologia”) e devem ser monitorados continuamente com relação a sinais9 precoces de alteração das funções vitais.
As informações devem ser dadas aos pacientes sobre as seguintes advertências e precauções.
Critérios de alta
Após a administração de Dormonid®, os pacientes devem receber alta hospitalar ou do consultório de procedimento, apenas quando autorizado pelo médico do paciente e se acompanhado por um atendente. Recomenda-se que o paciente esteja acompanhado ao retornar para casa após a alta.
Tolerância
Alguma perda de eficácia foi relatada quando Dormonid® injetável foi usado em sedação10 prolongada em unidades de terapia intensiva11. Pode ocorrer perda de eficácia do efeito hipnótico de benzodiazepínicos de curta duração de ação, após uso repetido por algumas semanas, com as formas orais.
Dependência
Quando Dormonid® injetável é usado em sedação10 prolongada em unidades de terapia intensiva11, deve-se ter em mente que pode se desenvolver dependência física a ele. O risco de dependência aumenta com a dose e a duração do tratamento e é também maior para pacientes12 com um histórico médico de abuso de álcool e/ou drogas.
Com relação a Dormonid® comprimidos, deve-se lembrar que o uso de benzodiazepínicos e agentes similares pode levar ao desenvolvimento de dependência física e psicológica a eles. O risco de dependência aumenta com a dose e a duração do tratamento; é maior também para pacientes12 com histórico médico de abuso de álcool ou drogas.
Sintomas13 de abstinência
Uma vez desenvolvida dependência, a interrupção abrupta do tratamento será acompanhada de sintomas13 de abstinência.
Esses sintomas13 podem consistir em cefaleia14, mialgia15, extrema ansiedade, tensão, inquietação, confusão mental e irritabilidade. Em casos graves, os seguintes sintomas13 podem ocorrer: desrealização, despersonalização, hiperacusia, amortecimento e parestesia16 de extremidades, hipersensibilidade à luz, ruído e contato físico, alucinações17 e convulsões.
Durante tratamento prolongado com Dormonid® injetável em unidade de terapia intensiva11, pode-se desenvolver dependência física. Portanto, o término abrupto do tratamento pode ser acompanhado por sintomas13 de abstinência. Os seguintes sintomas13 podem ocorrer: cefaleia14, dor muscular, ansiedade, tensão, agitação, confusão, irritabilidade, insônia rebote, mudanças de humor, alucinações17 e convulsões. Já que o risco de sintomas13 de abstinência é maior após a descontinuação abrupta do tratamento, é recomendado que a dose seja diminuída gradualmente.
Insônia rebote
Na administração de Dormonid® comprimidos, deve-se considerar que a insônia rebote, uma síndrome18 transitória em que sintomas13 que levaram ao tratamento com benzodiazepínico ou agentes similares reincidem de forma aumentada, pode ocorrer na interrupção do tratamento hipnótico. Pode ser acompanhada de outras reações, incluindo alterações de humor, ansiedade e inquietação. Como o risco de fenômenos de abstinência ou rebote é maior após descontinuação abrupta do tratamento, recomenda-se redução gradual da dose.
Duração do tratamento
A duração do tratamento com hipnóticos benzodiazepínicos deve ser a mais curta possível (vide “Posologia”) e não deve exceder duas semanas. Manutenção por tempo superior não deve ocorrer sem reavaliação da condição do paciente. O processo de redução gradual deve ser ajustado individualmente. Pode ser útil informar ao paciente, no início, que o tratamento terá duração limitada e explicar precisamente como a dose será progressivamente diminuída. Sobretudo, é importante que o paciente tenha conhecimento da possibilidade de sintomas13 rebote, o que poderá diminuir a ansiedade decorrente de tais sintomas13, caso eles se manifestem na descontinuação do medicamento. Há evidências de que, no caso de benzodiazepínicos de curta duração de ação, sintomas13 de abstinência podem ocorrer nos intervalos interdose, especialmente quando se utiliza dose elevada.
Amnésia19
Dormonid® injetável e Dormonid® comprimidos causam amnésia19 anterógrada (frequentemente esse efeito é muito desejável em situações tais como antes e durante procedimentos cirúrgicos e diagnósticos); sua duração é diretamente relacionada à dose administrada. Amnésia19 prolongada pode proporcionar problemas para pacientes12 ambulatoriais, que devem receber alta após a intervenção. Após receberem Dormonid® parenteralmente, os pacientes devem ser dispensados do hospital ou do consultório somente com acompanhante.
Dormonid® comprimidos também pode causar amnésia19 anterógrada, que ocorre mais frequentemente dentro das primeiras horas após a ingestão do produto. A condição ocorre mais frequentemente nas primeiras horas após a ingestão do produto e, portanto, para reduzir o risco, os pacientes devem se assegurar de que poderão ter um período ininterrupto de sono de sete a oito horas (vide também “Reações adversas”).
Reações paradoxais
Foram relatadas com Dormonid® injetável reações paradoxais, tais como agitação, movimentos involuntários (incluindo convulsões tônico-clônicas e tremores musculares), hiperatividade, hostilidade, reação de raiva20, agressividade, excitação e ataque. A mais alta incidência21 de susceptibilidade22 a tais reações foi relatada em crianças e em idosos. Se tais sintomas13 sugestivos de uma reação paradoxal23 ocorrerem, a resposta a Dormonid® deve ser avaliada antes do procedimento.
Na administração de Dormonid® comprimidos, deve-se considerar que podem ocorrer efeitos paradoxais e psiquiátricos, como inquietação, agitação, irritabilidade, agressividade e, mais raramente, delírios, acessos de raiva20, pesadelos, alucinações17, psicose24, comportamento inadequado e outros efeitos adversos relacionados ao comportamento quando se utilizam benzodiazepínicos ou agentes similares. Nesse caso, o uso do medicamento deve ser descontinuado.
A ocorrência desses efeitos é mais provável em pacientes idosos.
Alterações na eliminação de midazolam
A eliminação da droga pode estar alterada em pacientes que recebem substâncias que inibem ou induzem P4503A4 e pode ser necessário ajustar a dose de midazolam (vide “Interações medicamentosas”).
A eliminação da droga também pode demorar mais em pacientes com disfunção hepática25, baixo débito cardíaco26 e em neonatos27 (vide “Farmacocinética em Populações Especiais”).
Pacientes idosos: embora rara, a ocorrência de eventos adversos cardiorrespiratórios graves com risco de morte, incluindo depressão respiratória, apneia1, parada respiratória e/ou parada cardíaca, é mais provável em adultos acima de 60 anos e crianças. Além disso, em idosos e crianças, foi relatada com Dormonid® injetável e Dormonid® comprimidos incidência21 mais elevada de sensibilidade a reações paradoxais, tais como agitação, movimentos involuntários (incluindo convulsões tônico-clônicas e tremores musculares), hiperatividade, hostilidade, reação de raiva20, agressividade, excitação e agressão.
Portanto, em adultos acima de 60 anos, a dose deve ser determinada com cautela e devem ser considerados os fatores especiais relacionados a cada paciente (vide “Posologia”).
Pacientes pediátricos: eventos adversos hemodinâmicos ocorreram em pacientes pediátricos com instabilidade cardiovascular. Por isso a administração intravenosa rápida deve ser evitada nessa população. Por causa do risco aumentado de apneia1, aconselha-se extrema cautela ao sedar pacientes pré-termo e antes de pré-termo sem entubação traqueal.
Injeção4 rápida deve ser evitada na população neonatal.
O neonato28 tem função orgânica reduzida e/ou imatura e também é vulnerável aos efeitos respiratórios profundos e/ou prolongados de Dormonid® injetável e Dormonid® comprimidos.
Embora rara, a ocorrência de eventos adversos cardiorrespiratórios graves com de risco de morte, incluindo depressão respiratória, apneia1, parada respiratória e/ou parada cardíaca, é mais provável em crianças e adultos acima de 60 anos. Além disso, em crianças e idosos, foi relatada incidência21 mais elevada de sensibilidade a reações paradoxais, tais como agitação, movimentos involuntários (incluindo convulsões tônico-clônicas e tremores musculares), hiperatividade, hostilidade, reação de raiva20, agressividade, excitação e agressão com Dormonid® injetável e Dormonid® comprimidos.
Portanto, em crianças e adultos acima de 60 anos, a dose deve ser determinada com cautela, levando-se em consideração os fatores especiais relacionados a cada paciente (vide “Posologia”).
Pacientes com insuficiência renal6: em pacientes com insuficiência renal6, a farmacocinética de midazolam livre é similar à relatada em voluntários sadios. Entretanto, em pacientes com doença renal29 crônica, pode ocorrer um acúmulo de α-hidroximidazolam, contribuindo para a sedação10 prolongada.
Tabela 1 – Tempo para despertar (h) após cessar a infusão de midazolam
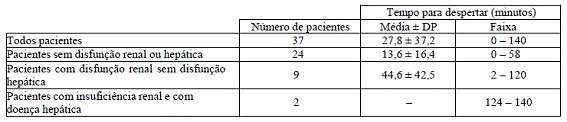
Pacientes com insuficiência hepática7
A insuficiência hepática7 reduz o clearance de midazolam I.V. com um aumento subsequente da meia-vida. Portanto, os efeitos clínicos podem ser mais intensos e prolongados. A dose necessária de midazolam pode ser reduzida e deve ser estabelecida monitoração adequada dos sinais vitais30 (vide “Posologia”).
Grupos específicos de pacientes
Pacientes idosos e debilitados: a dose recomendada de Dormonid® comprimidos é de 7,5 mg (vide “Posologia”).
Pacientes com insuficiência respiratória crônica5: é recomendada a dose mais baixa, por causa do risco de depressão respiratória (vide “Posologia”).
Benzodiazepínicos não são recomendados como tratamento principal de transtornos psicóticos.
Benzodiazepínicos não devem ser utilizados isoladamente para tratar depressão ou ansiedade associada à depressão, pois podem facilitar impulso suicida em pacientes em condições especificas de saúde31.
Crianças pré-termo: por causa do risco aumentado de apneia1, aconselha-se extrema cautela ao sedar pacientes pré-termo menores que 36 semanas de idade gestacional sem entubação traqueal. Deve-se evitar injeção4 rápida. É necessária monitoração cuidadosa da taxa respiratória e da saturação de oxigênio.
Pacientes pediátricos menores que 6 meses de idade são particularmente vulneráveis à obstrução de vias aéreas e hipoventilação. Nesses casos, a titulação com pequenos incrementos até o efeito clínico e monitoração cuidadosa da taxa respiratória e da saturação de oxigênio são essenciais.
Uso concomitante de álcool/depressores do SNC32: o uso concomitante de Dormonid® com álcool e/ou depressores do SNC32 deve ser evitado. O uso concomitante tem o potencial de aumentar os efeitos clínicos de Dormonid®, podendo incluir sedação10 grave, depressão respiratória e/ou cardiovascular clinicamente revelante (vide item “Interações Medicamentosas”).
Histórico médico de abuso de álcool e de drogas: Dormonid® deve ser evitado por pacientes com um histórico médico de abuso de álcool e de drogas.
Outros: assim como com qualquer substância depressora do sistema nervoso central33 e/ou com propriedades musculorrelaxantes, deve-se ter cuidado especial ao administrar Dormonid® a pacientes com miastenia34 gravis, por causa da fraqueza muscular preexistente.
Efeitos na habilidade de dirigir veículo ou operar máquinas
Sedação10, amnésia19, redução da capacidade de concentração e da força muscular prejudicam a capacidade de dirigir veículo ou operar máquinas. Antes de receber Dormonid® injetável, o paciente deve ser alertado para não dirigir veículo ou operar máquina até a sua recuperação.
Na administração de Dormonid® comprimidos, deve-se levar em consideração que se a duração do sono for insuficiente, é maior a probabilidade de redução da atenção (vide também “Interações Medicamentosas”).
Gravidez35 e lactação36
Categoria de risco na gravidez35: C. Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Não há dados suficientes sobre midazolam para avaliar sua segurança durante a gravidez35. Os benzodiazepínicos devem ser evitados durante a gravidez35 a não ser que não exista alternativa mais segura. Se o produto for prescrito à mulher em idade fértil, ela deve ser avisada de que deve procurar seu médico para descontinuar o medicamento, em caso de pretender engravidar ou se suspeitar de gravidez35. A administração de Dormonid® injetável e Dormonid® comprimidos no terceiro trimestre de gestação ou em altas doses durante o trabalho de parto pode produzir irregularidades no batimento cardíaco fetal, hipotonia37, sucção fraca, hipotermia38 e moderada depressão respiratória em neonatos27. Além disso, bebês39 nascidos de mães que receberam benzodiazepínicos cronicamente durante o último estágio da gravidez35 podem ter desenvolvido dependência física e podem estar sob algum risco de desenvolver sintomas13 de abstinência no período pós-natal.
Uma vez que o midazolam passa para o leite materno, Dormonid® comprimidos não deve ser administrado às mães que estejam amamentando.
Mulheres que estejam amamentando devem interromper o aleitamento durante 24 horas após a administração do Dormonid® injetável.
Até o momento, não há informações de que Dormonid® injetável (midazolam) e Dormonid® comprimidos (maleato de midazolam) possam causar doping.


