
INFORMAÇÕES TÉCNICAS CELEBRA
Propriedades Farmacodinâmicas
Grupo farmacoterapêutico: M01AH coxibes.
O mecanismo de ação do celecoxibe é via inibição da síntese das prostaglandinas1, principalmente pela inibição da enzima2 ciclooxigenase 2 (COX-2). Em concentrações terapêuticas em humanos, celecoxibe não inibe a ciclooxigenase 1 (COX-1). A COX-2 é induzida em resposta a estímulos inflamatórios. Isto leva à síntese e ao acúmulo de prostanóides inflamatórios, em particular a prostaglandina3 E2, causando inflamação4, edema5 e dor. O celecoxibe age como um agente antiinflamatório, analgésico6 e antipirético7 em modelos animais pelo bloqueio da produção de prostanóides inflamatórios via inibição da COX-2. Em modelos animais de tumores de colo8, celecoxibe reduziu a incidência9 e a multiplicidade dos tumores.
Estudos in vivo e ex vivo mostram que celecoxibe tem afinidade muito baixa pela enzima2 ciclooxigenase 1 (COX-1) de expressão constitutiva. Conseqüentemente, em doses terapêuticas, celecoxibe não tem efeito sobre prostanóides sintetizados pela ativação da COX-1, não interferindo, portanto, nos processos fisiológicos relacionados à COX-1 nos tecidos, particularmente no estômago10, intestino e plaquetas11.
Estudos Clínicos
Osteoartrite12 (OA):
O celecoxibe demonstrou uma redução significativa na dor articular em comparação com o placebo13. O celecoxibe foi avaliado para o tratamento dos sinais14 e sintomas15 da osteoartrite12 do joelho e quadril em aproximadamente 4.200 pacientes de estudos clínicos controlados por placebo13 e por agente ativo com até 12 semanas de duração. Em pacientes com osteoartrite12, o tratamento com celecoxibe 100 mg duas vezes ao dia ou 200 mg em dose única diária resultou em melhora do índice de osteoartrite12 de WOMAC (Western Ontario and McMaster Universities), um índice composto de dor, rigidez, e medidas funcionais em osteoartrite12.
Em três estudos de 12 semanas de duração em osteoartrite12 acompanhada de dor e vermelhidão, as doses de celecoxibe de 100 mg duas vezes ao dia e 200 mg duas vezes ao dia proporcionaram redução significativa da dor dentro de 24-48 horas após o início da administração. Em doses de 100 mg duas vezes ao dia ou 200 mg duas vezes ao dia, a eficácia do celecoxibe mostrou ser semelhante à do naproxeno 500 mg duas vezes ao dia. Doses de 200 mg duas vezes ao dia não proporcionaram benefício adicional acima do observado com 100 mg duas vezes ao dia. Uma dose diária total de 200 mg mostrou ser igualmente eficaz quer seja administrada como 100 mg duas vezes ao dia ou como 200 mg em dose única diária.
Artrite Reumatóide16 (AR):
O celecoxibe demonstrou uma redução significativa na sensibilidade/dor articular e no inchaço17 articular em comparação com o placebo13. O celecoxibe foi avaliado para o tratamento dos sinais14 e sintomas15 de artrite reumatóide16 em aproximadamente 2100 pacientes em estudos clínicos controlados por placebo13 e por agente ativo com até 24 semanas de duração. O celecoxibe mostrou ser superior ao placebo13 nestes estudos, quando se utilizou o Índice de Resposta ACR20, um índice composto de medidas clínicas, laboratoriais e funcionais da artrite reumatóide16. As doses de celecoxibe 100 mg duas vezes ao dia e 200 mg duas vezes ao dia apresentaram eficácia semelhante e ambas foram comparáveis à eficácia do naproxeno 500 mg duas vezes ao dia.
Embora o celecoxibe nas doses de 100 mg duas vezes ao dia e 200 mg duas vezes ao dia tenha proporcionado eficácia global semelhante, alguns pacientes obtiveram benefício adicional com a dose de 200 mg duas vezes ao dia. Doses de 400 mg duas vezes ao dia não proporcionaram benefício adicional acima do observado com 100-200 mg duas vezes ao dia.
Analgesia em dor aguda, incluindo Dismenorréia18 Primária:
Nos modelos de analgesia aguda de dor pós-cirurgia oral, dor pós-cirurgia ortopédica, e dismenorréia18 primária, o celecoxibe aliviou a dor classificada pelos pacientes como moderada a grave. Doses únicas (vide “Posologia”) de celecoxibe proporcionaram alívio da dor dentro de um período de 60 minutos.
Espondilite Anquilosante (EA):
O celecoxibe foi avaliado em pacientes com espondilite anquilosante em dois estudos clínicos placebo13-controlados por placebo13 e por agente ativo com 6 e 12 semanas de duração. O celecoxibe nas doses de 100 mg duas vezes ao dia, 200 mg em dose única diária e 400 mg em dose única diária mostrou ser estatisticamente superior ao placebo13 nestes estudos para todas as três medidas de eficácia co-primárias que avaliam a intensidade de dor global (Escala Analógica Visual), atividade da doença global (Escala Analógica Visual) e comprometimento funcional (Índice Funcional de Espondilite Anquilosante de Bath). No estudo de 12 semanas, não houve diferença no nível de melhora entre as doses de 200 mg e 400 mg de celecoxibe em uma comparação de alteração média em relação ao basal, porém houve uma maior porcentagem de pacientes que responderam ao celecoxibe 400 mg (53%) do que ao celecoxibe 200 mg (44%), utilizando-se a Avaliação dos critérios de resposta de Espondilite Anquilosante (ASAS 20). A ASAS 20 define resposta de um paciente ao tratamento como melhora em relação ao basal de pelo menos 20% e melhora absoluta de pelo menos 10 mm, em uma escala de 0 a 100 mm, em pelo menos três de quatro dos seguintes domínios: avaliação global do paciente, dor, Índice Funcional de Espondilite Anquilosante de Bath, e inflamação4. A análise de resposta também demonstrou ausência de alteração nas taxas de resposta em períodos superiores a 6 semanas.
Polipose Adenomatosa Familiar (PAF):
O celecoxibe foi avaliado na regressão e redução do número de pólipos19 adenomatosos colorretais, que pode levar ao desenvolvimento do câncer20 colorretal em pacientes com polipose adenomatosa familiar (PAF), como adjunto aos cuidados usuais (por ex., vigilância endoscópica e cirúrgica). Em um estudo randomizado21, duplo-cego, placebo13 controlado de 6 meses de duração, celecoxibe 400 mg, duas vezes ao dia, mostrou ser estatisticamente superior ao placebo13 em relação ao percentual de redução do número de pólipos19 colorretais (p = 0,003) e do peso do pólipo22 medido pela luz do diâmetro do pólipo22 (p = 0,001). Além disso, celecoxibe demonstrou superioridade clínica e estatística (p < 0,04) na melhora total endoscópica no colo8, reto23 e duodeno24. O celecoxibe foi efetivo e bem tolerado com doses de 400 mg duas vezes ao dia. Vide tabela 1.
Tabela 1 – Alteração da porcentagem média das variáveis de eficácia em Pacientes com PAF*
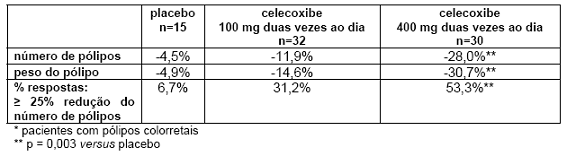
O perfil dos eventos adversos relatados pelos pacientes com PAF nos estudos clínicos, foi similar ao relatado pelos pacientes em estudos controlados de artrite25.
Estudos em Dismenorréia18:
Dois estudos foram realizados para avaliar a eficácia do celecoxibe em dismenorréia18, ambos randômicos, duplo-cego, com 3 braços cruzados, que compararam celecoxibe (n=253) a naproxeno (n=251) e placebo13 (n=256). Nos dois estudos as pacientes receberam a dose inicial da medicação definida randomicamente (celecoxibe 400 mg, naproxeno 550 mg ou placebo13) no primeiro dia do ciclo menstrual e, se necessário, doses das mesmas medicações (celecoxibe 200 mg, naproxeno 550 mg e placebo13) eram repetidas a cada 12 horas por 3 dias.
Em todas as medidas de eficácia utilizadas (tempo até o alívio da dor, redução da intensidade da dor nas 8 e 12 horas, seguintes a dose inicial; manutenção da intensidade da analgesia durante os 3 dias de tratamento – quando necessário – e o uso de medicação analgésica de resgate) celecoxibe e naproxeno foram estatisticamente superiores ao placebo13 (p<0,001). A avaliação do paciente em relação a eficácia do tratamento também foi superior (p<0,01) nos braços em que as medicações ativas foram usadas.
Informações Adicionais de Estudos Clínicos
Estudos endoscópicos
As avaliações endoscópicas do trato gastrintestinal foram realizadas em mais de 4.500 pacientes com artrite25 que foram admitidos em cinco estudos randomizados e controlados de 12-24 semanas de duração que utilizaram agentes comparativos ativos, dois dos quais também incluíram controles com placebo13. Não houve relação consistente entre a incidência9 de úlceras26 gastroduodenais e a dose de celecoxibe dentro do intervalo estudado.
A Tabela 2 resume a incidência9 de úlceras26 endoscópicas em dois estudos de 12 semanas de duração que admitiram pacientes cujas endoscopias basais revelaram inexistência de úlceras26.
Tabela 2 - Incidência9 de úlceras26 gastroduodenais dos estudos endoscópicos em pacientes com osteoartrite12 e artrite reumatóide16
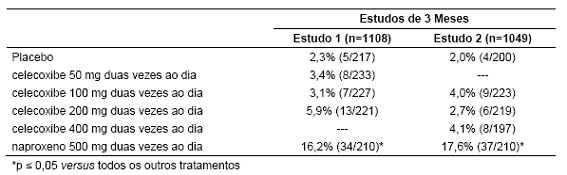
A Tabela 3 resume os dados de dois estudos de 12 semanas que incluiu pacientes cujas endoscopias basais revelaram ausência de úlceras26. Os pacientes foram submetidos a intervalos entre as endoscopias a cada 4 semanas para fornecer informações sobre o risco de úlcera27 em função do tempo.
Tabela 3 - Incidência9 de úlceras26 gastroduodenais de estudos de endoscopias seriais de 3 meses em pacientes com osteoartrite12 e artrite reumatóide16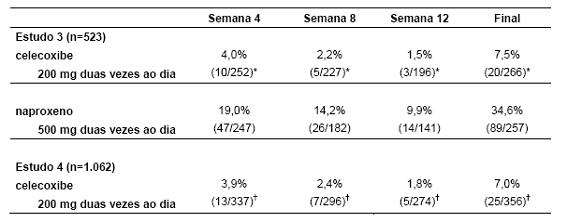

Foi conduzido um estudo randomizado21 e duplo-cego de 6 meses de duração em 430 pacientes com artrite reumatóide16, no qual um exame endoscópico foi realizado no 6º mês.
A incidência9 de úlceras26 endoscópicas em pacientes recebendo celecoxibe 200 mg duas vezes ao dia foi de 4% versus 15% para pacientes28 recebendo diclofenaco SR (liberação prolongada) 75 mg duas vezes ao dia (p < 0,001).
Em 4 dos 5 estudos endoscópicos, aproximadamente 11% dos pacientes (440/4.000) estavam tomando ácido acetilsalicílico (≤ 325 mg/dia). Nos grupos celecoxibe, a taxa de úlcera27 endoscópica pareceu ser maior nos usuários de ácido acetilsalicílico do que nos não usuários. No entanto, a taxa aumentada de úlceras26 nestes usuários de ácido acetilsalicílico foi menor que a taxa de úlceras26 endoscópicas observada nos grupos com agentes comparativos ativos, com ou sem ácido acetilsalicílico.
A correlação entre os achados dos estudos endoscópicos e a incidência9 relativa de eventos sérios clinicamente significativos no trato gastrintestinal superior29 não foi estabelecida. Sangramento sério clinicamente significativo no trato gastrintestinal superior29 foi observado, embora infreqüentemente, em pacientes recebendo celecoxibe em estudos controlados e abertos (vide “Advertências e Precauções - Efeitos Gastrintestinais (GI)”).
Meta-análises em Segurança Gastrintestinal de Estudos em Osteoartrite12 e Artrite Reumatóide16
Uma análise de 31 estudos clínicos controlados randomizados em osteoartrite12 e artrite reumatóide16, envolvendo 39.605 pacientes com osteoartrite12 (n=25.903), artrite reumatóide16 (n=3.232) ou pacientes com outras condições (n=10.470), comparou a incidência9 de eventos adversos gastrintestinais em pacientes tratados com celecoxibe e pacientes recebendo placebo13 ou AINEs (incluindo naproxeno, diclofenaco e ibuprofeno). A incidência9 clínica de úlcera27 e sangramento da úlcera27 com celecoxibe na dose diária total de 200 - 400 mg foi de 0,2% comparado com a incidência9 de 0,6% com AINEs (RR=0,35; 95% IC 0,22–0,56).
Estudo de Segurança Prolongada do celecoxibe em Artrite25 (CLASS) incluindo o uso concomitante de ácido acetilsalicílico (AAS- Aspirina)
Em um estudo prospectivo30 prolongado de resultados da segurança conduzido na fase pós-comercialização em aproximadamente 5.800 pacientes com osteoartrite12 e 2.200 pacientes com artrite reumatóide16, os pacientes receberam celecoxibe 400 mg duas vezes ao dia (4 vezes e 2 vezes as doses recomendadas para osteoartrite12 e artrite reumatóide16, respectivamente, e a dose aprovada para polipose adenomatosa familiar), ibuprofeno 800mg 3 vezes/dia ou diclofenaco 75 mg duas vezes ao dia (doses terapêuticas usuais). As exposições medianas para o celecoxibe (n=3.987) e o diclofenaco (n=1.996) foram de 9 meses enquanto com o ibuprofeno (n=1.985) foi de 6 meses.
As taxas cumulativas de Kaplan-Meier em 9 meses são fornecidas para todas as análises. O endpoint primário deste estudo foi a incidência9 de úlceras26 complicadas (sangramento gastrintestinal, perfuração ou obstrução). Os pacientes podiam tomar ácido acetilsalicílico (AAS) em baixa dose concomitante (≤ 325 mg/dia) como profilático cardiovascular (subgrupos de AAS: celecoxibe, n=882; diclofenaco, n=445; ibuprofeno, n=412). As diferenças de incidência9 de úlceras26 complicadas entre o celecoxibe e o grupo combinado de ibuprofeno e diclofenaco não foram estatisticamente significativas. Os pacientes recebendo celecoxibe e AAS em baixa dose concomitante apresentaram taxas 4 vezes maiores de úlceras26 complicadas em comparação com os que não receberam AAS (vide “Advertências e Precauções - Efeitos Gastrintestinais (GI)”). Os resultados para celecoxibe encontram-se na Tabela 4.
Tabela 4 - Efeitos da co-administração de ácido acetilsalicílico em baixa dose sobre as taxas de úlcera27 complicada com celecoxibe 400 mg duas vezes ao dia (Taxas de Kaplan-Meier em 9 meses [%])
Função plaquetária
Em voluntários sadios, o celecoxibe em doses terapêuticas e em doses múltiplas de 600 mg duas vezes ao dia (três vezes a dose mais alta recomendada) não apresentou efeito sobre a agregação plaquetária e tempo de sangramento em comparação com o placebo13. Todos os controles ativos (Inibidores inespecíficos da COX) reduziram significativamente a agregação plaquetária e prolongaram o tempo de sangramento.
Estudo de Celecoxibe versus Omeprazol e Diclofenaco em pacientes sob risco de Osteoartrite12 e Artrite Reumatóide16 (CONDOR)
Neste estudo prospectivo30 de 24 semanas em pacientes com idade ≥60 anos ou com histórico de úlcera27 gastroduodenal (excluindo usuários de aspirina em baixa dose), a porcentagem de pacientes com eventos gastrintestinais clinicamente significativos (endpoint primário composto) foi menor em pacientes tratados com celecoxibe 200 mg duas vezes ao dia comparado aos pacientes tratados com diclofenaco SR 75 mg duas vezes ao dia + omeprazol 20 mg uma vez ao dia. Este resultado é baseado na diminuição clinicamente significativa na hemoglobina31 (≥2g/dL) e/ou hematócrito32 (≥10%) de origem gastrintestinal definida ou suposta. Os resultados dos desfechos individuais desse endpoint composto foram os seguintes:
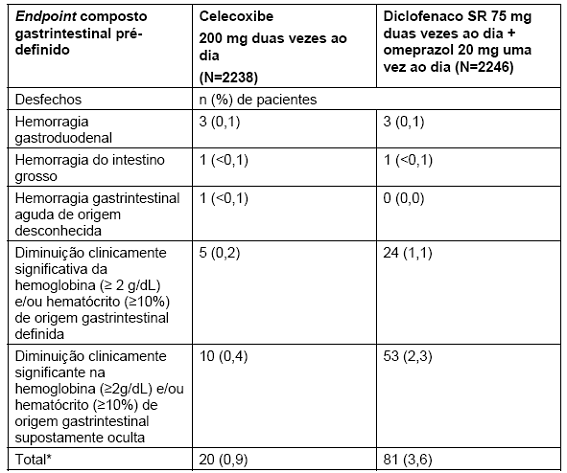
Para os seguintes componentes do endpoint composto gastrintestinal pré-definido, não houve eventos em ambos os grupos de tratamento: obstrução da saída gástrica; perfuração gastroduodenal, do intestino delgado33 ou do intestino grosso34; hemorragia35 do intestino delgado33. Todos os eventos compreendendo o endpoint composto gastrintestinal foram avaliados por um grupo de especialistas independente que não tinha conhecimento de qual grupo randomizado36 de tratamento o paciente fazia parte.
* Em uma análise de tempo para ocorrência de um desfecho, P<0,0001 para a comparação entre o grupo de tratamento com celecoxibe e o grupo de tratamento com omeprazol + diclofenaco para este endpoint.
Segurança cardiovascular – estudos a longo prazo envolvendo pacientes com pólipos19 adenomatosos esporádicos
Foram conduzidos dois estudos com celecoxibe envolvendo pacientes com pólipos19 adenomatosos esporádicos por ex., estudo APC (Adenoma37 Prevention with Celecoxib) e o estudo PreSAP (Prevention of Spontaneous Adenomatous Polyps). No estudo APC, houve um aumento dose-relacionado ao endpoint composto de morte cardiovascular, infarto do miocárdio38 e derrame39 (julgado) com celecoxibe comparado ao placebo13 por mais de 3 anos de tratamento. O estudo PreSAP não demonstrou um aumento de risco estatisticamente significativo para o mesmo endpoint.
No estudo APC, os riscos relativos comparados ao placebo13 para o endpoint composto de morte cardiovascular, infarto do miocárdio38 ou derrame39 (julgado) foram 3,4 (95% IC 1,4-8,5) com celecoxibe 400 mg duas vezes ao dia e 2,8 (95% IC 1,1–7,2) com celecoxibe 200 mg duas vezes ao dia (taxas cumulativas para o endpoint composto por mais de 3 anos de estudo em 20/671 indivíduos, 3,0% e 17/685 indivíduos, 2,5%, respectivamente, comparado a 6/679 indivíduos, 0,9% para placebo13). Os aumentos para ambos os grupos de doses de celecoxibe versus placebo13 foram devidos principalmente ao infarto do miocárdio38.
No estudo PreSAP, o risco relativo comparado ao palcebo para o mesmo endpoint composto foi de 1,2 (95% IC 0,6–2,4) com celecoxibe 400 mg uma vez ao dia (taxas cumulativas para o endpoint composto por mais de 3 anos foram 21/933 indivíduos, 2,3% comparado a 12/628 indivíduos, 1,9% para placebo13).
Segurança cardiovascular – meta-análise de estudos com uso crônico40
Não foi conduzido qualquer estudo clínico de longo prazo controlado e delineado especificamente para avaliar a segurança cardiovascular na administração crônica de celecoxibe com qualquer duração. Entretanto, foi conduzida uma meta-análise dos dados de segurança (eventos adversos considerados sérios pelo investigador) de 39 estudos clínicos completos com celecoxibe, de até 65 semanas de duração, representando 41.077 pacientes (23.030 (56,1%) pacientes expostos ao celecoxibe dose diária total de 200 – 800 mg, 13.990 (34,1%) pacientes expostos aos AINEs não-seletivos e 4.057 (9,9%) pacientes expostos ao placebo13).
Nesta análise, a taxa de eventos considerados para o endpoint composto de morte cardiovascular, infarto do miocárdio38 não-fatal e derrame39 não-fatal foi similar entre celecoxibe (n=19.773; 0,96 eventos/100 pacientes-ano) e o tratamento com AINEs não-seletivos (n=13.990; 1,12 eventos/100 pacientes-ano) (RR=0,90; 95% IC 0,60-1,33). Este padrão de efeito foi mantido com ou sem o uso do ácido acetilsalicílico (≤ 325 mg). Houve uma incidência9 maior de infarto do miocárdio38 não-fatal (RR=1,76; 95% IC 0,93–3,35). Entretanto, houve uma tendência de derrame39 não-fatal menor (RR=0,51; 95% IC 0,23-1,10) e a incidência9 de morte cardiovascular foi similar (RR=0,57; 95% IC 0,28-1,14) para celecoxibe comparado aos AINEs não-seletivos combinados.
Nesta análise, a taxa de eventos considerados do endpoint composto de morte cardiovascular, infarto do miocárdio38 não-fatal e derrame39 não-fatal foi de 1,42/100 paciente-ano para o tratamento com celecoxibe (n=7.462) e 1,20/100 pacientes-ano para placebo13 (n=4.057) (RR=1,11; 95% IC 0,47-2,67). Este padrão de efeito foi mantido com ou sem o uso de ácido acetilsalicílico (≤ 325 mg). Houve uma tendência maior de incidência9 de infarto do miocárdio38 não-fatal (RR=1,56; 95% IC 0,21-11,90) e de morte cardiovascular (RR=1,26; 95% IC 0,33-4,77), e a de derrame39 não-fatal foi similar (RR=0,80; 95% IC 0,19-3,31) para celecoxibe comparada ao placebo13.
Segurança cardiovascular
Os resultados de segurança cardiovascular foram avaliados no estudo CLASS. As taxas cumulativas Kaplan-Meier para os eventos adversos tromboembólicos cardiovasculares sérios relatados pelo investigador (incluindo infarto do miocárdio38, embolia41 pulmonar, trombose venosa profunda42, angina43 instável, ataque isquêmico44 transitório e acidente cerebrovascular isquêmico44) não demonstraram diferenças entre os grupos de tratamento com celecoxibe, diclofenaco ou ibuprofeno. As taxas cumulativas em todos os pacientes no nono mês para celecoxibe, diclofenaco e ibuprofeno foram 1,2%, 1,4% e 1,1% respectivamente. As taxas cumulativas em pacientes que não estavam utilizando o ácido acetilsalicílico no nono mês em cada um dos 3 grupos de tratamento foram menores que 1%. As taxas cumulativas para infarto do miocárdio38 em pacientes não-usuários de ácido acetilsalicílico no nono mês em cada um dos 3 grupos de tratamento foram menores que 0,2%. Não havia grupo placebo13 no estudo CLASS, o que limita a possibilidade de determinar se os 3 fármacos testados não tinham aumento de risco de eventos cardiovasculares ou se eles todos tiveram o risco aumentado em um grau similar.
Propriedades Farmacocinéticas
Absorção
A farmacocinética do celecoxibe foi avaliada em aproximadamente 1.500 indivíduos. Quando administrado em condições de jejum, o celecoxibe é bem absorvido atingindo concentrações plasmáticas máximas após aproximadamente 2-3 horas. A biodisponibilidade oral das cápsulas é de cerca de 99% em relação à administração em suspensão (forma farmacêutica oral de disponibilidade ideal). Em condições de jejum, tanto os níveis plasmáticos máximos (Cmáx) como as áreas sob a curva (AUC45) são quase proporcionais à dose de até 200 mg duas vezes ao dia; em doses mais altas, ocorrem aumentos menos proporcionais na Cmáx e AUC45.
Distribuição
A taxa de ligação a proteínas46 plasmáticas, que é independente da concentração, é de cerca de 97% em concentrações plasmáticas terapêuticas e o celecoxibe não se liga preferencialmente aos eritrócitos47 no sangue48.
Efeitos dos alimentos
A administração com alimentos (refeição rica em gorduras) retarda a absorção do celecoxibe resultando em um Tmáx de cerca de 4 horas e aumenta a biodisponibilidade em cerca de 20% (vide “Posologia”).
Em voluntários adultos saudáveis, a exposição sistêmica global (AUC45) de celecoxibe foi equivalente quando o celecoxibe foi administrado como cápsulas intactas ou cápsulas abertas cujo conteúdo foi misturada a suco de maçã. Não houve alterações significantes no Cmax, Tmax ou T1/2 após a administração do conteúdo das cápsulas abertas misturadas a suco de maçã.
Metabolismo49
O metabolismo49 de celecoxibe é mediado principalmente pela via citocromo P450 2C9. Foram identificados 3 metabólitos50, inativos como os inibidores da COX-1 e COX-2, no plasma51 humano por ex., álcool primário, o ácido carboxílico correspondente e seu glicuronídeo conjugado.
A atividade do citocromo P450 2C9 é reduzida em indivíduos com polimorfismo genético que levam à atividade reduzida da enzima2, tais como aquelas homozigóticas para o polimorfismo CYP2C9*3.
Em um estudo farmacocinético de celecoxibe 200 mg administrado uma vez ao dia em voluntários sadios, genotipados como CYP2C9*1/*1, CYP2C9*1/*3 ou CYP2C9*3/*3, a média de Cmáx e AUC0-24 de celecoxibe no 7º dia foram de aproximadamente 4 vezes e 7 vezes, respectivamente, em indivíduos genotipados como CYP2C9*3/*3 comparados aos outros genótipos. Em três estudos diferentes de dose única, envolvendo um total de 5 indivíduos genotipados como CYP2C9*3/*3, AUC0-24 aumentada com dose única em aproximadamente 3 vezes comparado aos metabolizadores normais. É estimado que a freqüência do genótipo52 homozigoto *3/*3 é 0,3-1,0% entre os diferentes grupos étnicos.
O celecoxibe deve ser administrado com cautela a pacientes com deficiência ou suspeita de deficiência de metabolizadores CYP2C9 baseados no histórico prévio/experiência com outros substratos CYP2C9. Considerar o início de tratamento com a metade da menor dose recomendada (vide “Posologia” e “Interações Medicamentosas”).
Excreção
O celecoxibe é eliminado predominantemente por metabolismo49 hepático, com pequena concentração (< 1%) da dose excretada inalterada na urina53. Após múltiplas doses, a meia-vida de eliminação é de 8 a 12 horas e o clearance é de aproximadamente 500 mL/min. Com administrações múltiplas, as condições do estado de equilíbrio são atingidas até o 5o dia. A variação dos parâmetros farmacocinéticos (AUC45, Cmáx e meia-vida) entre indivíduos é da ordem de 30%. O volume médio de distribuição é de aproximadamente 500 litros por 70 kg em indivíduos jovens adultos saudáveis, indicando extensa distribuição em todos os tecidos. Estudos pré-clínicos indicam que o celecoxibe atravessa a barreira hematoencefálica.
Populações Especiais
Idosos: na população com idade >65 anos, ocorre um aumento de 1,5 a 2 vezes a média de Cmáx e de AUC45 para o celecoxibe. Esta é uma alteração predominantemente relacionada ao peso em vez de ser relacionada à idade, os níveis de celecoxibe ficando mais altos em indivíduos de menor peso e, conseqüentemente mais altos na população idosa, que geralmente apresenta peso médio inferior ao peso médio da população mais jovem. Portanto, as mulheres idosas tendem a apresentar concentrações plasmáticas do fármaco54 mais altas do que os homens idosos. Geralmente não é necessário ajuste de dose. No entanto, para pacientes28 idosos com menos de 50 kg, deve-se introduzir o tratamento com a menor dose recomendada.
Raça: uma meta-análise de estudos farmacocinéticos sugeriu que a AUC45 de celecoxibe é aproximadamente 40% maior em pacientes da raça negra quando comparada a pacientes da raça branca. A causa e significado clínico desse achado não são conhecidos e, portanto, o tratamento deve ser iniciado com a menor dose recomendada.
Insuficiência hepática55: as concentrações plasmáticas de celecoxibe em pacientes com insuficiência hepática55 leve (classe A de Child-Pugh) não são significativamente diferentes dos controles pareados por sexo e idade. Em pacientes com insuficiência hepática55 moderada (classe B de Child-Pugh) a concentração plasmática de celecoxibe é cerca de 2 vezes a do grupo controle. Para doses em pacientes com insuficiência hepática55 grave (classe C de Child-Pugh) vide “Posologia”.
A dose diária recomendada de Celebra® (celecoxibe) deve ser reduzida à metade em pacientes com polipose adenomatosa familiar (PAF) com insuficiência hepática55 moderada.
Insuficiência renal56: a farmacocinética do celecoxibe em indivíduos idosos com redução do ritmo de filtração glomerular (RFG) relacionada à idade (RFG médio > 65 mL/min/1,73 m2) e em pacientes com insuficiência renal56 crônica estável (RFG entre 35 e 60 mL/min/1,73 m2) foi comparável a de indivíduos com função renal57 normal. Não foi descoberta relação significante entre creatinina58 sérica (ou clearance de creatinina58) e clearance de celecoxibe. Em insuficiência renal56 grave, não é esperada uma alteração do clearence de celecoxibe uma vez que a principal via de eliminação é hepática59 para metabólitos50 inativos.
Efeitos renais: até o presente momento, o papel das enzimas ciclooxigenase 1 e 2 na fisiologia60 renal57 ainda não é plenamente conhecido. O celecoxibe reduz a excreção urinária de PGE2 e da 6-ceto-PGF1 (um metabólito61 da prostaciclina), mas não altera o nível sérico de tromboxano B2 (TXB2), e a excreção urinária de 11-deidro-TXB2, um metabólito61 do tromboxano inalterado (ambos resultantes da atividade da COX-1). Estudos específicos demonstraram que celecoxibe não produz diminuição do ritmo de filtração glomerular em idosos ou em pacientes com insuficiência renal56 crônica. Estes estudos também demonstraram reduções transitórias na excreção fracionada de sódio. Nos estudos conduzidos em pacientes com artrite25, uma incidência9 comparável de edema5 periférico foi observada em relação à verificada com inibidores inespecíficos da COX (que também apresentam atividade inibitória da COX-2). Isto foi mais evidente em pacientes recebendo terapia diurética concomitante. No entanto, não foram observados aumentos das incidências de hipertensão62 e insuficiência cardíaca63 e o edema5 periférico foi leve e auto-limitante.
Dados de Segurança Pré-clínica
Dados de segurança pré-clínica revelam ausência de risco especial para humanos com base nos estudos convencionais de toxicidade64 de dose repetida, mutagenicidade ou carcinogenicidade. Estudos de toxicidade64 embrio-fetais convencionais resultaram em ocorrências dose-dependentes de hérnia65 de hiato em fetos de ratos e malformações66 cardiovasculares em fetos de coelhos. Em ambas as espécies, estes efeitos foram observados em níveis de exposição sistêmica 5-6 vezes os observados na dose clínica mais alta recomendada (400 mg/dia).
Em ratos, a exposição ao celecoxibe durante o início do desenvolvimento embrionário resultou em perdas pré- e pós-implantação, e reduziu a sobrevida67 embrio/fetal. Estes efeitos, que foram observados em doses orais de aproximadamente 6 vezes a exposição sistêmica em humanos, são esperados devido à inibição da síntese de prostaglandina3.
Toxicologia
Um aumento na incidência9 de achados experimentais de espermatocele com ou sem alterações secundárias, assim como hipoespermia epididimal mínima, assim como insignificante dilatação dos túbulos seminíferos tem sido encontrado em ratos jovens. Estes achados reprodutivos aparentemente relacionados ao tratamento, não aumentaram a incidência9 ou severidade com dose, e pode indicar uma exarcebação de uma condição espontânea. Achados reprodutivos similares não foram observados em estudos com cachorros jovens e adultos ou em ratos adultos tratados com celecoxibe. A significância clínica desta observação é desconhecida


