
CARACTERÍSTICAS MERONEM IV
Propriedades Farmacodinâmicas
O meropeném é um antibiótico carbapenêmico para uso parenteral que é estável à deidropeptidase-I humana (DHP-I). O meropeném é estruturalmente similar ao imipeném.
O meropeném exerce sua ação bactericida através da interferência com a síntese da parede celular bacteriana. A facilidade com que penetra nas células1 bacterianas, seu alto nível de estabilidade a todas as serinas beta-lactamases e sua notável afinidade pelas proteínas2 ligantes de penicilina (PBPs) explicam a potente atividade bactericida de meropeném contra um amplo espectro de bactérias aeróbicas e anaeróbicas. As concentrações bactericidas estão geralmente dentro do dobro da diluição das concentrações inibitórias mínimas (CIMs).
O meropeném é estável em testes de suscetibilidade que podem ser realizados utilizando-se os sistemas de rotina normal. Testes in vitro mostram que meropeném pode atuar de forma sinérgica com vários antibióticos. Demonstrou-se que meropeném, tanto in vitro quanto in vivo, possui um efeito pós-antibiótico contra microorganismos gram-positivos e gram-negativos.
Um conjunto de critérios de suscetibilidade de meropeném são recomendados baseados na farmacocinética e na correlação de resultados clínicos e microbiólogicos com o diâmetro da zona e com a concentração inibitória mínima (CIM) do microorganismo infectante.
| Categorização | Método de estabelecimento |
| Diâmetro da zona (mm) Ponto de ruptura CIM (mg/l) | |
| Suscetível ≥ 14 | ≤ 4 |
| Intermediário 12-13 | 8 |
| Resistente ≤ 11 | ≥ 16 |
O espectro antibacteriano in vitro de meropeném inclui a maioria dos microorganismos gram-positivos e gram-negativos clinicamente significantes e cepas3 de bactérias aeróbicas e anaeróbicas conforme relação abaixo:
Gram-positivos aeróbios:
Bacillus spp.; Corynebacterium diphtheriae; Enterococcus faecalis, Enterococcus liquifaciens, Enterococcus avium; Erysipelothrix rhusiopathiae; Listeria monocytogenes; Lactobacillus spp.; Nocardia asteroides; Staphylococcus aureus (penicilinase-negativos e positivos), Staphylococcus (coagulase-negativos), incluindo: Staphylococcus epidermidis, Staphylococcus saprophyticus, Staphylococcus capitis, Staphylococcus cohnii, Staphylococcus xylosus, Staphylococcus warneri, Staphylococcus hominis, Staphylococcus simulans, Staphylococcus intermedius, Staphylococcus sciuri, Staphylococcus lugdunensis; Streptococcus pneumoniae (sensível e resistente a penicilina), Streptococcus agalactiae, Streptococcus pyogenes, Streptococcus equi, Streptococcus bovis, Streptococcus mitis, Streptococcus mitior, Streptococcus milleri, Streptococcus sanguis, Streptococcus viridans, Streptococcus salivarius, Streptococcus morbillorum, Streptococcus cremoris, Streptococcus Grupo G, Streptococcus Grupo F; Rhodococcus equi.
Gram-negativos aeróbios:
Achromobacter xylosoxidans; Acinetobacter anitratus, Acinetobacter lwoffii, Acinetobacter baumanii, Acinetobacter junii, Acinetobacter haemolyticus; Aeromonas hydrophila, Aeromonas sorbria, Aeromonas caviae; Alcaligenes faecalis; Bordetella bronchiseptica; Brucella melitensis; Campylobacter coli, Campylobacter jejuni; Citrobacter freundii, Citrobacter diversus, Citrobacter koseri, Citrobacter amalonaticus; Enterobacter aerogenes, Enterobacter (Pantoea) agglomerans, Enterobacter cloacae, Enterobacter sakazakii; Escherichia coli, Escherichia hermannii; Gardnerella vaginalis; Haemophilus influenzae (incluindo cepas3 beta-lactamase-positivas e resistentes a ampicilina), Haemophilus parainfluenzae, Haemophilus ducreyi; Helicobacter pylori; Neisseria meningitidis, Neisseria gonorrhoeae (incluindo cepas3 beta-lactamase-positivas, resistentes a penicilina e a espectinomicina); Hafnia alvei; Klebsiella pneumoniae, Klebsiella aerogenes, Klebsiella ozaenae, Klebsiella oxytoca; Moraxella (Branhamella) catarrhalis; Morganella morganii; Proteus mirabilis, Proteus vulgaris, Proteus penneri; Providencia rettgeri, Providencia stuartii, Providencia alcalifaciens; Pasteurella multocida; Plesiomonas shigelloides; Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas alcaligenes, Burkholderia (Pseudomonas) cepacia, Pseudomonas fluorescens, Pseudomonas stutzeri, Pseudomonas pickettii, Pseudomonas pseudomallei, Pseudomonas acidovorans; Salmonella spp. (incluindo Salmonella enteritidis/typhi); Serratia marcescens, Serratia liquefaciens, Serratia rubidaea; Shigella sonnei, Shigella flexneri, Shigella boydii, Shigella dysenteriae; Vibrio cholerae, Vibrio parahaemolyticus, Vibrio vulnificus;Yersinia enterocolitica.
Bactérias anaeróbias:
Actinomyces odontolyticus, Actinomyces meyeri, Actinomyces israellii; Bacteroides-Prevotella-Porphyromonas spp., Bacteroides fragilis, Bacteroides vulgatus, Bacteroides variabilis, Bacteroides pneumosintes, Bacteroides coagulans, Bacteroides uniformis, Bacteroides distasonis, Bacteroides ovatus, Bacteroides thetaiotaomicron, Bacteroides eggerthii, Bacteroides capsillosis, Bacteroides gracilis, Bacteroides levii, Bacteroides caccae, Bacteroides ureolyticus; Prevotella buccalis, Prevotella melaninogenica, Prevotella intermedia, Prevotella bivia, Prevotella corporis, Prevotella splanchnicus, Prevotella oralis, Prevotella disiens, Prevotella rumenicola, Prevotella oris, Prevotella buccae, Prevotella denticola; Porphyromonas asaccharolytica, Porphyromonas gingivalis; Bifidobacterium spp.; Bilophila wadsworthia; Clostridium perfringens, Clostridium bifermentans, Clostridium ramosum, Clostridium sporogenes, Clostridium cadaveris, Clostridium difficile, Clostridium sordellii, Clostridium butyricum, Clostridium clostridiiformis, Clostridium innocuum, Clostridium subterminale, Clostridium tertium; Eubacterium lentum, Eubacterium aerofaciens; Fusobacterium mortiferum, Fusobacterium necrophorum, Fusobacterium nucleatum, Fusobacterium varium; Mobiluncus curtisii, Mobiluncus mulieris; Peptostreptococcus anaerobius, Peptostreptococcus micros, Peptostreptococcus saccharolyticus, Peptostreptococcus asaccharolyticus, Peptostreptococcus magnus, Peptostreptococcus prevotii; Peptococcus saccharolyticus; Propionibacterium acnes, Propionibacterium avidum, Propionibacterium granulosum; Veillonella parvula; Wolinella recta.
Uma comparação da porcentagem de isolados bacterianos totalmente suscetíveis ao meropeném em concentrações de 4 mg/l e 8 mg/l (Tabela 1) em dezembro de 1993, e, a partir desta data, até julho de 1998, mostra que não houve alterações significantes na atividade de meropeném no decorrer deste período de tempo.
Tabela 1: Dados de suscetibilidade de meropeném apresentados como % de linhagens inibidas por meropeném na concentração de 4 mg/l e 8 mg/l em dezembro de 1993, e, a partir desta data, até 1998.
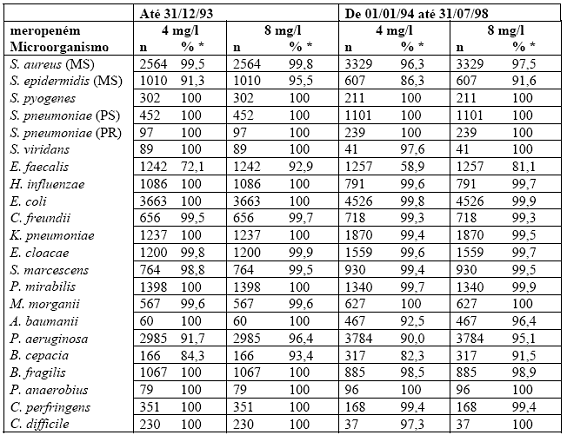
* % suscetível
MS: suscetível à meticilina; PS: suscetível à penicilina; PR: resistente à penicilina.
O meropeném e o imipeném têm um perfil similar de utilidade clínica e atividade contra bactérias multi-resistentes. Entretanto, meropeném é intrinsecamente mais potente contra Pseudomonas aeruginosa e pode ser ativo in vitro contra as cepas3 resistentes ao imipeném.
O meropeném é ativo in vitro contra muitas cepas3 resistentes a outros antibióticos beta-lactâmicos. Isto é explicado parcialmente pela maior estabilidade às beta-lactamases. A atividade in vitro contra cepas3 resistentes a classes de antibióticos não relacionadas, como aminoglicosídeos ou quinolonas, é normal.
Enterococcus faecium, Stenotrophomonas (Xanthomonas) maltophilia e Staphilococcus resistentes à meticilina têm-se mostrado resistentes ao meropeném.
Propriedades Farmacocinéticas
Uma infusão de 30 minutos de uma dose única de MERONEM IV em voluntários sadios resulta em picos de níveis plasmáticos de aproximadamente 11 mcg/ml para doses de 250 mg; 23 mcg/ml para doses de 500 mg; 49 mcg/ml para doses de 1 g e 115 mcg/ml após dose de 2 g.
Uma injeção4 intravenosa (IV) em bolus5 de MERONEM IV com duração de 5 minutos em voluntários sadios resulta em picos de níveis plasmáticos de aproximadamente 52 mcg/ml para a dose de 500 mg e 112 mcg/ml para a dose de 1 g.
Infusões intravenosas de 1 g durante 2, 3 e 5 minutos foram comparadas em um estudo cruzado de três braços. Estas diferentes durações de infusão resultaram em picos de níveis plasmáticos de 110, 91 e 94 mcg/ml, respectivamente.
Após administração IV de 500 mg, os níveis plasmáticos de meropeném declinam até valores de 1 mcg/ml ou menos, 6 horas após a administração.
Quando múltiplas doses são administradas a indivíduos com função renal6 normal, em intervalos de 8 horas, não há ocorrência de acúmulo de meropeném.
Em indivíduos com função renal6 normal, a meia-vida de eliminação de meropeném é de aproximadamente 1 hora.
A ligação de meropeném às proteínas2 plasmáticas é de aproximadamente 2%.
Aproximadamente 70% da dose IV administrada é recuperada como meropeném inalterado na urina7 após 12 horas. Depois desse período uma pequena excreção urinária é detectável. As concentrações urinárias de meropeném em excesso de 10 mcg/ml são mantidas por até 5 horas com a dose de 500 mg. Não foi observado acúmulo de meropeném no plasma8 ou urina7 com regimes que utilizam 500 mg administrados a cada 8 horas ou 1 g administrado a cada 6 horas em voluntários com função renal6 normal.
O meropeném possui um metabólito9 microbiologicamente inativo.
O meropeném tem boa penetração na maioria dos tecidos e fluidos corporais, incluindo o líquido cérebro10-espinhal de pacientes com meningite11 bacteriana, alcançando concentrações acima das requeridas para inibir a maioria das bactérias.
Estudos em neonatos12 e crianças demonstraram que a farmacocinética de meropeném em crianças é similar àquela para adultos. A meia-vida de eliminação do meropeném esteve aumentada para aproximadamente 1,75 hora em crianças com idades entre 3 e 5 meses. As concentrações de meropeném aumentam com o aumento da dose na faixa de 10 a 40 mg/kg.
Estudos farmacocinéticos em pacientes com insuficiência renal13 demonstraram que a depuração plasmática de meropeném se correlaciona com a depuração de creatinina14. Em indivíduos com função renal6 alterada são necessários ajustes de dose.
Estudos farmacocinéticos em idosos demonstraram uma redução na depuração plasmática de meropeném, que se correlacionou com a redução na depuração de creatinina14 associada à idade.
Estudos farmacocinéticos em pacientes com doença hepática15 não demonstraram efeitos da mesma sobre a farmacocinética do meropeném.
Dados de segurança pré-clínica
Estudos em animais indicam que meropeném é bem tolerado pelos rins16. Evidência histológica17 de dano tubular renal6 foi observado em camundongos e em cães apenas em doses de 2000 mg/kg e em doses superiores.
O meropeném é geralmente bem tolerado pelo Sistema Nervoso Central18 (SNC19). Foram observados efeitos apenas com doses muito altas de 2000 mg/kg ou mais.
A LD50 IV de meropeném em roedores é superior a 2000 mg/kg. Em estudos de doses repetidas de até 6 meses de duração foram observados apenas efeitos secundários, incluindo
um pequeno decréscimo nos parâmetros dos glóbulos vermelhos e um aumento no peso do fígado20 em cães, com dose de 500 mg/kg.
Não houve evidência de potencial mutagênico nos 5 testes realizados e nenhuma evidência de toxicidade21 reprodutiva, incluindo potencial teratogênico22, em estudos nas doses mais altas possíveis em ratos e macacos (o nível de dose sem efeito de uma pequena redução no peso corpóreo F1 em rato foi 120 mg/kg).
Houve um aumento na evidência de abortos com 500 mg/kg em um estudo preliminar em macacos.
Não houve evidência de sensibilidade aumentada ao meropeném em animais jovens em comparação com animais adultos. A formulação intravenosa foi bem tolerada em estudos em animais. A formulação intramuscular causou necrose23 reversível no local da injeção4.
O único metabólito9 de meropeném teve um perfil similar de baixa toxicidade21 em estudos em animais.


