PRECAUÇÕES E ADVERTÊNCIAS AMATO
NOS PACIENTES COM OU SEM HISTÓRICO DE CRISES EPILÉPTICAS OU EPILEPSIA1, AS DROGAS ANTIEPILÉPTICAS INCLUINDO O TOPIRAMATO DEVEM SER GRADATIVAMENTE DESCONTINUADAS, PARA MINIMIZAR A POSSIBILIDADE DE CRISES EPILÉPTICAS OU AUMENTO DA FREQUÊNCIA DE CRISES EPILÉPTICAS.
EM ESTUDOS CLÍNICOS, AS DOSES DIÁRIAS FORAM DIMINUÍDAS DE 50-100 MG NOS ADULTOS COM EPILEPSIA1 E 25-50 MG EM ADULTOS RECEBENDO TOPIRAMATO EM INTERVALOS SEMANAIS A DOSES DE ATÉ 100 MG/DIA PARA A PROFILAXIA DA ENXAQUECA2. EM ESTUDOS CLÍNICOS EM CRIANÇAS, TOPIRAMATO FOI RETIRADO GRADUALMENTE POR UM PERÍODO DE 2-8 SEMANAS. NAS SITUAÇÕES ONDE A RETIRADA RÁPIDA DE TOPIRAMATO É DE RECOMENDAÇÃO MÉDICA, É RECOMENDADA MONITORAÇÃO APROPRIADA.
A PRINCIPAL VIA DE ELIMINAÇÃO DO TOPIRAMATO E SEUS METABÓLITOS3 É ATRAVÉS DOS RINS4. A ELIMINAÇÃO PELOS RINS4 É DEPENDENTE DA FUNÇÃO RENAL5 E INDEPENDE DA IDADE. PACIENTES COM INSUFICIÊNCIA RENAL6 MODERADA OU GRAVE PODEM LEVAR DE 10 A 15 DIAS PARA ATINGIR AS CONCENTRAÇÕES PLASMÁTICAS NO ESTADO DE EQUILÍBRIO, EM COMPARAÇÃO COM O PERÍODO DE 4 A 8 DIAS, OBSERVADO EM PACIENTES COM FUNÇÃO RENAL5 NORMAL.
EM TODOS OS PACIENTES, O TATEAMENTO DA DOSE DEVERÁ SER ORIENTADO PELO RESULTADO CLÍNICO (ISTO É, CONTROLE DAS CRISES, EVITANDO EFEITOS COLATERAIS7), CONSIDERANDO-SE QUE INDIVÍDUOS SABIDAMENTE PORTADORES DE INSUFICIÊNCIA RENAL6 PODERÃO PRECISAR DE UM TEMPO MAIS LONGO PARA ALCANÇAR O ESTADO DE EQUILÍBRIO, A CADA DOSE.
HIDRATAÇÃO ADEQUADA DURANTE O USO DE TOPIRAMATO É MUITO IMPORTANTE. HIDRATAÇÃO PODE REDUZIR O RISCO DE NEFROLITÍASE. HIDRATAÇÃO APROPRIADA ANTES E DURANTE ATIVIDADES COMO EXERCÍCIOS FÍSICOS OU EXPOSIÇÃO A TEMPERATURAS ELEVADAS PODE REDUZIR O RISCO DE EVENTOS ADVERSOS RELACIONADOS AO CALOR.
TRANSTORNOS DO HUMOR / DEPRESSÃO
UM AUMENTO NA INCIDÊNCIA8 DE TRANSTORNOS DO HUMOR E DEPRESSÃO TEM SIDO OBSERVADOS DURANTE O TRATAMENTO COM TOPIRAMATO.
TENTATIVA DE SUICÍDIO
NAS FASES DUPLO-CEGA DE ESTUDOS CLÍNICOS COM TOPIRAMATO EM INDICAÇÕES JÁ APROVADAS E EM ESTUDO, TENTATIVAS DE SUICÍDIO OCORRERAM NA TAXA DE 0,003 (13 EVENTOS/3999 PACIENTES ANO) COM USO DE TOPIRAMATO VERSUS (0 EVENTOS/1430 PACIENTES ANO) COM USO DE PLACEBO9. UM CASO DE SUICÍDIO DE PACIENTE EM USO DE TOPIRAMATO FOI RELATADO EM ESTUDO EM TRANSTORNO BIPOLAR.
NEFROLITÍASE
ALGUNS PACIENTES, ESPECIALMENTE AQUELES COM PREDISPOSIÇÃO À NEFROLITÍASE, PODEM TER RISCO AUMENTADO DE FORMAÇÃO DE CÁLCULO10 RENAL5 E SINAIS11 E SINTOMAS12 ASSOCIADOS, TAIS COMO CÓLICA RENAL5, DOR RENAL5 E DOR EM FLANCO13.
FATORES DE RISCO DE NEFROLITÍASE INCLUEM ANTECEDENTES DE CÁLCULO10 RENAL5, HISTÓRICO FAMILIAR DE NEFROLITÍASE E HIPERCALCIÚRIA14. NENHUM DESSES FATORES DE RISCO PODE ANTECIPAR COM CERTEZA A FORMAÇÃO DE CÁLCULO10 DURANTE TRATAMENTO COM TOPIRAMATO. ALÉM DISSO, PACIENTES UTILIZANDO OUTROS MEDICAMENTOS ASSOCIADOS À POSSIBILIDADE DE OCORRÊNCIA DE NEFROLITÍASE PODEM TER UM RISCO AUMENTADO.
FUNÇÃO HEPÁTICA15 DIMINUÍDA
TOPIRAMATO DEVE SER ADMINISTRADO COM CUIDADO EM PACIENTES COM INSUFICIÊNCIA HEPÁTICA16, UMA VEZ QUE O “CLEARANCE” DO TOPIRAMATO PODE ESTAR REDUZIDO NESTE GRUPO DE PACIENTES.
MIOPIA17 AGUDA E GLAU COMA18 AGUDO19 DE ÂNGULO FECHADO SECUNDÁRIO
UMA SÍNDROME20 CONSISTINDO DE MIOPIA17 AGUDA E GLAUCOMA21 AGUDO19 DE ÂNGULO FECHADO SECUNDÁRIO TEM SIDO RELATADA EM PACIENTES EM USO DE TOPIRAMATO. OS SINTOMAS12 INCLUEM INÍCIO AGUDO19 DE REDUÇÃO DA ACUIDADE VISUAL22 E/OU DOR OCULAR. ACHADOS OFTALMOLÓGICOS PODEM INCLUIR MIOPIA17, REDUÇÃO DA CÂMARA ANTERIOR23, HIPEREMIA24 OCULAR (VERMELHIDÃO) E AUMENTO DA PRESSÃO INTRAOCULAR25. MIDRÍASE26 PODE OU NÃO ESTAR PRESENTE. ESTA SÍNDROME20 PODE ESTAR ASSOCIADA COM EFUSÃO27 SUPRACILIAR RESULTANDO NO DESLOCAMENTO DO CRISTALINO28 E DA ÍRIS29, COM GLAUCOMA21 AGUDO19 DE ÂNGULO FECHADO SECUNDÁRIO.
OS SINTOMAS12 OCORREM, CARACTERISTICAMENTE, NO PRIMEIRO MÊS APÓS O INÍCIO DO TRATAMENTO COM TOPIRAMATO. AO CONTRÁRIO DO GLAUCOMA21 DE ÂNGULO FECHADO PRIMÁRIO, QUE É RARO EM PESSOAS COM MENOS DE 40 ANOS, O GLAUCOMA21 AGUDO19 DE ÂNGULO FECHADO SECUNDÁRIO ASSOCIADO COM TOPIRAMATO TEM SIDO RELATADO TANTO EM PACIENTES PEDIÁTRICOS COMO ADULTOS. O TRATAMENTO INCLUI A INTERRUPÇÃO DO TOPIRAMATO, O MAIS RÁPIDO POSSÍVEL DE ACORDO COM A AVALIAÇÃO DO MÉDICO, E MEDIDAS APROPRIADAS PARA REDUZIR A PRESSÃO INTRA-OCULAR. ESTAS MEDIDAS GERALMENTE RESULTAM NA REDUÇÃO DA PRESSÃO INTRA-OCULAR.
ACIDOSE METABÓLICA30
ACIDOSE METABÓLICA30, HIPERCLOREMIA, HIATO NÃO-ANIÔNICO (ISTO É, REDUÇÃO DO BICARBONATO SÉRICO ABAIXO DO INTERVALO DE REFERÊNCIA NORMAL NA AUSÊNCIA DE ALCALOSE31 RESPIRATÓRIA) ESTÃO ASSOCIADAS AO TRATAMENTO COM TOPIRAMATO. ESTA REDUÇÃO NO BICARBONATO SÉRICO ESTÁ RELACIONADA AO EFEITO INIBITÓRIO DO TOPIRAMATO NA ANIDRASE CARBÔNICA RENAL5. A REDUÇÃO NO BICARBONATO OCORRE GERALMENTE NO INÍCIO DO TRATAMENTO, MAS PODE OCORRER AO LONGO DA DURAÇÃO TRATAMENTO. ESTAS REDUÇÕES SÃO USUALMENTE LEVES A MODERADAS (REDUÇÃO MÉDIA DE 4 MMOL/L32 EM DOSES DE 100 MG/DIA OU ACIMA EM ADULTOS E APROXIMADAMENTE 6 MG/KG/DIA EM PACIENTES PEDIÁTRICOS). OS PACIENTES RARAMENTE APRESENTARAM REDUÇÃO À VALORES MENORES QUE 10 MMOL/L32. AS CONDIÇÕES OU TERAPIAS QUE PREDISPÕE A ACIDOSE33 (COMO DOENÇA RENAL5, DISTÚRBIOS RESPIRATÓRIOS GRAVES, “STATUS EPILEPTICUS”, DIARRÉIA34, CIRURGIA, DIETA CETOGÊNICA, OU ALGUNS FÁRMACOS) PODEM SER ADITIVOS AOS EFEITOS DO TOPIRAMATO NA REDUÇÃO DO BICARBONATO.
ACIDOSE METABÓLICA30 CRÔNICA EM PACIENTES PEDIÁTRICOS PODE REDUZIR AS TAXAS DE CRESCIMENTO. O EFEITO DO TOPIRAMATO NO CRESCIMENTO E SEQUELA35 RELATIVA AOS OSSOS NÃO FOI AVALIADO SISTEMATICAMENTE EM PACIENTES PEDIÁTRICOS OU ADULTOS.
DEPENDENDO DAS CONDIÇÕES DE BASE, RECOMENDA-SE AVALIAÇÃO ADEQUADA, INCLUINDO NÍVEIS DE BICARBONATO SÉRICO, DURANTE O TRATAMENTO COM TOPIRAMATO. SE ACIDOSE METABÓLICA30 OCORRER E PERSISTIR, DEVE-SE CONSIDERAR REDUÇÃO DA DOSE OU INTERRUPÇÃO DO TOPIRAMATO (USANDO REDUÇÃO GRADUAL DA DOSE).
SUPLEMENTAÇÃO36 NUTRICIONAL
A SUPLEMENTAÇÃO36 DA DIETA OU O AUMENTO DA INGESTÃO DE ALIMENTOS DEVE SER CONSIDERADO SE O PACIENTE APRESENTAR PERDA DE PESO DURANTE O TRATAMENTO COM TOPIRAMATO.
GRAVIDEZ37 E LACTAÇÃO38
USO DURANTE A GRAVIDEZ37
EM ESTUDOS PRÉ-CLÍNICOS, O TOPIRAMATO TEM DEMONSTRADO APRESENTAR EFEITOS TERATOGÊNICOS39 NAS ESPÉCIES ESTUDADAS (CAMUNDONGOS, RATOS E COELHOS). EM RATOS, O TOPIRAMATO ATRAVESSOU A BARREIRA PLACENTÁRIA. NÃO FORAM REALIZADOS ESTUDOS COM TOPIRAMATO EM GESTANTES. ENTRETANTO, TOPIRAMATO PODERÁ SER UTILIZADO DURANTE A GRAVIDEZ37 SOMENTE SE O BENEFÍCIO ESPERADO SUPERAR O RISCO POTENCIAL PARA O FETO40.
USO DURANTE A LACTAÇÃO38
O TOPIRAMATO É ELIMINADO NO LEITE DE RATAS. A EXCREÇÃO DO TOPIRAMATO NO LEITE HUMANO NÃO FOI AVALIADA EM ESTUDOS CONTROLADOS. A OBSERVAÇÃO EM UM NÚMERO LIMITADO DE PACIENTES SUGERE UMA EXCREÇÃO EXTENSA DO TOPIRAMATO NO LEITE. UMA VEZ QUE MUITAS DROGAS SÃO EXCRETADAS NO LEITE HUMANO, DEVESE DECIDIR ENTRE EVITAR A AMAMENTAÇÃO41 OU DESCONTINUAR O TRATAMENTO COM A DROGA, LEVANDO-SE EM CONSIDERAÇÃO A IMPORTÂNCIA DO MEDICAMENTO PARA A MÃE.
DURANTE A EXPERIÊNCIA PÓS-COMERCIALIZAÇÃO, CASOS DE HIPOSPADIA42 FORAM RELATADOS EM BEBÊS43 DO SEXO MASCULINO EXPOSTOS AO TOPIRAMATO NO ÚTERO44, COM OU SEM OUTROS ANTICONVULSIVANTES; NO ENTANTO, UMA RELAÇÃO CAUSAL COM O TOPIRAMATO NÃO FOI ESTABELECIDA.
EFEITOS SOBRE A CAPACIDADE DE DIRIGIR VEÍCULOS E OPERAR MÁQUINAS
TOPIRAMATO AGE SOBRE O SISTEMA NERVOSO CENTRAL45, PODENDO PRODUZIR SONOLÊNCIA, TONTURA46 OU OUTROS SINTOMAS12 RELACIONADOS. EMBORA TAIS REAÇÕES SEJAM DE INTENSIDADE LEVE OU MODERADA, PODEM SER POTENCIALMENTE PERIGOSAS PARA PACIENTES47 DIRIGINDO VEÍCULOS OU OPERANDO MÁQUINAS, PARTICULARMENTE ATÉ QUE SE CONHEÇA A REAÇÃO INDIVIDUAL DO PACIENTE AO FÁRMACO48.
- INTERAÇÕES MEDICAMENTOSAS
EFEITOS DO TOPIRAMATO SOBRE OUTRAS DROGAS ANTIEPILÉPTICAS
A ASSOCIAÇÃO DE TOPIRAMATO A OUTRAS DROGAS ANTIEPILÉPTICAS (FENITOÍNA, CARBAMAZEPINA, ÁCIDO VALPRÓICO, FENOBARBITAL, PRIMIDONA) NÃO AFETA SUAS CONCENTRAÇÕES PLASMÁTICAS NO ESTADO DE EQUILÍBRIO, EXCETO, OCASIONALMENTE, EM ALGUNS PACIENTES, EM QUE A ADIÇÃO DE TOPIRAMATO À FENITOÍNA PODERÁ RESULTAR EM AUMENTO DAS CONCENTRAÇÕES PLASMÁTICAS DE FENITOÍNA. ISTO SE DEVE POSSIVELMENTE À INIBIÇÃO DE UMA ISOFORMA ESPECÍFICA DE UMA ENZIMA49 POLIMÓRFICA (CYP2C19). CONSEQUENTEMENTE, DEVERÁ SER REALIZADA DOSAGEM DO NÍVEL PLASMÁTICO DE FENITOÍNA EM QUALQUER PACIENTE EM TRATAMENTO COM FENITOÍNA QUE APRESENTE SINAIS11 OU SINTOMAS12 DE TOXICIDADE50. UM ESTUDO DE INTERAÇÃO FARMACOCINÉTICA EM PACIENTES COM EPILEPSIA1 DEMONSTROU QUE A ASSOCIAÇÃO DO TOPIRAMATO À LAMOTRIGINA NÃO APRESENTOU EFEITO NA CONCENTRAÇÃO PLASMÁTICA DE LAMOTRIGINA NO ESTADO ESTACIONÁRIO COM DOSES DE TOPIRAMATO DE 100 A 400 MG/DIA. ALÉM DISSO, A CONCENTRAÇÃO PLASMÁTICA DE TOPIRAMATO NO ESTADO ESTACIONÁRIO NÃO SOFREU ALTERAÇÃO DURANTE OU APÓS A RETIRADA DO TRATAMENTO COM LAMOTRIGINA (DOSE MÉDIA DE 327 MG/DIA).
EFEITOS DE OUTRAS DROGAS ANTIEPILÉPTICAS SOBRE TOPIRAMATO
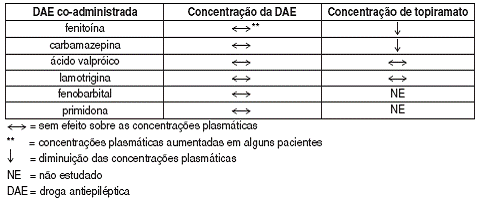
A FENITOÍNA E A CARBAMAZEPINA DIMINUEM AS CONCENTRAÇÕES PLASMÁTICAS DO TOPIRAMATO A ADIÇÃO OU DESCONTINUAÇÃO DA FENITOÍNA OU DA CARBAMAZEPINA AO TRATAMENTO COM TOPIRAMATO PODERÁ REQUERER UM AJUSTE DE DOSE DESTE ÚLTIMO. O TATEAMENTO DA DOSE DEVERÁ SER REALIZADO DE ACORDO COM O EFEITO CLÍNICO.
TANTO A ADIÇÃO QUANTO A RETIRADA DO ÁCIDO VALPRÓICO NÃO PRODUZEM MUDANÇAS CLINICAMENTE SIGNIFICATIVAS NAS CONCENTRAÇÕES PLASMÁTICAS DE TOPIRAMATO E, PORTANTO, NÃO EXIGEM AJUSTE DA DOSE DO TOPIRAMATO. OS RESULTADOS DESTAS INTERAÇÕES ESTÃO RESUMIDOS NA TABELA A SEGUIR:
- OUTRAS INTERAÇÕES MEDICAMENTOSAS
DIGOXINA: EM UM ESTUDO DE DOSE ÚNICA, A ADMINISTRAÇÃO CONCOMITANTE DE TOPIRAMATO PROVOCOU UMA REDUÇÃO DE 12% NA ÁREA SOB A CURVA DE CONCENTRAÇÃO PLASMÁTICA (AUC51) DA DIGOXINA. A IMPORTÂNCIA CLÍNICA DESTA OBSERVAÇÃO NÃO FOI DETERMINADA. QUANDO O TOPIRAMATO FOR ASSOCIADO OU DESCONTINUADO EM PACIENTES SUBMETIDOS A TRATAMENTO COM A DIGOXINA, RECOMENDA-SE ATENÇÃO À MONITORAÇÃO ROTINEIRA E CUIDADOSA DAS CONCENTRAÇÕES SÉRICAS DE DIGOXINA.
DEPRESSORES DO SNC52/ÁLCOOL: RECOMENDA-SE QUE TOPIRAMATO NÃO SEJA UTILIZADO CONCOMITANTEMENTE COM BEBIDAS ALCOÓLICAS OU COM OUTROS MEDICAMENTOS DEPRESSORES DO SNC52, POIS PODE OCORRER UM AUMENTO DA AÇÃO DE TOPIRAMATO.
ANTICONCEPCIONAIS ORAIS: EM UM ESTUDO DE INTERAÇÃO FARMACOCINÉTICA EM VOLUNTÁRIAS SADIAS, COM ADMINISTRAÇÃO CONCOMITANTE DE CONTRACEPTIVO ORAL COMBINADO CONTENDO 1 MG DE NORETINDRONA E 35 MCG DE ETINILESTRADIOL, TOPIRAMATO ADMINISTRADO ISOLADAMENTE NAS DOSES DE 50 A 200 MG/DIA, NÃO FOI ASSOCIADO A ALTERAÇÕES ESTATISTICAMENTE SIGNIFICANTES NA EXPOSIÇÃO MÉDIA (AUC51) AOS COMPONENTES DO CONTRACEPTIVO ORAL. EM OUTRO ESTUDO, A EXPOSIÇÃO AO ETINILESTRADIOL APRESENTOU REDUÇÃO ESTATISTICAMENTE SIGNIFICANTE COM DOSES DE 200, 400 E 800 MG/DIA (18%, 21% E 30% RESPECTIVAMENTE) QUANDO ADMINISTRADO COMO ADJUVANTE EM PACIENTES EM USO DE ÁCIDO VALPRÓICO. EM AMBOS OS ESTUDOS, TOPIRAMATO (50 MG/DIA A 800 MG/DIA) NÃO AFETOU SIGNIFICANTEMENTE A EXPOSIÇÃO À NORETINDRONA. ENTRETANTO, NAS DOSES ENTRE 200-800 MG/DIA, HOUVE UMA REDUÇÃO DOSE-DEPENDENTE NA EXPOSIÇÃO AO ETINILESTRADIOL E, NAS DOSES DE 50-200 MG/DIA, NÃO HOUVE ALTERAÇÃO SIGNIFICANTE DOSE DEPENDENTE NA EXPOSIÇÃO AO ETINILESTRADIOL.
A SIGNIFICÂNCIA CLÍNICA DAS ALTERAÇÕES OBSERVADAS NÃO É CONHECIDA. A POSSIBILIDADE DE REDUÇÃO DA EFICÁCIA DO CONTRACEPTIVO E AUMENTO NO SANGRAMENTO DE ESCAPE DEVE SER CONSIDERADA EM PACIENTES EM USO DE CONTRACEPTIVOS ORAIS COMBINADOS E TOPIRAMATO. DEVE-SE SOLICITAR A PACIENTES EM USO DE CONTRACEPTIVOS ORAIS QUE RELATEM QUALQUER ALTERAÇÃO EM SEUS PADRÕES MENSTRUAIS. A EFICÁCIA CONTRACEPTIVA PODE SER REDUZIDA, MESMO NA AUSÊNCIA DE SANGRAMENTO DE ESCAPE.
LÍTIO : EM VOLUNTÁRIOS SAUDÁVEIS, FOI OBSERVADA UMA REDUÇÃO (18% PARA AUC51) NA EXPOSIÇÃO SISTEMÁTICA PARA O LÍTIO DURANTE A ADMINISTRAÇÃO CONCOMITANTE COM TOPIRAMATO 200 MG/DIA. NOS PACIENTES COM TRANSTORNO BIPOLAR, A FARMACOCINÉTICA DO LÍTIO NÃO FOI AFETADA DURANTE O TRATAMENTO COM TOPIRAMATO EM DOSES DE 200 MG/DIA; ENTRETANTO, FOI OBSERVADO AUMENTO NA EXPOSIÇÃO SISTÊMICA (26% PARA AUC51) DEPOIS DE DOSES DO TOPIRAMATO DE ATÉ 600 MG/DIA. OS NÍVEIS DO LÍTIO DEVEM SER MONITORADOS QUANDO CO-ADMINISTRADOS COM TOPIRAMATO.
RISPERIDONA: OS ESTUDOS DE INTERAÇÃO DROGA-DROGA CONDUZIDOS SOB CONDIÇÕES DE DOSE ÚNICA E MÚLTIPLA EM VOLUNTÁRIOS SAUDÁVEIS E EM PACIENTES COM TRANSTORNO BIPOLAR ATINGIRAM RESULTADOS SIMILARES. QUANDO ADMINISTRADO CONCOMITANTEMENTE COM TOPIRAMATO EM DOSES ESCALADAS DE 100, 250 E 400 MG/DIA HOUVE UMA REDUÇÃO DA RISPERIDONA (ADMINISTRADA EM DOSES QUE VARIANDO DE 1 A 6 MG/DIA) NA EXPOSIÇÃO SISTÊMICA (16% E 33% PARA AUC51 NO ESTADO DE EQUILÍBRIO NAS 250 E 400 DOSES DE MG/DIA, RESPECTIVAMENTE). ALTERAÇÕES MÍNIMAS NA FARMACOCINÉTICA DO TOTAL DE PARTES ATIVAS (RISPERIDONA MAIS 9-HIDROXIRISPERIDONA) E NENHUMA ALTERAÇÃO PARA 9-HIDROXIRISPERIDONA FOI OBSERVADA. NÃO HOUVE MUDANÇA CLÍNICA SIGNIFICATIVAMENTE NA EXPOSIÇÃO SISTEMICA DO TOTAL DE PARTES ATIVAS DA RISPERIDONA OU DO TOPIRAMATO, PORTANTO ESTA INTERAÇÃO NÃO É PROVÁVEL SER DE SIGNIFICÂNCIA CLÍNICA.
HIDROCLOROTIA ZIDA: UM ESTUDO DE INTERAÇÃO MEDICAMENTOSA CONDUZIDO EM VOLUNTÁRIOS SADIOS AVALIOU A FARMACOCINÉTICA NO ESTADO ESTACIONÁRIO DA HIDROCLOROTIAZIDA (25 MG A CADA 24H) E DO TOPIRAMATO (96 MG A CADA 12H) QUANDO ADMINISTRADOS ISOLADA OU CONCOMITANTEMENTE. OS RESULTADOS DESTE ESTUDO INDICARAM QUE A Cmáx DO TOPIRAMATO AUMENTOU 27% E A AUC51 AUMENTOU 29% QUANDO A HIDROCLOROTIAZIDA FOI ASSOCIADA AO TOPIRAMATO. A SIGNIFICÂNCIA CLÍNICA DESTA ALTERAÇÃO É DESCONHECIDA. A ASSOCIAÇÃO DE HIDROCLOROTIAZIDA AO TRATAMENTO COM TOPIRAMATO PODE PRECISAR DE UM AJUSTE DA DOSE DO TOPIRAMATO. A FARMACOCINÉTICA DA HIDROCLOROTIAZIDA NO ESTADO ESTACIONÁRIO NÃO FOI INFLUENCIADA SIGNIFICATIVAMENTE PELA ADMINISTRAÇÃO CONCOMITANTE DO TOPIRAMATO. OS RESULTADOS LABORATORIAIS CLÍNICOS INDICARAM REDUÇÃO NO POTÁSSIO SÉRICO APÓS ADMINISTRAÇÃO DO TOPIRAMATO OU DA HIDROCLOROTIAZIDA, SENDO MAIOR QUANDO A HIDROCLOROTIAZIDA E O TOPIRAMATO FORAM ADMINISTRADOS EM COMBINAÇÃO.
METFORMINA53: UM ESTUDO DE INTERAÇÃO MEDICAMENTOSA CONDUZIDO EM VOLUNTÁRIOS SADIOS AVALIOU A FARMACOCINÉTICA DA METFORMINA53 E DO TOPIRAMATO NO ESTADO DE EQUILÍBRIO NO PLASMA54 QUANDO A METFORMINA53 FOI ADMINISTRADA ISOLADA E QUANDO A METFORMINA53 E O TOPIRAMATO FORAM ADMINISTRADOS SIMULTANEAMENTE. OS RESULTADOS DO ESTUDO INDICARAM QUE A Cmáx MÉDIA E A AUC0-12 h MÉDIA DA METFORMINA53 AUMENTARAM EM 18% E 25%, RESPECTIVAMENTE, ENQUANTO QUE O “CLEARANCE” MÉDIO DIMINUIU 20% QUANDO
A METFORMINA53 FOI CO-ADMINISTRADA COM TOPIRAMATO. O TOPIRAMATO NÃO AFETA O Tmáx DA METFORMINA53. A SIGNIFICÂNCIA CLÍNICA DO EFEITO DO TOPIRAMATO NA FARMACOCINÉTICA DA METFORMINA53 NÃO ESTÁ CLARA. O “CLEARANCE” PLASMÁTICO ORAL DO TOPIRAMATO PARECE SER REDUZIDO QUANDO ADMINISTRADO COM METFORMINA53. A EXTENSÃO DA ALTERAÇÃO NO “CLEARANCE” É DESCONHECIDA. A SIGNIFICÂNCIA CLÍNICA DO EFEITO DA METFORMINA53 NA FARMACOCINÉTICA DO TOPIRAMATO NÃO ESTÁ CLARA. QUANDO TOPIRAMATO É ADMINISTRADO OU RETIRADO EM PACIENTES TRATADOS COM METFORMINA53, DEVE-SE TER ESPECIAL ATENÇÃO NA MONITORIZAÇÃO ROTINEIRA PARA UM CONTROLE ADEQUADO DO DIABETES55.
PIOGLITAZONA: UM ESTUDO DE INTERAÇÃO MEDICAMENTOSA CONDUZIDO EM VOLUNTÁRIOS SADIOS AVALIOU A FARMACOCINÉTICA NO ESTADO ESTACIONÁRIO DO TOPIRAMATO E DA PIOGLITAZONA QUANDO ADMINISTRADOS ISOLADA OU CONCOMITANTEMENTE. UMA REDUÇÃO DE 15% NA AUCt, SS DE PIOGLITAZONA SEM ALTERAÇÃO NA Cmáx, SS FOI OBSERVADA. ESTE ACHADO NÃO FOI ESTATISTICAMENTE SIGNIFICANTE. ALÉM DISSO, REDUÇÕES DE 13% NA Cmáx , SS E DE 16% NA AUCt, SS DO HIDRÓXIMETABÓLITO ATIVO FORAM OBSERVADAS, ASSIM COMO UMA REDUÇÃO DE 60% TANTO NA Cmáx , SS COMO NA AUCt, SS DO CETO-METABÓLITO56 ATIVO FORAM OBSERVADAS. A SIGNIFICÂNCIA CLÍNICA DESTES ACHADOS É DESCONHECIDA. QUANDO TOPIRAMATO É ASSOCIADO AO TRATAMENTO COM PIOGLITAZONA OU PIOGLITAZONA É ASSOCIADA AO TRATAMENTO COM TOPIRAMATO, DEVE-SE TER ATENÇÃO ESPECIAL À ROTINA DE MONITORAMENTO DOS PACIENTES PARA UM CONTROLE ADEQUADO DO ESTADO DIABÉTICO.
GLIBURIDA: UM ESTUDO DE INTERAÇÃO DROGA-DROGA CONDUZIDOS NOS PACIENTES COM DIABETES TIPO 257 AVALIOU A FARMACOCINÉTICA NO ESTADO DE EQUILÍBRIO DA GLIBURIDA (5MG/DIA) ISOLADA E CONCOMITANTEMENTE COM TOPIRAMATO (150 MG/DIA). HOUVE UMA REDUÇÃO DE 25% NA AUC24 DA GLIBURIDA DURANTE A ADMINISTRAÇÃO DO TOPIRAMATO. A EXPOSIÇÃO SISTEMICA DOS METABOLITOS3 ATIVOS, 4-TRANS-HIDROXI-GLIBURIDA (M1) E 3-CISHIDROXIGLIBURIDA (M2), TAMBÉM FORAM REDUZIDAS EM 13% E 15%, RESPECTIVAMENTE. A FARMACOCINÉTICA NO ESTADO DE EQUILÍBRIO DO TOPIRAMATO NÃO FOI AFETADA PELA ADMINISTRAÇÃO CONCOMITANTE DA GLIBURIDA. QUANDO O TOPIRAMATO É ADICIONADO A TERAPIA DA GLIBURIDA OU A GLIBURIDA É ADICIONADA A TERAPIA DO
TOPIRAMATO, DEVE SER FEITA UMA ROTINA DE MONITORIZAÇÃO CUIDADOSA DOS PACIENTES PARA O CONTROLE ADEQUADO DO ESTADO DA SUA DOENÇA DIABÉTICA.
OUTRAS FORMAS DE INTERAÇÃO:
AGENTES QUE PREDISPÕEM À NEFROLITÍASE
TOPIRAMATO PODE AUMENTAR O RISCO DE NEFROLITÍASE EM PACIENTES EM USO CONCOMITANTE DE OUTROS AGENTES QUE PREDISPÕEM À NEFROLITÍASE. DURANTE TRATAMENTO COM TOPIRAMATO, TAIS AGENTES DEVERÃO SER EVITADOS, UMA VEZ QUE ELES CRIAM UM AMBIENTE FISIOLÓGICO58 QUE AUMENTA O RISCO DE FORMAÇÃO
DE CÁLCULO10 RENAL5.
ÁCIDO VALPRÓICO
A ADMINISTRAÇÃO CONCOMITANTE DO TOPIRAMATO E DO ÁCIDO VALPRÓICO FOI ASSOCIADA COM HIPERAMONEMIA COM OU SEM ENCEFALOPATIA59 NOS PACIENTES QUE TOLERARAM UMA OU OUTRA DROGA ISOLADA. NA MAIORIA DE CASOS, OS SINTOMAS12 E OS SINAIS11 CESSARAM COM A DESCONTINUAÇÃO DE UMA OU OUTRA DROGA. ESTE EVENTO ADVERSO NÃO É DEVIDO A UMA INTERAÇÃO FARMACOCINÉTICA. UMA ASSOCIAÇÃO DE HIPERAMONEMIA COM MONOTERAPIA DO TOPIRAMATO OU DO TRATAMENTO CONCOMITANTE COM OUTROS ANTIEPILÉPTICOS NÃO FOI ESTABELECIDA.
ESTUDOS ADICIONAIS DE INTERAÇÃO MEDICAMENTOSA FARMACOCINÉTICA:
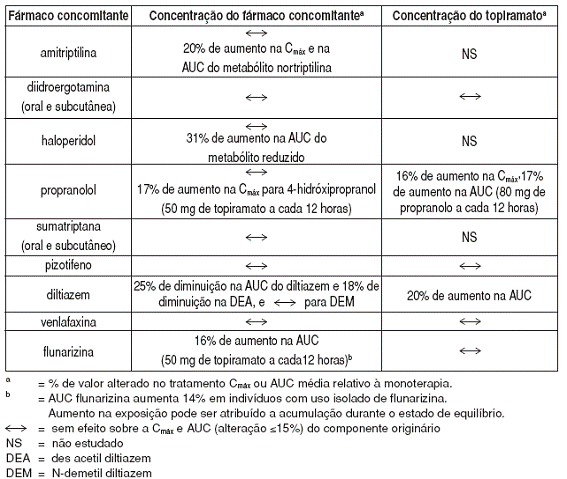
ESTUDOS CLÍNICOS FORAM CONDUZIDOS PARA AVALIAR A INTERAÇÃO MEDICAMENTOSA FARMACOCINÉTICA POTENCIAL ENTRE O TOPIRAMATO E OUTROS AGENTES. AS ALTERAÇÕES NA Cmáx E NA AUC51 COMO RESULTADO DAS INTERAÇÕES ESTÃO DESCRITAS A SEGUIR. A SEGUNDA COLUNA (CONCENTRAÇÃO DO FÁRMACO48 CONCOMITANTE) DESCREVE O QUE ACONTECE COM A CONCENTRAÇÃO DO FÁRMACO48 CONCOMITANTE LISTADO NA PRIMEIRA COLUNA QUANDO TOPIRAMATO É ASSOCIADO. A TERCEIRA COLUNA (CONCENTRAÇÃO DO TOPIRAMATO) MENCIONA COMO A CO-ADMINISTRAÇÃO DO FÁRMACO48 LISTADO NA PRIMEIRA COLUNA MODIFICA A CONCENTRAÇÃO DO TOPIRAMATO.
RESUMO DOS RESULTADOS DOS ESTUDOS ADICIONAIS DE INTERAÇÃO MEDICAMENTOSA FARMACOCINÉTICA