REAÇÕES ADVERSAS CLORIDRATO DE VENLAFAXINA
As informações incluídas no sub-item “Achados adversos observados em estudos controlados por placebo1 e de curto prazo com cloridrato de venlafaxina cápsulas de liberação prolongada” baseiam-se nos dados de um pool de três estudos clínicos controlados de 8 e 12 semanas de duração em transtorno depressivo maior (inclui dois estudos nos EUA e um na Europa), nos dados de até 8 semanas do pool de 5 estudos clínicos controlados em Transtorno de Ansiedade Generalizada (TAG) com este medicamento e nos dados de até 12 semanas de um pool de dois estudos clínicos controlados em Fobia2 Social e nos dados de até 12 semanas de um pool de quatro estudos clínicos controlados em Transtorno do Pânico.
As informações sobre outros eventos adversos associados a este medicamento no programa de desenvolvimento completo da formulação e ao cloridrato de venlafaxina comprimidos (formulação de liberação imediata) estão incluídas no sub-item “Outros eventos adversos observados durante a avaliação précomercialização de cloridrato de venlafaxina comprimidos e cloridrato de venlafaxina cápsulas de liberação prolongada”.
• Achados adversos observados em estudos controlados por placebo1 e de curto prazo com cloridrato de venlafaxina cápsulas de liberação prolongada
Eventos Adversos Associados à Descontinuação do Tratamento: aproximadamente 11% dos 357 pacientes que receberam as cápsulas de liberação prolongada de cloridrato de venlafaxina nos estudos clínicos controlados por placebo1 em transtorno depressivo maior descontinuaram o tratamento devido a uma experiência adversa em comparação a 6% dos 285 pacientes tratados com placebo1 nesses estudos.
Aproximadamente 18% dos 1.381 pacientes que receberam cloridrato de venlafaxina cápsulas nos estudos clínicos controlados por placebo1 em Transtorno de Ansiedade Generalizada descontinuaram o tratamento devido a uma experiência adversa em comparação a 12% dos 555 pacientes tratados com placebo1 nesses estudos. Aproximadamente 17% dos 277 pacientes que receberam cloridrato de venlafaxina cápsulas de liberação prolongada nos estudos clínicos controlados por placebo1 em Fobia2 Social descontinuaram o tratamento devido a uma experiência adversa em comparação a 5% dos 274 pacientes tratados com placebo1 nesses estudos. Aproximadamente 7% dos 1.001 pacientes que receberam as cápsulas de cloridrato de venlafaxina nos estudos clínicos controlados por placebo1 em Transtorno do Pânico descontinuaram o tratamento devido a uma experiência adversa em comparação a 6% dos 662 pacientes tratados com placebo1 nesses estudos. Os eventos mais comuns que resultaram na descontinuação do tratamento e que foram considerados relacionados ao medicamento (ou seja, que resultaram na descontinuação do tratamento em no mínimo 1% dos pacientes tratados com este medicamento numa taxa no mínimo duas vezes maior que a do placebo1 em qualquer das indicações) são apresentados na Tabela 1.
TABELA 1 - Eventos adversos comuns que resultaram na descontinuação do tratamento nos estudos controlados por placebo1 (1)
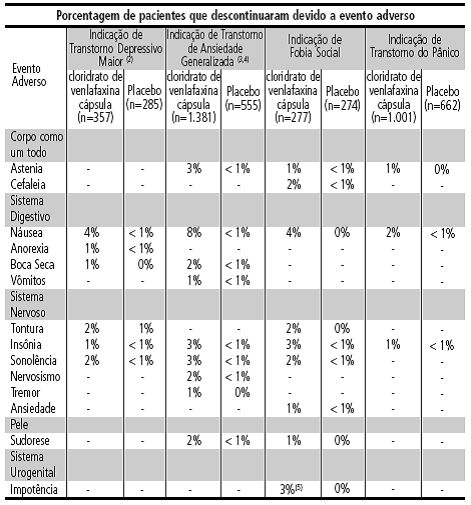
(1) Dois estudos em transtorno depressivo maior foram de dose flexível e um foi de dose fixa. Quatro estudos em Transtorno de Ansiedade Generalizada foram de dose fixa e um foi de dose flexível. Os dois estudos em Fobia2 Social foram de dose flexível. Dois estudos em Transtorno no Pânico foram de dose flexível e dois foram de dose fixa. (2) Nos estudos controlados por placebo1 de transtorno depressivo maior nos EUA, os seguintes eventos também foram eventos comuns que resultaram na descontinuação do tratamento e foram considerados relacionados ao medicamento nos pacientes tratados com cloridrato de venlafaxina cápsulas de liberação prolongada (% cloridrato de venlafaxina [n=192], % Placebo1 [n=202]): hipertensão3 (1%, < 1%); diarreia4 (1%, 0%); parestesia5 (1%, 0%); tremor (1%, 0%); visão6 anormal, principalmente visão6 turva (1%, 0%) e ejaculação7 anormal, principalmente retardada (1%, 0%). (3) Em dois estudos controlados por placebo1 e a curto prazo de Transtorno de Ansiedade Generalizada nos EUA, os seguintes eventos também foram eventos comuns que resultaram na descontinuação do tratamento e foram considerados relacionados ao medicamento nos pacientes tratados com cloridrato de venlafaxina cápsulas de liberação prolongada (% cloridrato de venlafaxina [n=476], % Placebo1 [n=201]): cefaleia8 (4%, <1%); vasodilatação (1%, 0%); anorexia9 (2%, < 1%); tontura10 (4%, 1%); pensamento anormal (1%, 0%) e visão6 anormal (1%, 0%). (4) Nos estudos controlados por placebo1 e a longo prazo de Transtorno de Ansiedade Generalizada, o seguinte evento também foi um evento comum que resultou na descontinuação do tratamento e foi considerado relacionado ao medicamento nos pacientes tratados com este medicamento (% cloridrato de venlafaxina [n=535], % Placebo1 [n=257]): diminuição da libido11 (1%, 0%). (5) A incidência12 baseia-se no número de homens (cloridrato de venlafaxina = 158, placebo1 = 153).
Eventos Adversos Ocorridos com Incidência12 de no Mínimo 2% Entre os Pacientes Tratados com cloridrato de venlafaxina cápsula de liberação prolongada: as Tabelas 2, 3, 4 e 5 enumeram a incidência12, arredondada para a porcentagem mais próxima, de eventos adversos decorrentes do tratamento ocorridos durante a terapia aguda de transtorno depressivo maior (até 12 semanas; intervalo de dose de 75 a 225 mg/dia),
Transtorno de Ansiedade Generalizada (até 8 semanas; intervalo de dose de 37,5 a 225 mg/dia), Fobia2 Social (até 12 semanas; intervalo de dose de 75 a 225 mg/dia) e Transtorno do Pânico (até 12 semanas; intervalo de dose de 37,5 a 225 mg/dia), respectivamente, em no mínimo 2% dos pacientes tratados com cloridrato de venlafaxina, em que a incidência12 em pacientes tratados com cloridrato de venlafaxina foi maior que a incidência12 nos respectivos pacientes tratados com placebo1. A Tabela mostra a porcentagem de pacientes em cada grupo que apresentou, pelo menos, um episódio de evento em algum momento durante o tratamento. Os eventos adversos relatados foram classificados utilizando a terminologia padrão com base no Dicionário COSTART. O médico prescritor deve estar ciente de que esses números não podem ser usados para prever a incidência12 de efeitos colaterais13 na prática clínica usual, em que as características do paciente e os outros fatores diferem dos que prevaleceram nos estudos clínicos. Da mesma forma, as frequências mencionadas não podem ser comparadas aos números obtidos em outras investigações clínicas envolvendo tratamentos, usos e investigadores diferentes. Os números citados, contudo, realmente fornecem ao médico prescritor algum fundamento para estimar a contribuição relativa dos fatores medicamentosos e não-medicamentosos para a taxa de incidência12 de efeitos colaterais13 na população estudada.
Eventos Adversos Frequentemente Observados das Tabelas 2, 3, 4 e 5:
Transtorno Depressivo Maior - observar em particular os seguintes eventos adversos ocorridos em, no mínimo, 5% dos pacientes tratados com cloridrato de venlafaxina e numa taxa no mínimo duas vezes maior que a do grupo placebo1 em todos os estudos controlados por placebo1 em transtorno depressivo maior (Tabela 2): ejaculação7 anormal, queixas gastrintestinais (náusea14, boca15 seca e anorexia9), queixas do SNC16 (tontura10, sonolência e sonhos anormais) e sudorese17. Nos dois estudos controlados por placebo1 nos EUA, os seguintes eventos adicionais ocorreram em, no mínimo, 5% dos pacientes tratados com cloridrato de venlafaxina (n=192) e numa taxa no mínimo duas vezes maior que a do grupo placebo1: anormalidades da função sexual (impotência18 em homens, anorgasmia19 em mulheres e diminuição da libido11), queixas gastrintestinais (constipação20 e flatulência), queixas do SNC16 (insônia, nervosismo e tremor), problemas nos sentidos (visão6 anormal), efeitos cardiovasculares (hipertensão3 e vasodilatação) e bocejos.
Transtornos de Ansiedade Generalizada - observar em particular os seguintes eventos adversos ocorridos em, no mínimo, 5% dos pacientes tratados com cloridrato de venlafaxina e, numa taxa no mínimo duas vezes maior que a do grupo placebo1 em todos os estudos controlados por placebo1 na indicação de Transtorno de Ansiedade Generalizada (Tabela 3): anormalidades da função sexual (ejaculação7 anormal e impotência18), queixas gastrintestinais (náusea14, boca15 seca, anorexia9 e constipação20), problemas dos sentidos (visão6 anormal) e sudorese17.
Fobia2 Social - observar em particular os seguintes eventos adversos ocorridos em, no mínimo, 5% dos pacientes tratados com cloridrato de venlafaxina e numa taxa no mínimo duas vezes maior que a do grupo placebo1 nos 2 estudos controlados por placebo1 na indicação de Fobia2 Social (Tabela 4): astenia21, queixas gastrintestinais (anorexia9, boca15 seca, náusea14), queixas do SNC16 (ansiedade, insônia, diminuição da libido11, nervosismo, sonolência, tontura10), anormalidades da função sexual (ejaculação7 anormal, disfunção orgásmica, impotência18), bocejos, sudorese17 e visão6 anormal.
Transtorno do Pânico - observar em particular os seguintes eventos adversos ocorridos em no mínimo 5% dos pacientes tratados com cloridrato de venlafaxina cápsula de liberação prolongada e numa taxa de pelo menos duas vezes maior que a do grupo placebo1 nos 4 estudos controlados por placebo1 na indicação de Transtorno do Pânico (Tabela 5): queixas gastrintestinais (anorexia9, constipação20, boca15 seca), queixas do SNC16 (sonolência, tremores), anormalidade da função sexual (ejaculação7 anormal) e sudorese17.
TABELA 2 - Incidência12 de Eventos Adversos Decorrentes do Tratamento nos Estudos Clínicos Controlados por Placebo1 e a Curto Prazo de cloridrato de venlafaxina cápsulas em Pacientes com Transtorno Depressivo Maior (1,2)
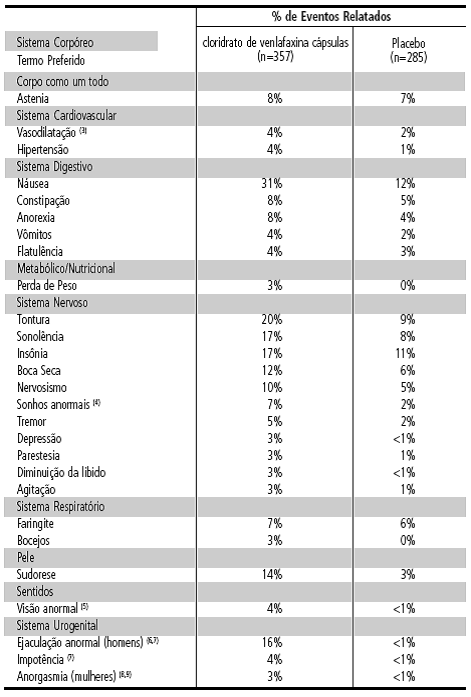
(1) Incidência12, arredondada para a % mais próxima, de eventos relatados por, no mínimo, 2% dos pacientes tratados com cloridrato de venlafaxina cápsulas, com exceção dos seguintes eventos que apresentaram uma incidência12 menor ou igual que a do placebo1: dor abdominal, dano acidental, ansiedade, dor nas costas22, bronquite, diarreia4, dismenorreia23, dispepsia24, síndrome25 da gripe26, cefaleia8, infecção27, dor, palpitação28, rinite29 e sinusite30.
(2) < 1% indica incidência12 maior que zero, mas menor que 1%.
(3) Principalmente “fogachos”.
(4) Principalmente “sonhos vívidos”, “pesadelos” e “aumento de sonhos”.
(5) Principalmente “visão turva” e “dificuldade de focalização”.
(6) Principalmente “ejaculação retardada”.
(7) A incidência12 baseia-se no número de homens.
(8) Principalmente “orgasmo retardado” ou “anorgasmia”.
(9) A incidência12 baseia-se no número de mulheres.
TABELA 3 – Incidência12 de Eventos Adversos Decorrentes do Tratamento em Estudos Clínicos Controlados por Placebo1 e a Curto Prazo de cloridrato de venlafaxina cápsulas em Pacientes com Transtorno de Ansiedade Generalizada (1,2)
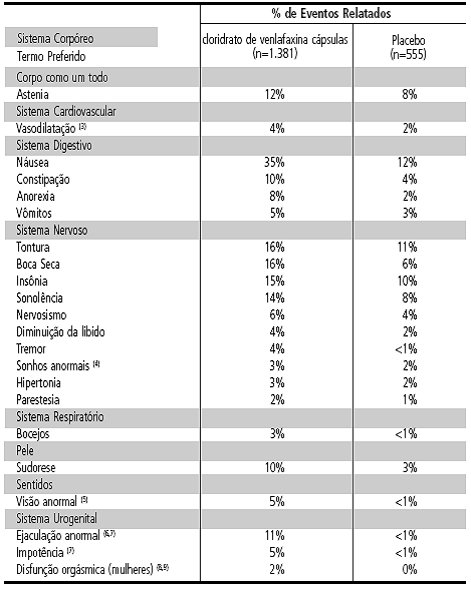
(1) Os eventos adversos cuja taxa de relato para cloridrato de venlafaxina cápsulas foi menor ou igual à do placebo1 não foram incluídos. Esses eventos são: dor abdominal, dano acidental, ansiedade, dor nas costas22, diarreia4, dismenorreia23, dispepsia24, síndrome25 da gripe26, cefaleia8, infecção27, mialgia31, dor, palpitação28, faringite32, rinite29, tinido e frequência urinária.
(2) < 1% significa maior que zero, mas menor que 1%.
(3) Principalmente “fogachos".
(4) Principalmente “sonhos vívidos”, “pesadelos” e “aumento de sonhos”.
(5) Principalmente “visão turva” e “dificuldade de focalização”.
(6) Inclui “ejaculação retardada” e “anorgasmia”.
(7) A porcentagem baseia-se no número de homens (cloridrato de venlafaxina = 525, placebo1 = 220).
(8) Inclui “orgasmo retardado”, “orgasmo anormal” e “anorgasmia”.
(9) A porcentagem baseia-se no número de mulheres (cloridrato de venlafaxina = 856, placebo1 = 335)
TABELA 4 – Incidência12 de Eventos Adversos Decorrentes do Tratamento nos Estudos Clínicos Controlados por Placebo1 e a Curto Prazo de cloridrato de venlafaxina cápsulas em Pacientes com Fobia2 Social (1,2)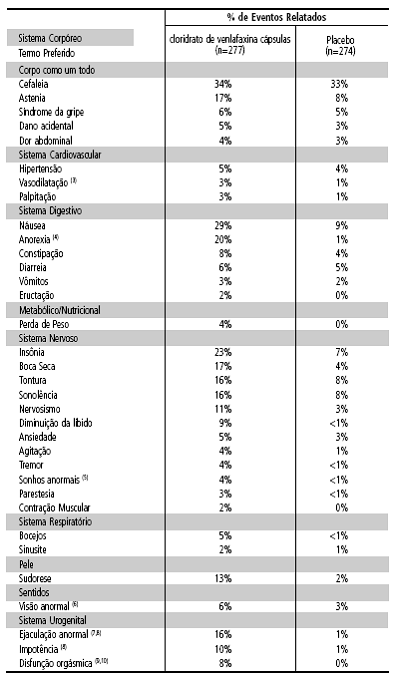
(1) Os eventos adversos cuja taxa de relato para cloridrato de venlafaxina cápsulas foi menor ou igual à do placebo1 não foram incluídos. Esses eventos são: dor nas costas22, depressão, dismenorreia23, dispepsia24, infecção27, mialgia31, dor, faringite32, erupção33 cutânea34, rinite29 e infecção27 no trato respiratório superior. (2) < 1% significa maior que zero, mas menor que 1%. (3) Principalmente “fogachos”. (4) Principalmente “diminuição do apetite” e “perda do apetite”. (5) Principalmente “sonhos vívidos”, “pesadelos” e “aumento de sonhos”. (6) Principalmente “visão turva”. (7) Inclui “ejaculação retardada” e “anorgasmia”. (8) A porcentagem baseia-se no número de homens (cloridrato de venlafaxina = 158, placebo1 = 153). (9) Inclui “orgasmo anormal” e “anorgasmia”. (10) A porcentagem baseia-se no número de mulheres (cloridrato de venlafaxina = 119, placebo1 = 121).
TABELA 5 – Incidência12 de Eventos Adversos Decorrentes do Tratamento nos Estudos Clínicos Controlados por Placebo1 e a Curto Prazo de cloridrato de venlafaxina cápsulas em Pacientes com Transtorno do Pânico (1,2)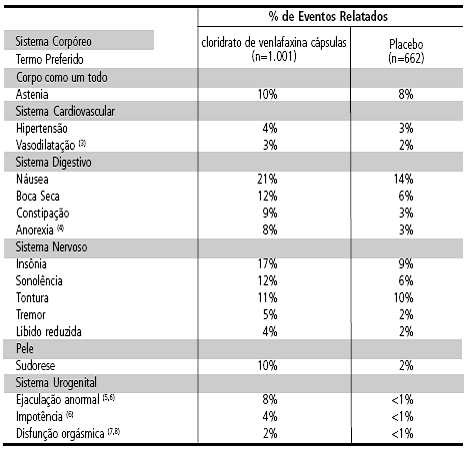
(1) Os eventos adversos cuja taxa de relato para cloridrato de venlafaxina cápsulas foi menor ou igual à do placebo1 não foram incluídos. Esses eventos são: dor abdominal, visão6 anormal, dano acidental, ansiedade, dor nas costas22, diarreia4, dismenorreia23, dispepsia24, síndrome25 da gripe26, cefaleia8, infecção27, nervosismo, dor, parestesia5, faringite32, erupção33 cutânea34, rinite29 e vômitos35. (2) < 1% significa maior que zero, mas menor que 1%. (3) Principalmente “fogachos”. (4) Principalmente “diminuição do apetite” e “perda do apetite”. (5) Inclui “ejaculação retardada” e “anorgasmia”. (6) A porcentagem baseia-se no número de homens (cloridrato de venlafaxina = 335, placebo1 = 238). (7) Inclui “anorgasmia” e “orgasmo retardado”. (8) A porcentagem baseia-se no número de mulheres (cloridrato de venlafaxina = 666, placebo1 = 424).
Alterações dos Sinais Vitais36 - o tratamento com cloridrato de venlafaxina cápsulas de liberação prolongada por até 12 semanas nos estudos pré-comercialização e controlados por placebo1 em transtorno depressivo maior foi associado a aumento final médio durante o tratamento da frequência de pulso de aproximadamente 2 batimentos por minuto em comparação a 1 batimento por minuto com placebo1. O tratamento com cloridrato de venlafaxina cápsulas por até 8 semanas nos estudos pré-comercialização e controlados por placebo1 em
Transtorno de Ansiedade Generalizada foi associado a aumento final médio durante o tratamento da freqüência de pulso de aproximadamente 2 batimentos por minuto em comparação a menos de 1 batimento por minuto com o placebo1. O tratamento com cloridrato de venlafaxina cápsulas por até 12 semanas nos estudos précomercialização e controlados por placebo1 em Fobia2 Social foi associado a aumento final médio durante o tratamento da frequência de pulso de aproximadamente 4 batimentos por minuto em comparação a um aumento de 1 batimento por minuto com o placebo1. O tratamento com este medicamento por até 12 semanas nos estudos pré-comercialização e controlados por placebo1 em Transtorno do Pânico foi associado ao aumento final médio durante o tratamento da frequência de pulso de aproximadamente 1 batimento por minuto em comparação à diminuição de menos de 1 batimento por minuto com o placebo1. Em um estudo de dose flexível, com doses de cloridrato de venlafaxina comprimidos no intervalo de 200-375 mg/dia e dose média maior que 300 mg/dia, a pulsação média aumentou cerca de 2 batimentos por minuto em comparação à diminuição de cerca de 1 batimento por minuto com o placebo1.
Alterações Laboratoriais - o tratamento com cloridrato de venlafaxina cápsulas de liberação prolongada por até 12 semanas nos estudos pré-comercialização e controlados por placebo1 em transtorno depressivo maior foi associado a aumento final médio durante o tratamento da concentração sérica de colesterol37 de aproximadamente 1,5 mg/dl38 em comparação à diminuição final média de 7,4 mg/dl38 com o placebo1. O tratamento com cloridrato de venlafaxina por até 8 semanas e até 6 meses nos estudos pré-comercialização e controlados por placebo1 em Transtorno de Ansiedade Generalizada foi associado a aumentos finais médios durante o tratamento da concentração sérica de colesterol37 de aproximadamente 1,0 mg/dl38 e 2,3 mg/dl38, respectivamente, enquanto os indivíduos do grupo placebo1 apresentaram diminuições finais médias de 4,9 mg/dl38 e de 7,7 mg/dl38, respectivamente. O tratamento com cloridrato de venlafaxina por até 12 semanas nos estudos pré-comercialização e controlados por placebo1 em Fobia2 Social, foi associado a aumentos finais médios durante o tratamento da concentração sérica de colesterol37 de aproximadamente 11,4 mg/dl38 em comparação à diminuição final média de 2,2 mg/dl38 com o placebo1. O tratamento com cloridrato de venlafaxina por até 12 semanas nos estudos pré-comercialização controlados por placebo1 em Transtorno do Pânico, foi associado a aumentos finais médios durante o tratamento da concentração sérica de colesterol37 de aproximadamente 5,8 mg/dl38 em comparação à diminuição final média de 3,7 mg/dl38 com o placebo1. Os pacientes tratados com cloridrato de venlafaxina comprimidos por, no mínimo 3 meses nos estudos de extensão controlados por placebo1 e de 12 meses de duração apresentaram um aumento final médio durante o tratamento do colesterol37 total de 9,1 mg/dl38 em comparação à diminuição de 7,1 mg/dl38 entre os pacientes tratados com placebo1. Esse aumento foi dependente da duração no período do estudo e tendeu a ser maior com as doses mais elevadas. Foram relatados aumentos clinicamente relevantes do colesterol37 sérico, definidos como:
1) aumento final durante o tratamento de colesterol37 sérico ≥ 50 mg/dl38 em relação à Fase Basal e para um valor ≥ 261 mg/dl38 ou 2) aumento médio durante o tratamento de colesterol37 sérico ≥ 50 mg/dl38 em relação à Fase Basal e para um valor ≥ 261 mg/dl38 em 5,3% dos pacientes tratados com a venlafaxina e em 0,0% dos que receberam o placebo1.
Alterações de ECG - em um estudo de dose flexível, com doses de cloridrato de venlafaxina comprimidos no intervalo de 200 a 375 mg/dia e dose média maior que 300 mg/dia, a alteração média da freqüência cardíaca foi de 8,5 batimentos por minuto em comparação a 1,7 batimento por minuto com o placebo1.
• Outros Eventos Adversos Observados Durante a Avaliação Pré-comercialização de cloridrato de venlafaxina comprimidos e cloridrato de venlafaxina cápsulas de liberação prolongada - durante a avaliação pré-comercialização, foram administradas doses múltiplas de cloridrato de venlafaxina cápsulas a 705 pacientes nos estudos Fase 3 em transtorno depressivo maior e cloridrato de venlafaxina comprimidos foi administrado a 96 pacientes. Durante a sua avaliação pré-comercialização, doses múltiplas de cloridrato de venlafaxina cápsulas também foram administradas a 1.381 pacientes nos estudos Fase 3 de
Transtorno de Ansiedade Generalizada, a 277 nos estudos Fase 3 de Fobia2 Social e a 1.001 nos estudos Fase 3 de Transtorno do Pânico. Além disso, na avaliação pré-comercialização de cloridrato de venlafaxina comprimidos, doses múltiplas foram administradas a 2.897 pacientes em estudos Fase 2-3 de transtorno depressivo maior. As condições e a duração da exposição à venlafaxina nos dois programas de desenvolvimento variaram muito e incluíram (em categorias sobrepostas) estudos abertos e duplo-cegos, não-controlados e controlados, estudos com pacientes internados (apenas cloridrato de venlafaxina comprimidos) e ambulatoriais
e estudos com dose fixa e titulação de dose. Os eventos indesejáveis associados a essa exposição foram registrados pelos investigadores clínicos utilizando a terminologia de sua escolha. Consequentemente, não é possível fornecer uma estimativa significativa da proporção de indivíduos que apresentaram eventos adversos sem primeiro agrupar os tipos semelhantes de eventos indesejáveis em um número menor de categorias padronizadas de eventos.
Nas listas a seguir, os eventos adversos relatados foram classificados utilizando a terminologia padrão do Dicionário COSTART. As frequências apresentadas, portanto, representam a proporção de 6.357 pacientes expostos a doses múltiplas de quaisquer formulações da venlafaxina que apresentaram um evento do tipo mencionado em, no mínimo, uma ocasião enquanto recebiam a venlafaxina. Todos os eventos relatados estão incluídos, exceto os já relacionados nas Tabelas 2, 3, 4 e 5 e os eventos para os quais a relação com o medicamento era remota. Se o termo COSTART para um evento fosse muito geral e não informativo, era substituído por um termo mais informativo. É importante enfatizar que, embora tenham ocorrido durante o tratamento com a venlafaxina, os eventos relatados não foram necessariamente causados por ela. Os eventos são classificados ainda por sistema corpóreo e relacionados em ordem decrescente de frequência, utilizando as definições a seguir: eventos adversos frequentes são definidos como os ocorridos em uma ou mais ocasiões em, no mínimo, 1/100 pacientes; eventos adversos infrequentes são os ocorridos em 1/100 a 1/1.000 pacientes; eventos raros são os ocorridos em menos de 1/1.000 pacientes.
Corpo como um todo - Frequente: dor torácica subesternal, calafrios39, febre40 e dor no pescoço41. Infrequente: edema42 facial, dano intencional, indisposição, monilíase, rigidez do pescoço41, dor pélvica43, reação de fotossensibilidade, tentativa de suicídio e síndrome25 de abstinência. Raro: apendicite44, bacteremia45, carcinoma46 e celulite47.
Sistema cardiovascular48 - Frequente: enxaqueca49, hipotensão50 postural e taquicardia51. Infrequente: angina52 pectoris, arritmia53, bradicardia54, extra-sístole55, hipotensão50, distúrbio vascular56 periférico (principalmente pés frios e/ou mãos57 frias), síncope58 e tromboflebite59. Raro: aneurisma60 da aorta61, arterite, bloqueio atrioventricular de primeiro grau, bigeminismo, bloqueio de ramo, fragilidade capilar62, isquemia63 cerebral, doença arterial coronariana, insuficiência cardíaca congestiva64, parada cardíaca, hematoma65, distúrbio cardiovascular (distúrbio circulatório e da válvula mitral), hemorragia66 mucocutânea, infarto do miocárdio67, palidez e arritmia53 sinusal.
Sistema digestivo68 - Frequente: aumento do apetite. Infrequente: bruxismo, colite69, disfagia70, edema42 da língua71, esofagite72, gastrite73, gastroenterite74, úlcera75 gastrintestinal, gengivite76, glossite77, hemorragia66 retal, hemorroidas78, melena79, monilíase oral, estomatite80 e ulceração81 na boca15. Raro: distensão abdominal, dor biliar, queilite, colecistite82, colelitíase83, espasmos84 esofágicos, duodenite, hematêmese85, doença do refluxo gastroesofágico86, hemorragia66 gastrintestinal, hemorragia66 gengival, hepatite87, ileíte88, icterícia89, obstrução intestinal, sensibilidade hepática90, parotite, periodontite, proctite91, distúrbio retal, glândulas salivares92 aumentadas, salivação aumentada, fezes amolecidas e descoloração da língua71.
Sistema endócrino93 - Raro: galactorreia94, bócio95, hipertireoidismo96, hipotireoidismo97, nódulo98 tireoideano, tireoidite.
Sistema linfático99 e sangue100 - Frequente: equimose101. Infrequente: anemia102, leucocitose103, leucopenia104, linfadenopatia e trombocitemia. Raro: basofilia, tempo de sangramento aumentado, cianose105, eosinofilia106, linfocitose, mieloma107 múltiplo, púrpura108 e trombocitopenia109.
Metabólico e nutricional - Frequente: edema42 e ganho de peso. Infrequente: fosfatase alcalina110 aumentada, hipercolesterolemia111, hiperglicemia112, hiperlipemia, hipocalemia113, TGO (AST) aumentada, TGP (ALT) aumentada e sede. Raro: intolerância ao álcool, bilirrubinemia, ureia114 sanguínea aumentada, creatinina115 aumentada, desidratação116, diabetes mellitus117, glicosúria118, gota119, cicatrização anormal, hemocromatose120, hipercalcinúria, hipercalemia121, hiperfosfatemia, hiperuricemia, hipocolesterolemia, hipoglicemia122, hiponatremia123, hipofosfatemia, hipoproteinemia e uremia124.
Sistema musculoesquelético - Frequente: artralgia125. Infrequente: artrite126, artrose127, esporões ósseos, bursite128, cãimbras nas pernas, miastenia129 e tenossinovite. Raro: dor óssea, fratura130 patológica, cãibra muscular, espasmos84 musculares, rigidez musculoesquelética, miopatia131, osteoporose132, osteosclerose, fasciíte plantar, artrite reumatóide133 e ruptura de tendão134.
Sistema nervoso135 - Frequente: amnésia136, confusão, despersonalização, hipestesia, pensamento anormal e vertigem137. Infrequente: acatisia138, apatia139, ataxia140, parestesia5 perioral, estimulação do SNC16, labilidade emocional, euforia, alucinações141, hostilidade, hiperestesia, hipercinesia142, hipotonia143, incoordenação, reação maníaca, mioclonia144, neuralgia145, neuropatia146, psicose147, crises convulsivas, fala anormal, estupor e trismo. Raro: comportamento anormal/alterado, transtorno de ajuste, acinesia, abuso de álcool, afasia148, bradicinesia149, síndrome25 bucolingual, acidente vascular cerebral150, sensação de embriaguez, perda da consciência, delírios, demência151, distonia152, energia aumentada, paralisia153 facial, marcha anormal, Síndrome25 de Guillain-Barre, hipercloridria, hipocinesia, histeria, dificuldades para controlar impulso, libido11 aumentada, cinesia, neurite154, nistagmo155, reação paranóica, paresia156, depressão psicótica, reflexos diminuídos, reflexos aumentados, ideação suicida e torcicolo157.
Sistema respiratório158 - Frequente: tosse aumentada e dispneia159. Infrequente: asma160, congestão torácica, epistaxe161, hiperventilação, laringismo, laringite162, pneumonia163 e alteração da voz. Raro: atelectasia164, hemoptise165, hipoventilação, hipóxia166, edema42 de laringe167, pleurisia, embolia168 pulmonar e apneia169 do sono.
Pele170 e apêndices - Frequente: prurido171. Infrequente: acne172, alopecia173, dermatite174 de contato, pele170 ressecada, eczema175, erupção33 cutânea34 maculopapular176, psoríase177 e urticária178. Raro: unhas179 fracas, eritema nodoso180, dermatite174 esfoliativa, dermatite174 liquenoide, descoloração do cabelo181, descoloração da pele170, furunculose, hirsutismo182, leucoderma, miliária, erupção33 cutânea34 petequial, erupção33 cutânea34 pustular, erupção33 cutânea34 vesiculobolhosa, seborreia183, atrofia184 cutânea34, hipertrofia185 cutânea34, estrias cutâneas186 e sudorese17 diminuída.
Sentidos - Frequente: anormalidade de acomodação, midríase187 e alteração do paladar188. Infrequente: conjuntivite189, diplopia190, olhos191 ressecados, dor nos olhos191, hiperacusia, otite média192, parosmia, fotofobia193, perda do paladar188 e defeito do campo visual194. Raro: blefarite195, catarata196, cromatopsia, edema42 conjuntival, lesão197 corneana, surdez, exoftalmia, hemorragia66 ocular, glaucoma198, hemorragia66 retineana, hemorragia66 subconjuntival, ceratite, labirintite199, miose200, papiledema, reflexo pupilar reduzido, otite externa201, esclerite202 e uveíte203.
Sistema urogenital204 - Frequente: distúrbio prostático (prostatite205, próstata206 aumentada e irritabilidade da próstata206)* e micção207 prejudicada. Infrequente: albuminúria208, amenorreia209*, cistite210, disúria211, hematúria212, cálculo213 renal214, dor nos rins215, leucorreia216*, menorragia217*, metrorragia218*, noctúria, dor nas mamas219, poliúria220, piúria, incontinência urinária221, retenção urinária222, urgência223 urinária, hemorragia vaginal224* e vaginite225*. Raro: aborto*, anúria226, secreção das mamas219, inchaço227 das mamas219, balanite*, aumento das mamas219 e endometriose228*, lactação229 feminina*, mama230 fibrocística, cristalúria cálcica, cervicite231*, orquite232*, cisto de ovário233*, dor na bexiga234, ereção235 prolongada*, ginecomastia236 (homens)*, hipomenorreia*, função renal214 anormal, mastite237, menopausa238*, pielonefrite239, oligúria240, salpingite*, urolitíase, hemorragia66 uterina*, espasmo241 uterino* e secura vaginal*.
* Com base no número de homens e mulheres, conforme o caso.
Relatos Pós-comercialização - Os relatos voluntários de outros eventos adversos temporariamente associados ao uso da venlafaxina recebidos desde o lançamento comercial e que podem não ter relação causal com o uso da venlafaxina são: agranulocitose242, anafilaxia243, anemia aplásica244, catatonia, anormalias congênitas245, creatinina115 fosfoquinase aumentada, tromboflebite59 venosa profunda, delírio246; anormalidades no ECG como prolongamento do intervalo QT; arritmias247 cardíacas incluindo fibrilação atrial, taquicardia51 supraventricular, extra-sístole ventricular248 e relatos raros de fibrilação ventricular e taquicardia51 ventricular, incluindo torsades de pointes; necrose249 epidérmica/Síndrome de Stevens-Johnson250, eritema multiforme251, sintomas252 extrapiramidais (incluindo discinesia e discinesia tardia253), hemorragia66 (incluindo sangramento ocular e gastrintestinal), eventos hepáticos (incluindo elevação de gama glutamil transpeptidase; anormalidade das provas de função hepática90 não-específicas; dano hepático, necrose249 ou insuficiência254 e fígado255 gorduroso), movimentos involuntários, HDL256 aumentado, eventos semelhantes à síndrome25 neuroléptica maligna (incluindo um caso de uma criança de 10 anos que poderia estar tomando metilfenidato, foi tratada e recuperou-se), neutropenia257, suores noturnos, pancreatite258, pancitopenia259, pânico, prolactina260 aumentada, eosinofilia106 pulmonar, insuficiência renal261, rabdomiólise262, síndrome da serotonina263, sensações elétricas semelhantes a choque264 ou tinido (em alguns casos, posteriores à descontinuação da venlafaxina ou à diminuição gradativa da dose) e síndrome25 da secreção inapropriada de hormônio265 antidiurético (normalmente em idosos). Houve relatos de níveis elevados de clozapina temporariamente associados a eventos adversos, incluindo convulsões, após a adição da venlafaxina. Houve relatos de aumento do tempo de protrombina266, tempo de tromboplastina267 parcial ou INR (International Normalized Ratio) quando a venlafaxina foi administrada a pacientes que estavam recebendo tratamento com varfarina.
Complementos