
REAÇÕES ADVERSAS CLORIDRATO DE IRINOTECANO
DADOS DE EVENTOS ADVERSOS FORAM COLETADOS E ANALISADOS EXTENSIVAMENTE NO PROGRAMA DE ESTUDOS CLÍNICOS PARA NEOPLASIA1 COLO2-RETAL METASTÁTICA RECORRENTE OU QUE PROGREDIU DEPOIS DE TERAPIA COM BASE NO 5-FU (SEGUNDA LINHA) E SÃO APRESENTADOS ABAIXO (POPULAÇÃO DE PACIENTES DESCRITA A SEGUIR). ESPERA-SE QUE OS EVENTOS ADVERSOS OCORRIDOS NAS OUTRAS INDICAÇÕES SEJAM SEMELHANTES AOS OCORRIDOS NO CASO DE TRATAMENTO DE SEGUNDA LINHA DE NEOPLASIA1 COLO2-RETAL.
ESQUEMA DE DOSES SEMANAIS
EM TRÊS ESTUDOS CLÍNICOS REALIZADOS NOS EUA, 304 PACIENTES COM CARCINOMA3 METASTÁTICO DO CÓLON4 OU RETO5 QUE HAVIAM APRESENTADO RECIDIVA6 OU AVANÇO DA DOENÇA APÓS UMA TERAPIA BASEADA EM 5-FU FORAM TRATADOS COM CLORIDRATO DE IRINOTECANO COMO AGENTE ÚNICO, EM UM ESQUEMA DE DOSAGEM DE 100 A 125 MG/M2.
DEZESSETE DESSES PACIENTES FORAM A ÓBITO7 DENTRO DE UM PERÍODO DE 30 DIAS APÓS A ADMINISTRAÇÃO DO PRODUTO; EM CINCO CASOS (1,6%) AS MORTES FORAM POTENCIALMENTE FÁRMACO8-DEPENDENTES. OS CINCO PACIENTES APRESENTARAM EFEITOS ADVERSOS VARIADOS, QUE INCLUÍRAM EFEITOS CONHECIDOS DO PRODUTO (MIELOSSUPRESSÃO, SEPTICEMIA9 NEUTROPÊNICA SEM FEBRE10, OBSTRUÇÃO DE INTESTINO DELGADO11, ACÚMULO DE FLUIDO, ESTOMATITE12, NÁUSEA13, VÔMITOS14, DIARRÉIA15 E DESIDRATAÇÃO16). UM DESSES PACIENTES FOI A ÓBITO7 POR “SÉPSIS” NEUTROPÊNICA SEM FEBRE10. A NEUTROPENIA17 FEBRIL, DEFINIDA COMO NEUTROPENIA17 DE GRAU 4 PELO NCI E FEBRE10 DE GRAU 2 OU MAIOR, OCORREU EM OUTROS NOVE PACIENTES, TENDO ESSES PACIENTES SE RECUPERADO COM TRATAMENTO DE SUPORTE. CENTO E DEZENOVE PACIENTES FORAM HOSPITALIZADOS NUM TOTAL DE 156 VEZES DEVIDO A EFEITOS ADVERSOS; 81 (26,6%) PACIENTES FORAM HOSPITALIZADOS DEVIDO A EVENTOS CONSIDERADOS RELACIONADOS AO IRINOTECANO. AS RAZÕES PRINCIPAIS PARA A HOSPITALIZAÇÃO FÁRMACO8-RELACIONADA FORAM DIARRÉIA15, COM OU SEM NÁUSEA13 E/OU VÔMITOS14; NEUTROPENIA17/LEUCOPENIA18, COM OU SEM DIARRÉIA15 E/OU FEBRE10; E NÁUSEAS19 E/OU VÔMITOS14. FORAM REALIZADOS AJUSTES POSOLÓGICOS DURANTE O CICLO DE TRATAMENTO E NOS CICLOS SUBSEQÜENTES, COM BASE NA TOLERÂNCIA INDIVIDUAL DO PACIENTE. AS RAZÕES MAIS COMUNS PARA A REDUÇÃO DE DOSE FORAM DIARRÉIA15 TARDIA, NEUTROPENIA17 E LEUCOPENIA18. TREZE PACIENTES DESCONTINUARAM O TRATAMENTO COM CLORIDRATO DE IRINOTECANO DEVIDO A EVENTOS ADVERSOS.
OS EVENTOS ADVERSOS (GRAUS 1-4 NCI) RELACIONADOS À DROGA CONFORME O JULGAMENTO DO INVESTIGADOR QUE FORAM RELATADOS EM MAIS DE 10% DOS 304 PACIENTES INCLUÍDOS NOS TRÊS ESTUDOS DO ESQUEMA POSOLÓGICO SEMANAL ESTÃO LISTADOS EM ORDEM DECRESCENTE DE FREQÜÊNCIA NA TABELA 1.
TABELA 1. EVENTOS ADVERSOS GRAUS 1 A 4 NCI RELACIONADOS À DROGA OBSERVADOS EM MAIS DE 10% DOS PACIENTES NOS ESTUDOS CLÍNICOS:

ESQUEMA POSOLÓGICO DE UMA DOSE A CADA 3 SEMANAS NO TOTAL, 535 PACIENTES COM NEOPLASIA1 COLO2-RETAL METASTÁTICA CUJA DOENÇA RECORREU OU PROGREDIU APÓS O TRATAMENTO PRÉVIO COM 5-FU, PARTICIPARAM DOS DOIS ESTUDOS DE FASE 3: 316 RECEBERAM O IRINOTECANO, 129 RECEBERAM O 5-FU E 90 RECEBERAM O MELHOR TRATAMENTO DE SUPORTE. ONZE PACIENTES TRATADOS COM O IRINOTECANO MORRERAM DENTRO DE 30 DIAS DE TRATAMENTO. EM TRÊS CASOS, AS MORTES FORAM POTENCIALMENTE RELACIONADAS COM O TRATAMENTO COM O IRINOTECANO E FORAM ATRIBUÍDAS À INFECÇÃO20 NEUTROPÊNICA, DIARRÉIA15 DE GRAU 4 E ASTENIA21, RESPECTIVAMENTE. AS HOSPITALIZAÇÕES POR EVENTOS ADVERSOS SÉRIOS (A DESPEITO DELES SEREM RELACIONADOS, OU NÃO, COM O TRATAMENTO EM ESTUDO) OCORRERAM PELO MENOS UMA VEZ EM 60% DOS PACIENTES QUE RECEBERAM O IRINOTECANO, 63% (57/90) QUE RECEBERAM O MELHOR TRATAMENTO DE SUPORTE E 39% (50/129) QUE RECEBERAM O TRATAMENTO BASEADO NA 5-FU. OITO POR CENTO DOS PACIENTES TRATADOS COM O IRINOTECANO E 7% (9/129) DOS PACIENTES TRATADOS COM O TRATAMENTO BASEADO NA 5-FU INTERROMPERAM O TRATAMENTO POR EVENTOS ADVERSOS.
DOS 316 PACIENTES TRATADOS COM O IRINOTECANO, OS EVENTOS ADVERSOS MAIS CLINICAMENTE SIGNIFICATIVOS (TODOS OS GRAUS: 1–4) FORAM DIARRÉIA15 (84%), ALOPECIA22 (72%), NÁUSEAS19 (70%), VÔMITOS14 (62%), SINTOMAS23 COLINÉRGICOS (47%) E NEUTROPENIA17 (30%). A TABELA A SEGUIR APRESENTA UMA LISTA DOS EVENTOS ADVERSOS DE GRAU 3 E 4, RELATADOS NOS PACIENTES ADMITIDOS EM TODOS OS BRAÇOS DE TRATAMENTO DOS DOIS ESTUDOS CLÍNICOS DESCRITOS.
TABELA 2. PORCENTAGEM DE PACIENTES QUE APRESENTARAM EVENTOS ADVERSOS DE GRAU 3 E 4 NOS ESTUDOS COMPARATIVOS DO TRATAMENTO COM UMA DOSE DE IRINOTECANO A CADA 3 SEMANAS:
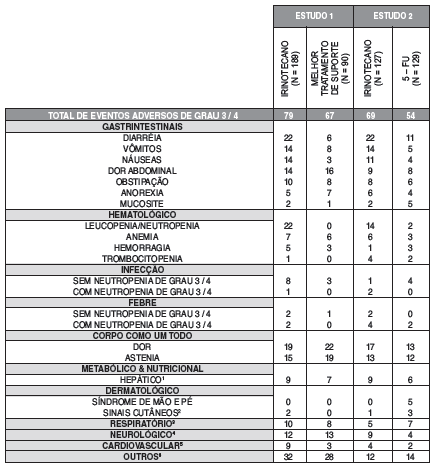
1 - HEPÁTICO INCLUI EVENTOS COMO ASCITE24 E ICTERÍCIA25
2 - SINAIS26 CUTÂNEOS INCLUEM EVENTOS COMO EXANTEMA27
3 - RESPIRATÓRIO INCLUI EVENTOS COMO DISPNÉIA28 E TOSSE
4 - NEUROLÓGICO INCLUI EVENTOS COMO SONOLÊNCIA
5 - CARDIOVASCULAR INCLUI EVENTOS COMO AS ARRITMIAS29, ISQUEMIA30 E DISFUNÇÃO CARDÍACA MECÂNICA
6 – OUTROS: INCLUI EVENTOS COMO LESÃO31 ACIDENTAL, HEPATOMEGALIA32, SÍNCOPE33, VERTIGEM34 E PERDA DE PESO
NO SISTEMA GASTRINTESTINAL, DIARRÉIA15, NÁUSEA13 E VÔMITO35 FORAM EVENTOS ADVERSOS COMUNS APÓS O TRATAMENTO COM O PRODUTO, PODENDO SER GRAVES. TAIS EVENTOS OCORRERAM PRECOCEMENTE (DURANTE OU ATÉ 24 HORAS DA ADMINISTRAÇÃO DO PRODUTO) OU TARDIAMENTE (MAIS DE 24 HORAS APÓS A ADMINISTRAÇÃO). NOS ESTUDOS CLÍNICOS UTILIZANDO O ESQUEMA POSOLÓGICO DE UMA DOSE A CADA 3 SEMANAS, O TEMPO MÉDIO PARA APARECIMENTO DA DIARRÉIA15 TARDIA FOI DE 5 DIAS APÓS A INFUSÃO DE IRINOTECANO. NOS ESTUDOS COM ESQUEMA POSOLÓGICO SEMANAL, O PERÍODO MÉDIO ATÉ O APARECIMENTO DE DIARRÉIA15 TARDIA FOI DE 11 DIAS APÓS A ADMINISTRAÇÃO DO PRODUTO. NO CASO DOS PACIENTES QUE INICIARAM O TRATAMENTO COM A DOSE DE 125 MG/M2, A DURAÇÃO MÉDIA DA DIARRÉIA15 DE QUALQUER GRADUAÇÃO FOI DE 3 DIAS. ENTRE OS PACIENTES TRATADOS COM A DOSE DE 125 MG/M2 QUE EXPERIMENTARAM DIARRÉIA15 DE GRAUS 3 OU 4, A DURAÇÃO MÉDIA DO EPISÓDIO DIARRÉICO FOI DE 7 DIAS. A FREQÜÊNCIA DE DIARRÉIA15 TARDIA GRAUS 3 E 4 FOI ALGO SUPERIOR EM PACIENTES QUE INICIARAM O TRATAMENTO COM 125 MG/M2 DO QUE EM PACIENTES QUE RECEBERAM UMA DOSE INICIAL DE 100 MG/M2 (34% VERSUS 24%). A FREQÜÊNCIA DE DIARRÉIA15 TARDIA GRAUS 3 E 4 FOI SIGNIFICATIVAMENTE MAIOR EM PACIENTES COM IDADE IGUAL OU SUPERIOR A 65 ANOS DO QUE EM PACIENTES COM IDADE INFERIOR A 65 ANOS (39,8% VERSUS 23,4%; P = 0,0025). EM UM DOS ESTUDOS, A FREQÜÊNCIA DE DIARRÉIA15 GRAUS 3 E 4 FOI SIGNIFICATIVAMENTE MAIOR EM PACIENTES DO SEXO MASCULINO DO QUE DO SEXO FEMININO (43,1% VERSUS 15,6%, P = 0,01). NÃO HOUVE, ENTRETANTO, DIFERENÇAS LIGADAS AO SEXO NA FREQÜÊNCIA DE DIARRÉIA15 TARDIA GRAUS 3 E 4 NOS OUTROS 2 ESTUDOS DO ESQUEMA POSOLÓGICO DE ADMINISTRAÇÃO SEMANAL. FORAM OBSERVADAS ÚLCERAS36 COLÔNICAS, ALGUMAS VEZES, COM HEMORRAGIA37 GASTRINTESTINAL, EM ASSOCIAÇÃO COM A ADMINISTRAÇÃO DE CLORIDRATO DE IRINOTECANO.
HEMATOLOGIA: O PRODUTO CAUSA COMUMENTE NEUTROPENIA17, LEUCOPENIA18 (INCLUINDO LINFOCITOPENIA) E ANEMIA38. A TROMBOCITOPENIA39 SÉRIA É INCOMUM. QUANDO A NEUTROPENIA17 FOI AVALIADA NOS ESTUDOS DE ADMINISTRAÇÃO SEMANAL, A FREQÜÊNCIA DA NEUTROPENIA17 DE GRAU 3 E 4 FOI SIGNIFICATIVAMENTE MAIOR EM PACIENTES QUE FORAM SUBMETIDOS À IRRADIAÇÃO PÉLVICA40/ABDOMINAL PRÉVIA QUE EM PACIENTES QUE NÃO SE SUBMETERAM A ESSE TIPO DE TRATAMENTO (48% [13/27] VERSUS 24% [67/277]; P = 0,04). NESSES MESMOS ESTUDOS, OS PACIENTES COM NÍVEIS SÉRICOS BASAIS DE BILIRRUBINA41 TOTAL DE 1,0 MG/DL42 OU MAIS TAMBÉM APRESENTARAM UMA PROBABILIDADE SIGNIFICATIVAMENTE MAIOR DE APRESENTAR NEUTROPENIA17 DE GRAU 3 OU 4 NA PRIMEIRA SESSÃO DE TRATAMENTO QUE OS PACIENTES COM NÍVEIS DE BILIRRUBINA41 INFERIORES A 1,0 MG/DL42 (50% [19/38] VERSUS 18% [47/266]; P < 0,001). NÃO HOUVE DIFERENÇAS SIGNIFICATIVAS NA FREQÜÊNCIA DE NEUTROPENIA17 DE GRAU 3 E 4 POR IDADE OU SEXO. NOS ESTUDOS CLÍNICOS QUE AVALIARAM O ESQUEMA DE ADMINISTRAÇÃO SEMANAL, OCORREU NEUTROPENIA17 FEBRIL (NEUTROPENIA17 DE GRAU 4 CONCOMITANTE DE ACORDO COM OS CRITÉRIOS DE NCI - INSTITUTO NACIONAL DO CÂNCER43 - E FEBRE10 DE GRAU 2 OU MAIS) EM 3% DOS PACIENTES; 6% DOS PACIENTES RECEBERAM G-CSF PARA O TRATAMENTO DE NEUTROPENIA17. FOI OBSERVADA ANEMIA38 DE GRAU 3 OU 4 DE ACORDO COM OS CRITÉRIOS DE NCI EM 7% DOS PACIENTES TRATADOS COM ADMINISTRAÇÕES SEMANAIS; FORAM FEITAS TRANSFUSÕES DE SANGUE44 A 10% DOS PACIENTES NESSES ESTUDOS.
GERAIS: ASTENIA21, FEBRE10 E DOR ABDOMINAL GERALMENTE SÃO OS EVENTOS MAIS COMUNS DESSE TIPO.
SINTOMAS23 COLINÉRGICOS: OS PACIENTES PODEM TER SINTOMAS23 COLINÉRGICOS DE RINITE45, SALIVAÇÃO AUMENTADA, MIOSE46, LACRIMEJAMENTO, DIAFORESE47, RUBOR E HIPERPERISTALTISMO INTESTINAL QUE PODE CAUSAR CÓLICAS48 ABDOMINAIS E DIARRÉIA15 PRECOCE. SE ESSES SINTOMAS23 OCORREREM, ELES MANIFESTAM-SE DURANTE A INFUSÃO DA DROGA OU IMEDIATAMENTE APÓS A INFUSÃO DA DROGA. PENSA-SE QUE ELES ESTEJAM RELACIONADOS COM A ATIVIDADE ANTICOLINESTERÁSICA DO COMPOSTO PARENTAL DE IRINOTECANO E ESPERASE QUE ELES OCORRAM MAIS FREQÜENTEMENTE COM DOSES MAIS ELEVADAS DO IRINOTECANO.
HEPÁTICO: NOS ESTUDOS CLÍNICOS QUE AVALIARAM O ESQUEMA POSOLÓGICO SEMANAL, FORAM OBSERVADAS ANORMALIDADES DE ENZIMAS HEPÁTICAS49 DE GRAU 3 OU 4 COM BASE NOS CRITÉRIOS DO NCI EM MENOS DE 10% DOS PACIENTES. ESSES EVENTOS OCORREM TIPICAMENTE EM PACIENTES COM METÁSTASES50 HEPÁTICAS51 COMPROVADAS.
DERMATOLÓGICO: FOI RELATADA ALOPECIA22 DURANTE O TRATAMENTO COM CLORIDRATO DE IRINOTECANO.
TAMBÉM FORAM RELATADOS EXANTEMAS52 QUE NÃO LEVARAM À INTERRUPÇÃO DO TRATAMENTO.
RESPIRATÓRIO: EVENTOS PULMONARES GRAVES SÃO INFREQÜENTES. NOS ESTUDOS CLÍNICOS QUE AVALIARAM O ESQUEMA POSOLÓGICO SEMANAL, FOI RELATADA DISPNÉIA28 DE GRAU 3 OU 4 COM BASE NOS CRITÉRIOS DO NCI EM 4% DOS PACIENTES. MAIS DA METADE DOS PACIENTES COM DISPNÉIA28 APRESENTAVAM METÁSTASES50
PULMONARES: NÃO SE SABE QUANTO O COMPROMETIMENTO PULMONAR MALIGNO OU OUTRAS DOENÇAS PULMONARES PRÉ-EXISTENTES PODEM TER CONTRIBUÍDO PARA A DISPNÉIA28 NESSES PACIENTES.
NEUROLÓGICO: PODEM OCORRER INSÔNIA E TONTURA53, MAS HABITUALMENTE ELAS NÃO SÃO CONSIDERADAS COMO DIRETAMENTE RELACIONADAS COM A ADMINISTRAÇÃO DO PRODUTO. A TONTURA53, ALGUMAS VEZES, PODE REPRESENTAR UMA EVIDÊNCIA SINTOMÁTICA54 DE HIPOTENSÃO55 ORTOSTÁTICA EM PACIENTES COM DESIDRATAÇÃO16.
CARDIOVASCULAR: PODE OCORRER VASODILATAÇÃO (RUBOR) DURANTE A ADMINISTRAÇÃO DE CLORIDRATO DE IRINOTECANO. TAMBÉM PODE OCORRER BRADICARDIA56, MAS ELA NÃO EXIGIU INTERVENÇÃO. ESSES EFEITOS FORAM ATRIBUÍDOS À SÍNDROME57 COLINÉRGICA58, OBSERVADA ALGUMAS VEZES DURANTE OU IMEDIATAMENTE APÓS A INFUSÃO DO PRODUTO.
ESTÃO LISTADOS NAS TABELAS 3 A 5, EM ORDEM DECRESCENTE DE FREQÜÊNCIA, OS EVENTOS ADVERSOS GRAUS 3 OU 4 NCI RELATADOS NOS ESTUDOS CLÍNICOS DO ESQUEMA POSOLÓGICO SEMANAL OU A CADA 3 SEMANAS (N=620).
TABELA 3. EVENTOS ADVERSOS GRAUS 3 OU 4 NCI RELACIONADOS À DROGA OBSERVADOS EM MAIS DE 10% DOS PACIENTES NOS ESTUDOS CLÍNICOS:
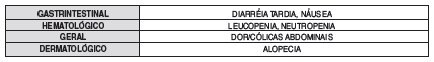
TABELA 4. EVENTOS ADVERSOS GRAUS 1 A 4 NCI RELACIONADOS À DROGA OBSERVADOS EM 1% A 10% DOS PACIENTES NOS ESTUDOS CLÍNICOS:

TABELA 5. EVENTOS ADVERSOS GRAUS 1 A 4 NCI RELACIONADOS À DROGA OBSERVADOS EM MENOS DE 1% DOS PACIENTES NOS ESTUDOS CLÍNICOS:

OS SEGUINTES EVENTOS ADICIONAIS RELACIONADOS À DROGA FORAM RELATADOS NOS ESTUDOS CLÍNICOS COM IRINOTECANO MAS NÃO VÃO DE ENCONTRO AOS CRITÉRIOS ACIMA DEFINIDOS (OCORRÊNCIA >10% DE EVENTOS RELACIONADOS À DROGA NCI GRAUS 1-4 OU DE NCI GRAUS 3 OU 4): RINITE45, SALIVAÇÃO AUMENTADA, MIOSE46, LACRIMEJAMENTO, DIAFORESE47, ERITEMA59, BRADICARDIA56, TONTURAS60, EXTRAVASAMENTO, SÍNDROME57 DA LISE61 TUMORAL E ULCERAÇÃO62 DO CÓLON4.
EFEITOS OBSERVADOS EM OUTROS ESTUDOS CLÍNICOS
O IRINOTECANO FOI ESTUDADO EM MAIS DE 1.100 PACIENTES NO JAPÃO. OS PACIENTES DESSES ESTUDOS APRESENTAVAM VÁRIOS TIPOS DE TUMOR63, INCLUINDO NEOPLASIA1 DE CÓLON4 OU RETO5, E FORAM TRATADOS COM VÁRIOS ESQUEMAS E DOSES DIFERENTES. EM GERAL, OS TIPOS DE EFEITOS TÓXICOS OBSERVADOS FORAM SEMELHANTES AOS OBSERVADOS NOS ESTUDOS REALIZADOS COM O CLORIDRATO DE IRINOTECANO NOS ESTADOS UNIDOS. ALGUMAS INFORMAÇÕES RELATADAS NOS ESTUDOS JAPONESES INDICAM QUE PACIENTES COM ASCITE24 CONSIDERÁVEL OU DERRAMES PLEURAIS TINHAM UM RISCO AUMENTADO DE NEUTROPENIA17 OU DIARRÉIA15. FOI OBSERVADA UMA SÍNDROME57 PULMONAR QUE OFERECE POTENCIALMENTE RISCO DE VIDA, CARACTERIZADA POR DISPNÉIA28, FEBRE10 E UM PADRÃO RETICULONODULAR À RADIOGRAFIA DE TÓRAX64, EM UMA PEQUENA PORCENTAGEM DE PACIENTES NOS PRIMEIROS ESTUDOS REALIZADOS NO JAPÃO. A CONTRIBUIÇÃO DO IRINOTECANO PARA ESSES EVENTOS PRELIMINARES FOI DIFÍCIL DE AVALIAR, PORQUE ESSES PACIENTES TAMBÉM TINHAM TUMORES PULMONARES E ALGUNS TINHAM UMA DOENÇA PULMONAR NÃO-MALIGNA PRÉ-EXISTENTE. ENTRETANTO, EM CONSEQÜÊNCIA DESSAS OBSERVAÇÕES, OS ESTUDOS CLÍNICOS REALIZADOS NOS ESTADOS UNIDOS ADMITIRAM POUCOS PACIENTES COM COMPROMETIMENTO DA FUNÇÃO PULMONAR, ASCITE24 SIGNIFICATIVA OU DERRAMES PLEURAIS.
FARMACOVIGILÂNCIA PÓS-COMERCIALIZAÇÃO
CASOS DE COLITE65 FORAM RELATADOS. EM ALGUNS CASOS, A COLITE65 FOI COMPLICADA POR ÍLEO66 OU MEGACÓLON67 TÓXICO. CASOS DE ÍLEO66 SEM COLITE65 ANTERIOR TAMBÉM FORAM RELATADOS. REAÇÕES DE HIPERSENSIBILIDADE INCLUSIVE REAÇÕES GRAVES ANAFILÁTICA OU ANAFILACTÓIDE FORAM RELATADAS (VIDE ITEM “ADVERTÊNCIAS” E “PRECAUÇÕES”).
- POSOLOGIA E ADMINISTRAÇÃO:
Todas as doses de irinotecano devem ser administradas como uma infusão intravenosa ao longo de 30 a 90 minutos.
A) Tratamento da neoplasia1 colo2-retal
Esquemas posológicos como agente único
Esquemas posológicos como agente único foram extensivamente estudados na neoplasia1 colo2-retal metastática.
Dose Inicial
Esquema Posológico Semanal: a dose recomendada de início do cloridrato de irinotecano como agente único é de 125 mg/m2. Uma dose menor inicial pode ser considerada (p. ex., 100 mg/m2) para pacientes68 com uma das seguintes condições: idade de 65 anos ou mais, radioterapia69 extensa anterior, status de desempenho de 2, níveis aumentados de bilirrubina41 ou neoplasia1 gástrica. O esquema de tratamento recomendado (um ciclo terapêutico) é de 125 mg/ m2 administrados uma vez por semana durante 4 semanas, seguido de um período de descanso de 2 semanas. Em seguida, os ciclos terapêuticos adicionais podem ser repetidos a cada 6 semanas (4 semanas em terapia, seguido de 2 semanas sem terapia). Recomenda-se que as doses posteriores sejam ajustadas a um valor máximo de 150 mg/m2 ou mínimo de 50 mg/m2, com incrementos de 25 mg/m2 a 50 mg/ m2 dependendo da tolerância individual ao tratamento de cada paciente (vide tabela a seguir). Desde que não se desenvolva uma toxicidade70 intolerável, o tratamento com ciclos terapêuticos adicionais de cloridrato de irinotecano pode ser continuado indefinidamente em pacientes responsivos ou em pacientes cuja doença permaneça estável. Os pacientes devem ser monitorados cuidadosamente quanto à toxicidade70.
Esquema Posológico de Uma Vez a Cada 2 Semanas: a dose usual recomendada de início do cloridrato de irinotecano é de 250 mg/m2 a cada duas semanas por infusão intravenosa. Uma dose inicial menor pode ser considerada (p.e., 200 mg/ m2) para pacientes68 com qualquer das seguintes condições: idade de 65 anos ou mais, radioterapia69 extensa anterior, status de desempenho de 2, níveis aumentados de bilirrubina41 ou neoplasia1 gástrica.
Esquema Posológico de Uma Vez a Cada 3 Semanas: a dose inicial recomendada habitual de cloridrato de irinotecano injetável para o esquema posológico de uma dose a cada 3 semanas é 350 mg/m2 por infusão intravenosa. Para os pacientes com 65 anos ou mais ou que receberam radioterapia69 pélvica40/abdominal anterior ou que têm um status de desempenho de 2 ou que apresentam neoplasia1 gástrica, a dose inicial recomendada é 300 mg/m2. Não se pode recomendar nenhuma dosagem para pacientes68 com bilirrubina41 > 2 mg/dl42, porque esses pacientes não foram incluídos nos estudos clínicos.
Após a instituição do tratamento com o produto, os pacientes devem ser monitorados cuidadosamente quanto à toxicidade70.
Doses subseqüentes devem ser ajustadas para 200 mg/m2 com incrementos de 50 mg/m2, dependendo da tolerância do paciente individual ao tratamento (vide tabela a seguir).
Todas as doses devem ser administradas como infusão intravenosa durante 90 minutos (vide item “Preparo e Estabilidade da Solução para Infusão”). O esquema terapêutico recomendado (uma sessão) é uma dose a cada 3 semanas. Desde que o paciente não desenvolva um efeito tóxico intolerável, o tratamento com sessões terapêuticas adicionais de cloridrato de irinotecano
pode ser mantido indefinidamente, desde que os pacientes continuem a obter um benefício clínico.
Esquemas Posológicos em Combinação
Dose Inicial
Irinotecano Combinado com 5-Fluoruracil (5-FU) e Folinato de cálcio: recomendado para uso em pacientes com neoplasia1 coloretal metastática.
A dose inicial recomendada é de 125 mg/m2 de cloridrato de irinotecano, 500 mg/m2 de 5-FU, e 20 mg/m2 de folinato de cálcio.
Doses iniciais menores podem ser consideradas para o cloridrato de irinotecano (p.e., 100 mg/m2) e 5-FU (p.e., 400 mg/m2) para os pacientes com 65 anos ou mais ou que receberam radioterapia69 pélvica40/abdominal anterior ou que têm um status de desempenho de 2 ou que apresentam níveis aumentados de bilirrubina41 ou neoplasia1 gástrica. O tratamento deve ser dado em cursos repetidos a cada 6 semanas, incluindo tratamento semanal por 4 semanas, seguido de um repouso de 2 semanas.
B) Tratamento dos outros tipos de neoplasias71
Esquemas posológicos como agente único
Três esquemas posológicos são recomendados para o tratamento de outros tipos de neoplasias71 (vide item “Indicações”).
O esquema A deve ser usado no tratamento da neoplasia1 pulmonar de células72 pequenas e não pequenas, neoplasia1 da mama73 inoperável ou recorrente e carcinoma3 de células72 esquamosas da pele74. Os esquemas A e B devem ser empregados no tratamento de neoplasia1 de cólo de útero75, neoplasia1 de ovário76, neoplasia1 gástrica recorrente ou inoperável e neoplasia1 colo2-retal (recorrente ou inoperável). O esquema C deve ser usado no tratamento de linfomas malignos (linfomas não-Hodgkin).
Esquema A: administração de 100 mg/m2 de cloridrato de irinotecano a adultos normais, uma vez por semana, por 3 a 4 semanas, por infusão intravenosa, seguida de repouso de pelo menos 2 semanas. Esse curso da terapia é então repetido.
Esquema B: administração de 150 mg/m2 de cloridrato de irinotecano a adultos normais, uma vez ao dia, a cada 2 semanas, 2 ou 3 vezes, por infusão intravenosa, seguida de repouso de pelo menos 3 semanas. Esse curso da terapia é então repetido.
Esquema C: administração de 40 mg/m2 de cloridrato de irinotecano, uma vez ao dia, por 3 dias consecutivos, por infusão intravenosa. Repetir as administrações em ciclos semanais por 2 ou 3 semanas consecutivas, seguidas de repouso de pelo menos 2 semanas. Esse curso da terapia é então repetido.
Esquemas Posológicos em Combinação
Irinotecano em Combinação com a cisplatina: o cloridrato de irinotecano foi estudado em combinação com a cisplatina para a neoplasia1 de pulmão77 de células72 pequenas e não-pequenas, neoplasia1 cervical, neoplasia1 gástrica e neoplasia1 de esôfago78. Esse regime pode ser usado no tratamento de pacientes com outros tipos de neoplasia1, exceto para a neoplasia1 colo2-retal (vide item “Indicações”).
A dose recomendada para início de tratamento é de 65 mg/m2 de cloridrato de irinotecano e 30 mg/m2 de cisplatina. Uma dose menor inicial de cloridrato de irinotecano (p.e., 50 mg/m2) pode ser considerada para pacientes68 com qualquer das seguintes condições: idade de 65 anos ou mais, radioterapia69 pélvica40/abdominal anterior, status de desempenho de 2, níveis aumentados de bilirrubina41 ou neoplasia1 gástrica. O tratamento deve ser dado em cursos repetidos a cada 6 semanas, incluindo tratamento semanal por 4 semanas, seguido de um repouso de 2 semanas.
Duração do Tratamento
Tanto para o regime de agente único como combinado, o tratamento com cursos adicionais de cloridrato de irinotecano pode ser continuado indefinidamente em pacientes que obtenham uma resposta tumoral ou em pacientes cuja neoplasia1 permaneça estável. Os pacientes devem ser cuidadosamente monitorados para toxicidade70 e devem ser retirados da terapia se ocorrer toxicidade70 inaceitável não responsiva à modificação da dose e cuidados rotineiros de suporte.
Recomendações para ajustes posológicos
A tabela a seguir descreve as modificações posológicas recomendadas durante um curso de tratamento e no início de cada curso subseqüente de tratamento para o esquema posológico como agente único. Essas recomendações baseiam-se nos efeitos tóxicos observados comumente com a administração desse produto. O tratamento programado semanal com cloridrato de irinotecano deve ser interrompido, quando ocorrem efeitos tóxicos intoleráveis ou de grau 3 ou 4. As modificações posológicas para efeitos tóxicos hematológicos que não a neutropenia17 (p.e., leucopenia18, anemia38 ou trombocitopenia39) durante uma sessão de tratamento são as mesmas recomendadas para a neutropenia17. No início de uma sessão de tratamento subseqüente, a dose do produto deve ser reduzida com base no pior grau de toxicidade70 observada na sessão prévia. Uma nova sessão de tratamento não deve ser iniciada, até que o número de granulócitos79 tenha alcançado ≥1.500/mm3 e o número de plaquetas80 tenha alcançado ≥100.000/mm3 e a diarréia15 relacionada com o tratamento tenha se resolvido completamente. O tratamento deve ser adiado por 1 a 2 semanas, para permitir a recuperação de efeitos tóxicos relacionados com o tratamento. Se o paciente não tiver se recuperado após um adiamento de 2 semanas, deve-se considerar a interrupção do tratamento com cloridrato de irinotecano. Recomenda-se que os pacientes recebam agentes antieméticos81 como pré-medicação (vide item “Precauções”).
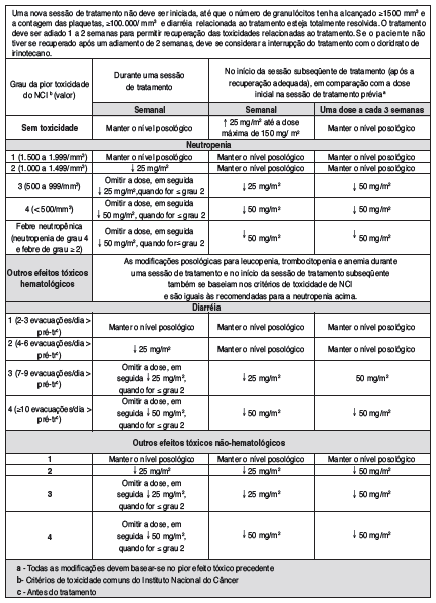
As modificações recomendadas da dose durante um curso de tratamento e no início de cada dose subseqüente de tratamento com cloridrato de irinotecano, 5-FU e folinato de cálcio estão descritas na tabela a seguir.
Modificações recomendadas da dose para esquemas combinados de irinotecano/5 – fluoruracil / folinato de cálcio:
Um novo curso de tratamento não deve ser iniciado até que a contagem dos granulócitos79 tenha alcançado ≥1500 mm3 e a contagem das plaquetas80, ≥100.000/mm3 e diarréia15 relacionada ao tratamento esteja totalmente resolvida. O tratamento deve ser adiado 1 a 2 semanas para permitir recuperação das toxicidades relacionadas ao tratamento. Se o paciente não se recuperou depois de 2 semanas, deve-se considerar a descontinuação de cloridrato de irinotecano.
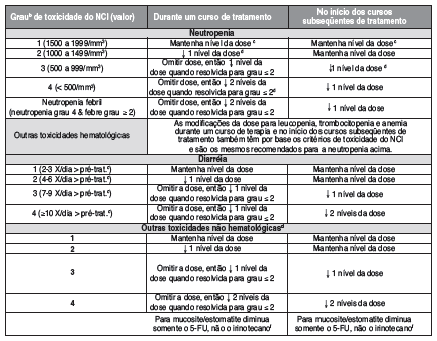
a - As modificações da dose referem-se ao 5-FU e cloridrato de irinotecano; a dose de LV permanece fixa em 20 mg/m2 (não ajustada).
b - National Cancer43 Institute Common Toxicity Criteria
c - Refere-se à dose inicial usada no curso anterior
d - Irinotecano: reduções do nível da dose = decréscimos de 25 mg/m 2 ; 5-FU: reduções do nível da dose = decréscimos de 100 mg/m 2
e - Pré-tratamento
f - Para mucosite82/estomatite12 diminua somente o 5-FU, não o cloridrato de irinotecano.
As modificações da dose recomendada para o início de cada curso da terapia com cisplatina e cloridrato de irinotecano e durante um curso de tratamento com cisplatina e cloridrato de irinotecano estão descritas nas tabelas a seguir.
Modificações da dose no início de um novo ciclo do esquema combinado de cisplatina e cloridrato de irinotecano (mg/m2) – Com base na pior toxicidade70 observada no ciclo anterior:
Um novo curso de tratamento não deve ser iniciado até que a contagem dos granulócitos79 tenha alcançado ≥ 1500 mm3 e a contagem das plaquetas80, ≥ 100.000/mm3 e diarréia15 relacionada ao tratamento esteja totalmente resolvida. O tratamento deve ser adiado 1 a 2 semanas para permitir recuperação das toxicidades relacionadas ao tratamento. Se o paciente não se recuperou depois de 2 semanas, deve-se considerar a desconstinuação de cloridrato de irinotecano.
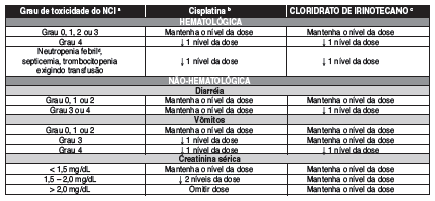
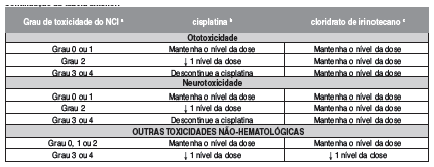
a - National Cancer43 Institute Common Toxicity Criteria
b - cisplatina: reduções do nível da dose: decréscimos de 7,5 mg/ m2
c - cloridrato de irinotecano: reduções do nível da dose: decréscimos de 10 mg/m2
d - Neutropenia17 febril é definida como na versão 2 do CTC: temperatura = 38,5°C concomitante com uma CAN < 10 x 10 9/L.
Modificações da dose durante um ciclo do esquema combinado de cisplatina e cloridrato de irinotecano (mg/m2) – Com base na pior toxicidade70 observada no ciclo anterior:
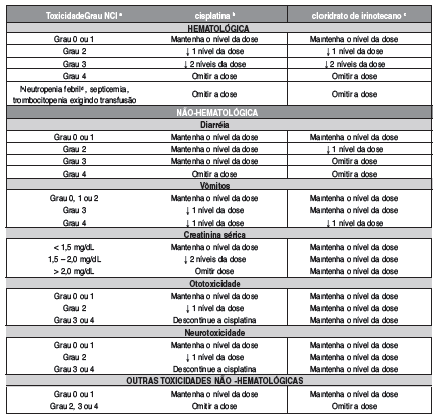
a - National Cancer43 Institute Common Toxicity Criteria
b - cisplatina: reduções do nível da dose: decréscimos de 7,5 mg/ m2
c - cloridrato de irinotecano: reduções do nível da dose: decréscimos de 10 mg/m2
d - Neutropenia17 febril é definida como na versão 2 do CTC: temperatura = 38,5 oC concomitante com uma CAN < 10 x 109/L.
Todas as modificações da dose devem ter por base a pior toxicidade70 anterior. Um novo curso de tratamento não deve ser começado até que a toxicidade70 tenha se reduzido a NCI grau 2 ou menos. O tratamento pode ser adiado por 1 a 2 semanas para permitir recuperação da toxicidade70 relacionada ao tratamento.
Se o paciente não se recuperou, deve-se considerar a descontinuação do cloridrato de irinotecano.
Precauções no Preparo e Administração:
Assim como ocorre com outros agentes antineoplásicos potencialmente tóxicos, deve-se ter cuidado no manuseio e preparo de soluções para infusão contendo cloridrato de irinotecano. Recomenda-se o uso de luvas. Caso a solução de cloridrato de irinotecano entre em contato com a pele74, lave a pele74 imediata e cuidadosamente com água e sabão.
Caso o produto entre em contato com membranas mucosas83, enxágue cuidadosamente com água. Existem várias diretrizes publicadas a respeito do manuseio e descarte de agentes antineoplásicos.
Preparo e Estabilidade da Solução para Infusão:
Deve-se inspecionar visualmente o conteúdo do frasco-ampola quanto à presença de material particulado e repetir essa inspeção84 quando da transferência da solução do frasco-ampola para a seringa85.
Cloridrato de irinotecano deve ser diluído antes da infusão. O produto deve ser diluído em soro86 glicosado a 5% USP (de preferência) ou solução injetável de cloreto de sódio a 0,9% USP, para atingir uma concentração final de 0,12 a 2,8 mg/mL.
A solução é física e quimicamente estável por até 24 horas em temperatura ambiente (aproximadamente 25°C) e em luz fluorescente ambiental. As soluções diluídas em soro86 glicosado a 5% USP, mantidas sob refrigeração (aproximadamente de 2°C a 8°C) e protegidas de luz, permanecem física e quimicamente estáveis por 48 horas. Não se recomenda a refrigeração de soluções diluídas com cloreto de sódio a 0,9% USP, devido à baixa e esporádica incidência87 de material particulado visível. Deve-se evitar o congelamento do produto e de soluções contendo cloridrato de irinotecano, uma vez que pode ocorrer precipitação da droga. Devido à possível contaminação microbiana durante a diluição, recomenda-se o uso da solução preparada dentro de 24 horas, quando mantida sob refrigeração (2°C a 8°C), ou dentro de 6 horas, caso mantida em temperatura ambiente (15°C a 30°C). Não se deve adicionar outras drogas à solução de infusão.
Cuidados especiais de manuseio e armazenamento:
O frasco-ampola de cloridrato de irinotecano é acondicionado em berço plástico, para protegê-lo contra quebras e vazamentos acidentais. O frasco-ampola deve ser inspecionado quanto a danos e sinais26 visíveis de vazamentos antes da retirada do berço. Se estiver danificado, incinere a embalagem sem abri-la.
Cloridrato de irinotecano deve ser armazenado sob temperatura ambiente (15°C a 30°C), protegido da luz. Recomenda-se que o frasco-ampola e o berço permaneçam no cartucho até o momento do uso.
- SUPERDOSAGEM:
Em estudos realizados, foram administradas doses únicas de até 750 mg/m2 de cloridrato de irinotecano. Os eventos adversos observados nesses pacientes foram semelhantes àqueles relatados com as doses e esquemas terapêuticos recomendados. Não se conhece um antídoto88 para a superdosagem do produto. Deve-se adotar medidas de suporte máximas para evitar a desidratação16 devido à diarréia15 e para tratar quaisquer complicações infecciosas.
Observou-se letalidade após doses únicas intravenosas de cloridrato de irinotecano de, aproximadamente, 111 mg/kg em camundongos e de 73 mg/kg em ratos (aproximadamente 2,6 e 3,4 vezes a dose humana recomendada de 125 mg/m2, respectivamente). A morte foi precedida de cianose89, tremores, dificuldade respiratória e convulsões.


