
REAÇÕES ADVERSAS BRATOR H
A avaliação da segurança de valsartana + hidroclorotiazida foi realizada em mais de 4.300 pacientes. As reações adversas foram, em geral, de intensidade leve e de natureza passageira.
A tabela de reações adversas abaixo está baseada em três estudos controlados que englobaram 7.616 pacientes. Destes, 4.372 pacientes receberam valsartana combinada com hidroclorotiazida. A valsartana + hidroclorotiazida apresentou incidência1 total de reações adversas ocorridas semelhante ao do placebo2.
Na tabela a seguir, estão incluídas todas as reações adversas que ocorreram no grupo que foi tratado com valsartana + hidroclorotiazida, com incidência1 igual ou superior a 1%, não dependendo de sua relação causal com a medicação do estudo.
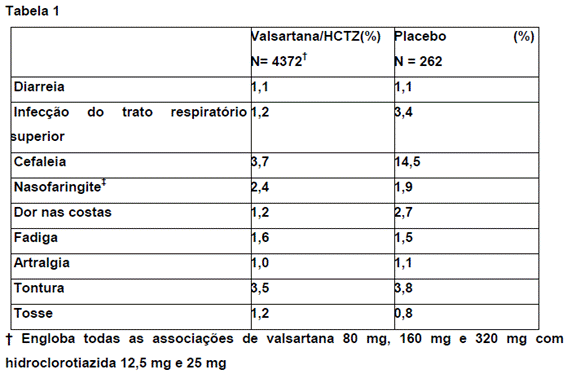
‡ Nasofaringite incluindo faringite3 + rinite4
HCTZ = hidroclorotiazida
Com frequência menor que 1%, outras reações adversas foram relatadas, incluindo: dor abdominal, dor no abdome5 superior, ansiedade, artrite6, astenia7, bronquite, bronquite aguda8, dor no peito9, tontura10 postural, dispepsia11, dispneia12, boca13 seca, disfunção erétil, gastroenterite14, hiperidrose15, hipostasia, hipocalemia16, hipotensão17, resfriado, insônia, espasmos18 musculares, tensão muscular, náusea19, congestão nasal, dor no pescoço20, edema21, edema21 periférico, otite média22, dor nas extremidades, palpitações23, parestesia24, dor faringolaríngea, poliúria25, pirexia26, congestão sinusal, sinusite27, sonolência, torção28 ligamentar, síncope29, taquicardia30, tinitus, infecção31 do trato urinário32, vertigem33, infecção31 viral, visão34 borrada e distúrbios da visão34. Não foi estabelecido se essas reações adversas têm relação causal com o tratamento.
Dados de pós-comercialização demonstraram casos muito raros de prurido35, erupção36 cutânea37, edema angioneurótico38, outras reações de hipersensibilidade alérgicas, incluindo vasculite39 e doença do soro40. Casos muito raros de mialgia41 e insuficiência renal42, também foram observados, e vários casos de edema pulmonar43 induzido por hidroclorotiazida com infiltração granulocítica e deposição de IgG nas membranas alveolares.
Uma reação idiossincrática rara mediada imunologicamente pela hidroclorotiazida pode ser o edema pulmonar43 não cardiogênico.
Dados laboratoriais
Foi observada uma redução superior a 20% no potássio sérico em 3,7% dos pacientes que receberam com valsartana + hidroclorotiazida, ao se comparar com o placebo2 ( 3,1%) (vide “Advertências e Precauções”).
Nos estudos clínicos controlados, o aumento da creatinina44 e ureia45 nitrogenada sanguínea (UNS) ocorreu em 0,4% e 6,3% respectivamente em pacientes que receberam placebo2 e em 1,9% e 14,7% respectivamente dos pacientes que receberam valsartana + hidroclorotiazida.
Em 0,1% dos pacientes tratados com valsartana + hidroclorotiazida versus 0,4% dos pacientes tratados com placebo2 foi observada neutropenia46.
Valsartana
Em estudos clínicos com pacientes apenas utilizando valsartana, outras reações adversas foram relatadas, independente de sua relação causal com o medicamento:
Com frequência inferior a 1%: insuficiência renal42 aguda, aumento ocasional nos valores da função hepática47 e diminuição da libido48.
Hidroclorotiazida
Ao passar dos anos a hidroclorotiazida tem sido muito prescrita, frequentemente em doses maiores à contida em valsartana + hidroclorotiazida. Em pacientes tratados com diuréticos49 tiazídicos, em monoterapia, inclusive hidroclorotiazida, houve relatos das seguintes reações adversas: Distúrbios metabólicos e eletrolíticos (vide “Advertências e Precauções”).
Outras
Comuns: náusea19 leve e vômitos50, diminuição do apetite, hipotensão17 ortostática, que pode ser agravada pelo uso de anestésicos, sedativos ou álcool, disfunção erétil e urticária51 e outras formas de erupção36 cutânea37.
Raras: distúrbios da visão34, colestase52 ou icterícia53, desconforto abdominal, cefaleia54, depressão, doenças do sono, reação de fotossensibilidade, diarreia55, parestesia24, arritmia56, constipação57, trombocitopenia58, algumas vezes acompanhada de púrpura59 e tonturas60.
Muito raras: reações cutâneas61 semelhantes ao lúpus62 eritematoso63, anemia hemolítica64, pancreatite65, agranulocitose66, reação de hipersensibilidade, depressão medular, necrólise epidérmica tóxica67, reativação do lúpus62 eritematoso63 cutâneo68, vasculite39 necrotizante, distúrbios respiratórios, inclusive pneumonite69 e edema pulmonar43 e leucopenia70.
Pneumonia71 intersticial72: sintomas73 associados à pneumonia71 intersticial72, tais como febre74, tosse, dispnéia12 e anormalidades radiográficas torácicas podem ocorrer com o uso de valsartana. Se tais sintomas73 forem observados após o tratamento com a valsartana, o medicamento deve ser descontinuado e devem ser iniciadas medidas apropriadas, como a administração de hormônios adrenocorticosteróides.
Em caso de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br, ou para a Vigilância Sanitária Estadual ou Municipal.


