
EFEITOS DE OUTRAS DROGAS ANTIEPILÉPTICAS SOBRE TOPIRAMATO
TOPIRAMATO
A FENITOÍNA E A CARBAMAZEPINA DIMINUEM AS CONCENTRAÇÕES PLASMÁTICAS DO TOPIRAMATO A ADIÇÃO OU DESCONTINUAÇÃO DA FENITOÍNA OU DA CARBAMAZEPINA AO TRATAMENTO COM TOPIRAMATO PODERÁ REQUERER UM AJUSTE DE DOSE DESTE ÚLTIMO. O TATEAMENTO DA DOSE DEVERÁ SER REALIZADO DE ACORDO COM O EFEITO CLÍNICO.
TANTO A ADIÇÃO QUANTO A RETIRADA DO ÁCIDO VALPRÓICO NÃO PRODUZEM MUDANÇAS CLINICAMENTE SIGNIFICATIVAS NAS CONCENTRAÇÕES PLASMÁTICAS DE TOPIRAMATO E, PORTANTO, NÃO EXIGEM AJUSTE DA DOSE DO TOPIRAMATO. OS RESULTADOS DESTAS INTERAÇÕES ESTÃO RESUMIDOS NA TABELA A SEGUIR.
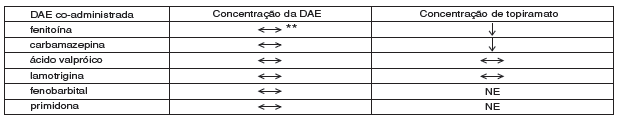
<-> = sem efeito sobre as concentrações plasmáticas
** = concentrações plasmática aumentadas em alguns pacientes
= diminuição das concentrações plámaticas
NE = não estudado
DAE = droga antiepilética
- OUTRAS INTERAÇÕES MEDICAMENTOSAS
DIGOXINA: EM UM ESTUDO DE DOSE ÚNICA, A ADMINISTRAÇÃO CONCOMITANTE DE TOPIRAMATO PROVOCOU UMA REDUÇÃO DE 12% NA ÁREA SOB A CURVA DE CONCENTRAÇÃO PLASMÁTICA (AUC1) DA DIGOXINA. A IMPORTÂNCIA CLÍNICA DESTA OBSERVAÇÃO NÃO FOI DETERMINADA. QUANDO O TOPIRAMATO FOR ASSOCIADO OU DESCONTINUADO EM PACIENTES SUBMETIDOS A TRATAMENTO COM A DIGOXINA, RECOMENDA-SE ATENÇÃO À MONITORAÇÃO ROTINEIRA E CUIDADOSA DAS CONCENTRAÇÕES SÉRICAS DE DIGOXINA.
DEPRESSORES DO SNC2/ÁLCOOL: RECOMENDA-SE QUE TOPIRAMATO NÃO SEJA UTILIZADO CONCOMITANTEMENTE COM BEBIDAS ALCOÓLICAS OU COM OUTROS MEDICAMENTOS DEPRESSORES DO SNC2, POIS PODE OCORRER UM AUMENTO DA AÇÃO DE TOPIRAMATO.
ANTICONCEPCIONAIS ORAIS: EM UM ESTUDO DE INTERAÇÃO FARMACOCINÉTICA EM VOLUNTÁRIAS SADIAS, COM ADMINISTRAÇÃO CONCOMITANTE DE CONTRACEPTIVO ORAL COMBINADO CONTENDO 1 MG DE NORETINDRONA E 35 MCG DE ETINILESTRADIOL, TOPIRAMATO ADMINISTRADO ISOLADAMENTE NAS DOSES DE 50 A 200 MG/DIA, NÃO FOI ASSOCIADO A ALTERAÇÕES ESTATISTICAMENTE SIGNIFICANTES NA EXPOSIÇÃO MÉDIA (AUC1) AOS COMPONENTES DO CONTRACEPTIVO ORAL. EM OUTRO ESTUDO, A EXPOSIÇÃO AO ETINILESTRADIOL APRESENTOU REDUÇÃO ESTATISTICAMENTE SIGNIFICANTE COM DOSES DE 200, 400 E 800 MG/DIA (18%, 21% E 30% RESPECTIVAMENTE) QUANDO ADMINISTRADO COMO ADJUVANTE EM PACIENTES EM USO DE ÁCIDO VALPRÓICO. EM AMBOS OS ESTUDOS, TOPIRAMATO (50 MG/DIA A 800 MG/DIA) NÃO AFETOU SIGNIFICANTEMENTE A EXPOSIÇÃO À NORETINDRONA.
ENTRETANTO, NAS DOSES ENTRE 200-800 MG/DIA, HOUVE UMA REDUÇÃO DOSE-DEPENDENTE NA EXPOSIÇÃO AO ETINILESTRADIOL E, NAS DOSES DE 50-200 MG/DIA, NÃO HOUVE ALTERAÇÃO SIGNIFICANTE DOSE DEPENDENTE NA EXPOSIÇÃO AO ETINILESTRADIOL.
A SIGNIFICÂNCIA CLÍNICA DAS ALTERAÇÕES OBSERVADAS NÃO É CONHECIDA. A POSSIBILIDADE DE REDUÇÃO DA EFICÁCIA DO CONTRACEPTIVO E AUMENTO NO SANGRAMENTO DE ESCAPE DEVE SER CONSIDERADA EM PACIENTES EM USO DE CONTRACEPTIVOS ORAIS COMBINADOS E TOPIRAMATO. DEVESE SOLICITAR A PACIENTES EM USO DE CONTRACEPTIVOS ORAIS QUE RELATEM QUALQUER ALTERAÇÃO EM SEUS PADRÕES MENSTRUAIS. A EFICÁCIA CONTRACEPTIVA PODE SER REDUZIDA, MESMO NA AUSÊNCIA DE SANGRAMENTO DE ESCAPE.
LÍTIO: EM VOLUNTÁRIOS SAUDÁVEIS, FOI OBSERVADA UMA REDUÇÃO (18% PARA AUC1) NA EXPOSIÇÃO SISTEMÁTICA PARA O LÍTIO DURANTE A ADMINISTRAÇÃO CONCOMITANTE COM TOPIRAMATO 200 MG/DIA. NOS PACIENTES COM TRANSTORNO BIPOLAR, A FARMACOCINÉTICA DO LÍTIO NÃO FOI AFETADA DURANTE O TRATAMENTO COM TOPIRAMATO EM DOSES DE 200 MG/DIA; ENTRETANTO, FOI OBSERVADO AUMENTO NA EXPOSIÇÃO SISTÊMICA (26% PARA AUC1) DEPOIS DE DOSES DO TOPIRAMATO DE ATÉ 600 MG/DIA. OS NÍVEIS DO LÍTIO DEVEM SER MONITORADOS QUANDO CO-ADMINISTRADOS COM TOPIRAMATO.
RISPERIDONA: OS ESTUDOS DE INTERAÇÃO DROGA-DROGA CONDUZIDOS SOB CONDIÇÕES DE DOSE ÚNICA E MÚLTIPLA EM VOLUNTÁRIOS SAUDÁVEIS E EM PACIENTES COMTRANSTORNO BIPOLAR ATINGIRAM RESULTADOS SIMILARES. QUANDO ADMINISTRADO CONCOMITANTEMENTE COM TOPIRAMATO EM DOSES ESCALADAS DE 100, 250 E 400 MG/DIA HOUVE UMA REDUÇÃO DA RISPERIDONA (ADMINISTRADA EM DOSES QUE VARIANDO DE 1 A 6 MG/DIA) NA EXPOSIÇÃO SISTÊMICA (16% E 33% PARA AUC1 NO ESTADO DE EQUILÍBRIO NAS 250 E 400 DOSES DE MG/DIA, RESPECTIVAMENTE). ALTERAÇÕES MÍNIMAS NA FARMACOCINÉTICA DO TOTAL DE PARTES ATIVAS (RISPERIDONA MAIS 9-HIDROXIRISPERIDONA) E NENHUMA ALTERAÇÃO PARA 9-HIDROXIRISPERIDONA FOI OBSERVADA. NÃO HOUVE MUDANÇA CLÍNICA SIGNIFICATIVAMENTE NA EXPOSIÇÃO SISTEMICA DO TOTAL DE PARTES ATIVAS DA RISPERIDONA OU DO TOPIRAMATO, PORTANTO ESTA INTERAÇÃO NÃO É PROVÁVEL SER DE SIGNIFICÂNCIA CLÍNICA.
HIDROCLOROTIAZIDA: UM ESTUDO DE INTERAÇÃO MEDICAMENTOSA CONDUZIDO EM VOLUNTÁRIOS SADIOS AVALIOU A FARMACOCINÉTICA NO ESTADO ESTACIONÁRIO DA
HIDROCLOROTIAZIDA (25 MG A CADA 24H) E DO TOPIRAMATO (96 MG A CADA 12H) QUANDO ADMINISTRADOS ISOLADA OU CONCOMITANTEMENTE. OS RESULTADOS DESTE ESTUDO INDICARAM QUE A Cmáx DO TOPIRAMATO AUMENTOU 27% E A AUC1 AUMENTOU 29% QUANDO A HIDROCLOROTIAZIDA FOI ASSOCIADA AO TOPIRAMATO. A SIGNIFICÂNCIA CLÍNICA DESTA ALTERAÇÃO É DESCONHECIDA. A ASSOCIAÇÃO DE HIDROCLOROTIAZIDA AO TRATAMENTO COM TOPIRAMATO PODE PRECISAR DE UM AJUSTE DA DOSE DO TOPIRAMATO. A FARMACOCINÉTICA DA HIDROCLOROTIAZIDA NO ESTADO ESTACIONÁRIO NÃO FOI INFLUENCIADA SIGNIFICATIVAMENTE PELA ADMINISTRAÇÃO CONCOMITANTE DO TOPIRAMATO. OS RESULTADOS LABORATORIAIS CLÍNICOS INDICARAM REDUÇÃO NO POTÁSSIO SÉRICO APÓS ADMINISTRAÇÃO DO TOPIRAMATO OU DA HIDROCLOROTIAZIDA, SENDO MAIOR QUANDO A HIDROCLOROTIAZIDA E O TOPIRAMATO FORAM ADMINISTRADOS EM COMBINAÇÃO.
METFORMINA3: UM ESTUDO DE INTERAÇÃO MEDICAMENTOSA CONDUZIDO EM VOLUNTÁRIOS SADIOS AVALIOU A FARMACOCINÉTICA DA METFORMINA3 E DO TOPIRAMATO NO ESTADO DE EQUILÍBRIO NO PLASMA4 QUANDO A METFORMINA3 FOI ADMINISTRADA ISOLADA E QUANDO A METFORMINA3 E O TOPIRAMATO FORAM ADMINISTRADOS SIMULTANEAMENTE. OS RESULTADOS DO ESTUDO INDICARAM QUE A Cmáx MÉDIA E A AUC0-12 h MÉDIA DA METFORMINA3 AUMENTARAM EM 18% E 25%, RESPECTIVAMENTE, ENQUANTO QUE O “CLEARANCE” MÉDIO DIMINUIU 20% QUANDO A METFORMINA3 FOI CO-ADMINISTRADA COM TOPIRAMATO. O TOPIRAMATO NÃO AFETA O Tmáx DA METFORMINA3. A SIGNIFICÂNCIA CLÍNICA DO EFEITO DO TOPIRAMATO NA FARMACOCINÉTICA DA METFORMINA3 NÃO ESTÁ CLARA. O “CLEARANCE” PLASMÁTICO ORAL DO TOPIRAMATO PARECE SER REDUZIDO QUANDO ADMINISTRADO COM METFORMINA3. A EXTENSÃO DA ALTERAÇÃO NO “CLEARANCE” É DESCONHECIDA. A SIGNIFICÂNCIA CLÍNICA DO EFEITO DA METFORMINA3 NA FARMACOCINÉTICA DO TOPIRAMATO NÃO ESTÁ CLARA. QUANDO TOPIRAMATO É ADMINISTRADO OU RETIRADO EM PACIENTES TRATADOS COM METFORMINA3, DEVE-SE TER ESPECIAL ATENÇÃO NA MONITORIZAÇÃO ROTINEIRA PARA UM CONTROLE ADEQUADO DO DIABETES5.
PIOGLITAZONA: UM ESTUDO DE INTERAÇÃO MEDICAMENTOSA CONDUZIDO EM VOLUNTÁRIOS SADIOS AVALIOU A FARMACOCINÉTICA NO ESTADO ESTACIONÁRIO DO TOPIRAMATO E DA PIOGLITAZONA QUANDO ADMINISTRADOS ISOLADA OU CONCOMITANTEMENTE. UMA REDUÇÃO DE 15% NA AUCt, SS DE PIOGLITAZONA SEM ALTERAÇÃO NA Cmáx , SS FOI OBSERVADA. ESTE ACHADO NÃO FOI ESTATISTICAMENTE SIGNIFICANTE. ALÉM DISSO, REDUÇÕES DE 13% NA Cmáx , SS E DE 16% NA AUCt, SS DO HIDRÓXIMETABÓLITO ATIVO FORAM OBSERVADAS, ASSIM
COMO UMA REDUÇÃO DE 60% TANTO NA Cmáx , SS COMO NA AUCt, SS DO CETO-METABÓLITO6 ATIVO FORAM OBSERVADAS. A SIGNIFICÂNCIA CLÍNICA DESTES ACHADOS É DESCONHECIDA.
QUANDO TOPIRAMATO É ASSOCIADO AO TRATAMENTO COM PIOGLITAZONA OU PIOGLITAZONA É ASSOCIADA AO TRATAMENTO COM TOPIRAMATO, DEVE-SE TER ATENÇÃO ESPECIAL À ROTINA DE MONITORAMENTO DOS PACIENTES PARA UM CONTROLE ADEQUADO DO ESTADO DIABÉTICO.
GLIBURIDA: UM ESTUDO DE INTERAÇÃO DROGA-DROGA CONDUZIDOS NOS PACIENTES COM DIABETES TIPO 27 AVALIOU A FARMACOCINÉTICA NO ESTADO DE EQUILÍBRIO DA GLIBURIDA (5MG/DIA) ISOLADA E CONCOMITANTEMENTE COM TOPIRAMATO (150 MG/DIA). HOUVE UMA REDUÇÃO DE 25% NA AUC24 DA GLIBURIDA DURANTE A ADMINISTRAÇÃO DO TOPIRAMATO. A EXPOSIÇÃO SISTEMICA DOS METABOLITOS8 ATIVOS, 4-TRANS-HIDROXI-GLIBURIDA (M1) E 3-CIS-HIDROXIGLIBURIDA (M2), TAMBÉM FORAM REDUZIDAS EM 13% E 15%, RESPECTIVAMENTE.
A FARMACOCINÉTICA NO ESTADO DE EQUILÍBRIO DO TOPIRAMATO NÃO FOI AFETADA PELA ADMINISTRAÇÃO CONCOMITANTE DA GLIBURIDA. QUANDO O TOPIRAMATO É ADICIONADO A TERAPIA DA GLIBURIDA OU A GLIBURIDA É ADICIONADA A TERAPIA DO TOPIRAMATO, DEVE SER FEITA UMA ROTINA DE MONITORIZAÇÃO CUIDADOSA DOS PACIENTES PARA O CONTROLE ADEQUADO DO ESTADO DA SUA DOENÇA DIABÉTICA.


