
INDICAÇÕES PACLITAXEL
Carcinoma1 de Ovário¹
- Terapia de primeira linha em combinação com um composto de platina para o tratamento do carcinoma1 avançado de ovário2.
- Terapia de segunda linha para o tratamento do carcinoma1 avançado de ovário2.
Câncer3 de Mama²
- Tratamento adjuvante do câncer3 de mama4 linfonodo5 positivo, administrado em sequência a uma terapia padrão combinada.
- Tratamento de primeira linha após recidiva6 da doença dentro de 6 meses de terapia adjuvante. A terapia anterior deve incluir uma antraciclina, a menos que clinicamente contraindicada.
- Terapia de primeira linha em câncer3 avançado ou metastático de mama4, em combinação com trastuzumabe, em pacientes com super expressão do HER-2 em níveis de 2+ e 3+ como determinado por imuno-histoquímica.
- Terapia de segunda linha após falha da quimioterapia7 combinada para doença metastática8. A terapia anterior deve incluir uma antraciclina, a menos que clinicamente contraindicada.
Câncer3 de Não-pequenas Células9 do Pulmão³
- Tratamento de primeira linha em combinação com um composto de platina ou como agente único para o tratamento do câncer3 de não-pequenas células9 do pulmão10 em pacientes que não são candidatos a cirurgia e/ou radioterapia11 com potencial de cura.
Sarcoma12 de Kapósi
- Tratamento de segunda linha no sarcoma12 de Kapósi relacionado à AIDS4.
1 CID C56 – Neoplasia13 maligna do ovário2.
2 CID C50 – Neoplasia13 maligna da mama4.
3 CID C34 – Neoplasia13 maligna dos brônquios14 e dos pulmões15.
4 CID B21.0 – Doença pelo HIV16 resultando em sarcoma12 de Kapósi.
- 2. RESULTADOS DE EFICÁCIA
Carcinoma1 de ovário2
- Terapia de primeira linha: A segurança e eficácia do paclitaxel acompanhado por cisplatina em pacientes com carcinoma1 de ovário2 avançado e sem quimioterapia7 prévia foram avaliadas em 2 estudos FASE III multicêntricos, randomizados e controlados. Em um estudo do INTERGRUPO conduzido pela Organização Europeia de Pesquisa e Tratamento de Câncer3 que envolvem o Grupo Escandinavo NOCOVA, o Instituto Nacional de Câncer3 do Canadá e o Grupo Escocês, 680 pacientes com estágio da doença IIB–C, III, ou IV (ressecção ampla ótima ou não ótima) receberam infusão de paclitaxel 175 mg/m² em um período de 3 horas seguida por cisplatina 75 mg/m² (Tc) ou ciclofosfamida 750 mg/m² seguidos por cisplatina 75 mg/m² (Cc) por uma mediana de seis ciclos.
Embora o protocolo permitisse uma terapia adicional, somente 15% dos pacientes receberam ambas as drogas por nove ou mais ciclos. Em um estudo conduzido pelo Grupo de Oncologia Ginecológica (GOG), 410 pacientes com Estágio III ou IV da doença (> 1 cm de doença residual após laparotomia17 para estadiamento ou metástase18 à distância) receberam infusão de paclitaxel 135 mg/m² num período de 24 horas seguido por cisplatina 75 mg/m² ou, senão ciclofosfamida 750 mg/m² seguido por cisplatina 75 mg/m² por 6 ciclos.
Em ambos os estudos, pacientes tratados com paclitaxel em combinação com cisplatina tiveram uma taxa de resposta significativamente maior, um tempo maior para progressão e um tempo de sobrevida19 maior, comparado com a terapia padrão.
Estas diferenças também foram significativas para o subgrupo de pacientes no estudo do Intergrupo com doença não otimamente ressecada, embora o estudo não tenha sido totalmente capacitado para análise de subgrupo (Tabelas 1 e 2).
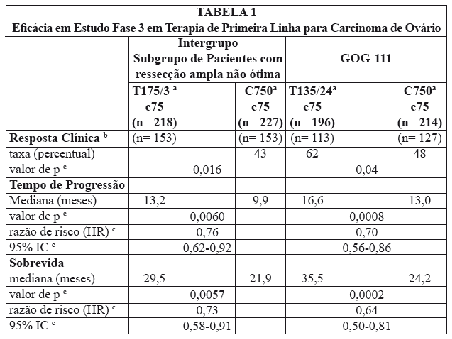
a - Dose de paclitaxel em mg/m²/duração da infusão em horas; Doses de ciclofosfamida e cisplatina em mg/m²
b - Pacientes apenas com doenças mensuráveis
c - Não estratificado para o Estudo do Intergrupo, Estratificado para Estudo GOG-111.
HR – Do inglês Hazard Ratio
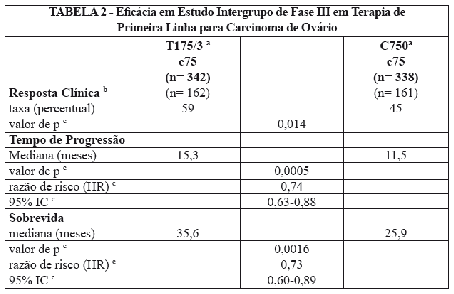
a - Dose de paclitaxel em mg/m²/duração da infusão em horas; Doses de ciclofosfamida e cisplatina em mg/m²
b - Pacientes apenas com doenças mensuráveis
c - Não estratificado
O perfil de eventos adversos para os pacientes que receberam paclitaxel, em combinação com cisplatina nestes estudos, foi qualitativamente consistente com o que foi observado na análise dos dados dos 812 pacientes tratados unicamente com paclitaxel em 10 estudos clínicos.
- Terapia de segunda linha: Dados de cinco estudos clínicos fase I e II (189 pacientes), um estudo de FASE III multicêntrico, randomizado20 (407 pacientes), assim como a análise dos dados de mais de 300 pacientes envolvidos em um programa de tratamento de um centro de referência foram usados para sustentar o uso de paclitaxel nos pacientes que tiveram falha inicial ou subsequente da quimioterapia7 para carcinoma1 de ovário2 metastático. Dois dos estudos FASE II (92 pacientes) utilizaram uma dose inicial de 135 a 170 mg/m2 na maioria dos
pacientes (> 90%), que receberam infusão contínua num período de 24 horas. As taxas de resposta destes dois estudos foram 22% (lC de 95%: 11 a 37%) e 30% (lC de 95%: 18 a 46%) com um total de 6 respostas completas e 18 parciais em 92 pacientes. A duração mediana da resposta global nestes dois estudos medidos no primeiro dia do tratamento foi de 7,2 meses (faixa: 3,5-15,8 meses) e 7,5 meses (faixa: 5,3-17,4 meses), respectivamente. A sobrevida19 mediana foi de 8,1 meses (faixa: 0,2-36,7 meses) e 15,9 meses (faixa: 1,8-34,5+ meses).
O estudo de FASE III teve um desenho bi-fatorial e comparou a eficácia e segurança do paclitaxel, administrado em 2 diferentes doses (135 ou 175 mg/m2) e programações (3 ou 24 horas de infusão).
A taxa de resposta global para 407 pacientes foi 16,2% (95% lC: 12,8 a 20,2%), com 6 respostas completas e 60 respostas parciais. A duração da resposta medida no primeiro dia de tratamento foi de 8,3 meses (faixa: 3,2-21,6 meses). O tempo mediano da progressão foi de 3,7 meses (faixa: 0,1+- 25,1+ meses). A sobrevida19 mediana foi de 11,5 meses (faixa: 0,2-26,3+ meses). As taxas de resposta, a sobrevida19 mediana e o tempo mediano de progressão para os 4 braços estão na tabela a seguir.
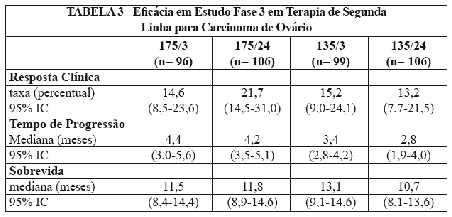
Análises foram realizadas conforme planejado no desenho do estudo bi-fatorial descrito no protocolo, comparando as duas doses (135 ou 175 mg/m²), independentemente do esquema (3 ou 24 horas) e os dois esquemas independentemente da dose.
Os pacientes que receberam a dose de 175 mg/m² tiveram uma taxa de resposta similar aos que receberam a dose de 135 mg/m² 18% vs. 14% (p=0,28). Não foi detectada nenhuma diferença na taxa de resposta quando comparado o período de infusão de 3 horas com o período de 24 horas: 15% vs. 17% (p=0,50).
Pacientes que receberam a dose de 175 mg/m² de paclitaxel tiveram um maior tempo de progressão do que aqueles que receberam a dose de 135 mg/m² de paclitaxel: mediana de 4,2 contra 3,1 meses (p= 0,03). O tempo mediano de progressão para os pacientes que receberam infusão de 3 horas contra 24 horas foi de 4,0 meses contra 3,7 meses, respectivamente. A sobrevida19 mediana foi de 11,6 meses em pacientes que receberam dose de 175 mg/m² de paclitaxel e 11,0 meses em pacientes que receberam a dose de 135 mg/m² (p=0,92). A sobrevida19 mediana foi de 11,7 meses em pacientes que receberam infusão de paclitaxel em um período de 3 horas de infusão e 11,2 meses em pacientes que receberam infusão em um período de 24 horas (p=0,91). Estas análises estatísticas devem ser vistas com cautela devido às múltiplas comparações realizadas.
Paclitaxel permaneceu eficaz em pacientes que desenvolveram resistência à terapia com platina (definido como tumor21 progressivo ou reincidência22 do tumor21 dentro de 6 meses após conclusão de terapia com platina), com taxas de respostas de 14% na FASE III e 31% nas Fases I e II dos estudos clínicos.
O perfil dos eventos adversos neste estudo FASE III foi consistente com aquele observado na análise de dados dos 812 pacientes tratados em 10 estudos clínicos.
Os resultados deste estudo randomizado23 suportam o uso de paclitaxel nas doses de 135 a 175 mg/m², administrados por infusão intravenosa num período de 3 horas.
Estas doses administradas por infusão num período de 24 horas demonstraram maior toxicidade24. Entretanto, o estudo não tinha poder suficiente para determinar se uma determinada dose e esquema produziram eficácia superior.
Câncer3 de mama4


