
RESULTADOS DE EFICÁCIA ONGLYZA
ONGLYZA foi estudado como monoterapia e em combinação com metformina1, glibenclamida e as tiazolidinedionas: pioglitazona e rosiglitazona.
Um total de 4148 pacientes com diabetes2 do tipo 2 foram randomizados, em seis estudos duplo-cego conduzidos para avaliar a segurança e a eficácia glicêmica de ONGLYZA. Um total de 3021 indivíduos desses estudos foi tratado com ONGLYZA. Nestes estudos, a média de idade dos pacientes foi de 54 anos, e 71% dos pacientes eram brancos, 16% eram asiáticos, 4% eram negros, e 9% eram de outros grupos raciais. Um adicional de 423 pacientes, incluindo 315 que receberam ONGLYZA, participaram de um estudo placebo3 controlado, variando a dose de 6 a 12 semanas de duração.
Nestes seis estudos duplo-cego, ONGLYZA foi avaliado em doses de 2,5 mg e 5 mg uma vez por dia. Em três desses estudos também foi avaliada a dose única de 10 mg ao dia. A dose diária de 10 mg de saxagliptina não forneceu maior eficácia do que a dose diária de 5 mg. O tratamento com ONGLYZA produziu em todas as doses clinicamente relevantes melhorias estatisticamente significativas na hemoglobina4 A1c5 (A1C5), na glicemia de jejum6 do plasma7 (FPG), e na glicemia pós-prandial8 (PPG), 2 horas PPG que seguem o teste de tolerância glicemia9 oral (OGTT), comparadas ao grupo controle.
Reduções em A1C5 foram observadas através dos subgrupos que incluíram o gênero, a idade, a raça e o índice de massa corporal10 (IMC11) inicial.
ONGLYZA não está associado a grandes alterações no peso ou índice de lipídeos no plasma7 no jejum quando comparados ao placebo3.
ONGLYZA foi avaliado em dois estudos adicionais em pacientes com diabetes2: um estudo ativo-controlado comparando terapia com ONGLYZA adjuvante à glipizida12 em 858 pacientes inadequadamente controlados com metformina1 isolada, e um estudo placebo3-controlado comparando ONGLYZA a placebo3 em 170 pacientes com diabetes tipo 213 e insuficiência renal14 moderada ou grave, ou doença renal15 em estágio terminal (ESRD).
Monoterapia
Um total de 766 pacientes virgens de tratamento do diabetes tipo 213 inadequadamente controlados com dieta e exercícios (A1C5 ≥7% a ≤10%) participaram de dois estudos duplocego, controlados com placebo3 de 24 semanas de duração para avaliar a eficácia e a segurança da monoterapia com ONGLYZA.
No primeiro estudo, depois de um estudo único-cego de 2 semanas, de dieta, exercício e um período inicial com placebo3, os 401 pacientes foram randomizados para os grupos de ONGLYZA 2,5 mg, 5 mg ou 10 mg ou placebo3. Os pacientes que não conseguiram cumprir metas glicêmicas específicas durante o estudo foram tratados com a terapia de resgate com metformina1, adicionada ao grupo placebo3 ou ao grupo ONGLYZA. A eficácia foi avaliada na última medição antes da terapia de resgate para os pacientes que precisaram desta. A titulação de dose de ONGLYZA não foi permitida neste estudo.
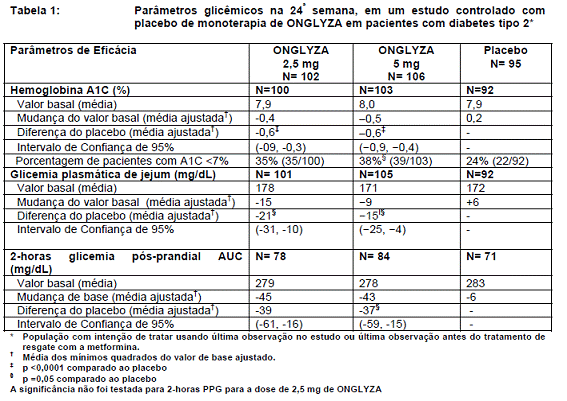
O tratamento com ONGLYZA 2,5 mg e 5 mg por dia, proporcionou melhorias significativas na A1C5, FPG, e PPG em comparação com o placebo3 (Tabela 1). A proporção de pacientes que descontinuaram o tratamento por falta de controle glicêmico ou que receberam terapia de resgate para obter a glicemia9 pré-especificada foi 16% no grupo ONGLYZA 2,5 mg, 20% no grupo ONGLYZA, 5 mg e 26% no grupo placebo3.
Um segundo estudo de 24 semanas de monoterapia foi realizado para avaliar uma escala de regimes posológicos de ONGLYZA. Os pacientes virgens de tratamento com diabetes2 inadequadamente controlada (≥ 7% ≤10% de A1C5) submeteram-se a um estudo único-cego de 2 semanas, de dieta e exercícios em um período inicial com placebo3. Um total de 365 pacientes foram randomizados para receber as dosagens de 2,5 mg todas as manhãs, 5 mg todas as manhãs, 2,5 mg todas as manhãs com possibilidade de titulação de dose para 5 mg todas as manhãs, 5 mg todas as noites ou placebo3. Pacientes que não obtiveram a glicemia9 desejada foram tratados com terapia de metformina1 de resgate adicionados ao placebo3 ou ONGLYZA, o número de pacientes randomizados por grupo de tratamento variou de 71 a 74.
O tratamento com ONGLYZA 5 mg a cada manhã ou 5 mg a cada noite forneceu melhorias significativas em A1C5 contra o placebo3 (redução média placebo3-corrigida de - 0.4% e -0.3%, respectivamente). O tratamento com ONGLYZA 2,5 mg a cada manhã também forneceu melhorias significativas em A1C5 contra o placebo3 (redução média placebo3-corrigida de - 0.4%).
Terapia em combinação
Terapia combinada16 em adição a metformina1
Um total de 743 pacientes com diabetes tipo 213 participaram de estudo randomizado17, duplocego, placebo3-controlado, de duração de 24 semanas, para avaliar a eficácia e segurança de ONGLYZA em combinação com metformina1 em pacientes com controle glicêmico inadequado (A1C5 ≥7% e ≤10%) com metformina1 sozinha. Foi exigido que os pacientes estivessem utilizando uma dose estável de metformina1 (1500 mg para 2550 mg diariamente) durante, pelo menos, 8 semanas, para então serem adicionados a este estudo.
Pacientes que obedeceram aos critérios de elegibilidade foram incluídos em um período únicocego, de duas-semanas, com dieta e exercício, e início com placebo3 durante o qual os pacientes receberam metformina1 na dose de pré-estudo deles, até 2500 mg diariamente. Após o período inicial, os pacientes elegíveis foram randomizados a 2,5 mg, 5 mg, ou 10 mg de ONGLYZA ou placebo3, em adição à dose atual de metformina1 aberta. Pacientes que não obtiveram a glicemia9 desejada durante o estudo foram tratados com pioglitazona como terapia de resgate, adicionadasàs medições do estudo. Titulações de dose de ONGLYZA e de metformina1 não foram permitidas neste estudo.
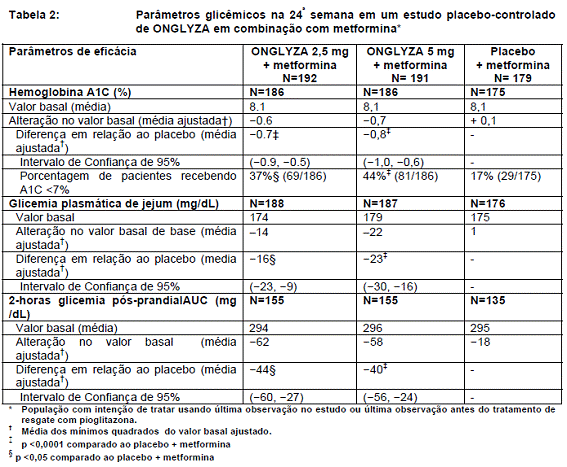
Em combinação com a metformina1, ONGLYZA 2,5 mg e 5 mg promoveu melhoras significativas em A1C5, FPG, e PPG comparados com o grupo placebo3 mais metformina1 (Tabela 2). Alterações médias desde o início para A1C5 ao longo do tempo e na avaliação são mostrados na Figura 1. A proporção de pacientes que interromperam o tratamento por falta de controle glicêmico, ou que foram resgatadas para atender os critérios glicêmicos pré-especificados foi de 15% para a dose de ONGLYZA 2,5 mg adicionada à metformina1, 13% para o grupo de ONGLYZA 5 mg adicionada à metformina1, e 27% no grupo placebo3 adicionada à metformina1.

Um total de 565 pacientes com diabetes tipo 213 participaram deste estudo randomizado17, duplocego, placebo3-controlado de duração de 24 semanas, para avaliar a eficácia e segurança de ONGLYZA em combinação com uma tiazolidinediona (TZD) em pacientes com controle glicêmico inadequado (A1C5 ≥7% a ≤10.5%) com TZD sozinha. Foi exigido que os pacientes estivessem fazendo uso de uma dose estável de pioglitazona (30 mg-45 mg uma vez ao dia) ou rosiglitazona (4 mg uma vez ao dia ou 8 mg ou uma vez ao dia ou em duas doses divididas de 4 mg) durante pelo menos 12 semanas para, então serem incluídos neste estudo.
Pacientes que obedeceram aos critérios de elegibilidade foram incluídos em um período únicocego, de duas-semanas, com dieta e exercício e início com placebo3, durante o qual os pacientes receberam TZD na dose de pré-estudo deles. Após o período inicial, os pacientes elegíveis foram randomizados a 2,5 mg, 5 mg de ONGLYZA ou placebo3, em adição à dose atual de TZD. Pacientes que não obtiveram a glicemia9 desejada durante o estudo foram tratados com metformina1 como terapia de resgate, adicionados ao placebo3 ou ONGLYZA mais TZD. Titulações de dose de ONGLYZA e de TZD não foram permitidas neste estudo. Uma mudança no regime terapêutico de TZD de rosiglitazona para pioglitazona com doses terapêuticas equivalentes e especificadas foram permitidas à discrição do investigador caso o mesmo acreditasse ser clinicamente apropriado.
Em combinação com TZD, ONGLYZA 2,5 mg e 5 mg promoveu melhorias significativas em A1C5, FPG, e PPG comparados com o grupo placebo3 mais TZD (Tabela 3). A proporção de pacientes que descontinuaram por falta de controle glicêmico ou que receberam tratamento de resgate para atingir os critérios de glicemia9 pré-especificados foi de 10% para o grupo de ONGLYZA 2,5 mg mais TZD, 6% para o grupo de ONGLYZA 5 mg mais TZD e de 10% para o grupo placebo3 mais TZD.

Terapia combinada16 em adição a glibenclamida
Um total de 768 pacientes com diabetes tipo 213 participaram deste estudo randomizado17, duplocego, placebo3-controlado de duração de 24 semanas, para avaliar a eficácia e segurança de ONGLYZA em combinação com uma sulfoniluréia (SU) em pacientes com controle glicêmico inadequado (A1C5 ≥7,5% a ≤10%) com a dose submáxima de SU sozinha. Foi exigido que os pacientes estivessem fazendo uso de uma dose de SU por dois meses ou mais para, então serem incluídos neste estudo. Neste estudo, uma combinação em dose fixa de ONGLYZA e uma dose intermediária de SU foi comparada à titulação com uma maior dose de SU.
Pacientes que obedeceram aos critérios de elegibilidade foram incluídos em um período únicocego, de quatro-semanas, de dieta e exercício, e início com placebo3 durante o qual os pacientes receberam glibenclamida 7,5 mg uma vez ao dia. Após o período inicial, os pacientes elegíveis com A1C5 ≥7% a ≤10% foram randomizados a 2,5 mg ou 5 mg de ONGLYZA mais 7,5 mg de glibenclamida ou placebo3 mais 10 mg de dose total diária de glibenclamida. Pacientes que receberam placebo3 foram elegíveispara receberem glibenclamida em titulação de aumento de dose até uma dose diária total de 15 mg. Titulações de aumento de glibenclamida não foram permitidas para pacientes18 que receberam ONGLYZA 2,5 mg ou 5 mg. A diminuição de dose de glibenclamida foi permitida em qualquer grupo de tratamento durante o período de 24 semanas do estudo caso houvesse hipoglicemia19, conforme julgado pelo investigador. Aproximadamente 92% dos pacientes do grupo placebo3 mais glibenclamida tiveram a dose titulada para uma dose total diária de 15 mg durante as primeiras 4 semanas do período de estudo. Pacientes que não obtiveram as metas de glicemia9 específicas foram tratados com metformina1 de resgate, e adicionados à medicação do estudo já em andamento. A titulação de dose de ONGLYZA não foi permitida durante o estudo.
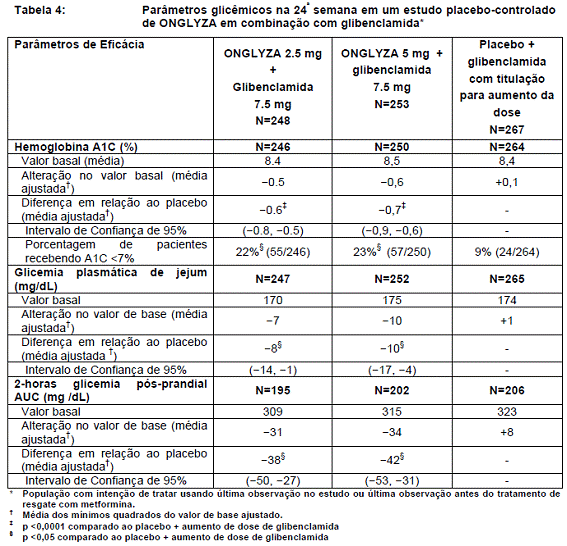
Em combinação com a glibenclamida, ONGLYZA 2,5 mg e 5 mg promoveram melhorias significativas em A1C5, FPG, e PPG comparados com o grupo placebo3 mais glibenclamida titulada (Tabela 4). A proporção de pacientes que descontinuaram por falta de controle glicêmico ou que receberam tratamento de resgate para atingir os critérios de glicemia9 pré-especificados foi de 18% no grupo de ONGLYZA 2,5 mg mais glibenclamida , 17% no grupo de ONGLYZA 5 mg mais glibenclamida e 30% no grupo placebo3 mais glibenclamida.
Combinação com a metformina1 em pacientes virgens de tratamento
Um total de 1306 pacientes virgens de tratamento com diabetes tipo 213 participaram deste estudo randomizado17, duplo-cego, ativo-controlado de duração de 24 semanas, para avaliar a eficácia e segurança de ONGLYZA em combinação com metformina1 para o tratamento inicial de pacientes com controle glicêmico inadequado (A1C5 ≥8% a ≤12%) com dieta e exercício apenas. Foi exigido que os pacientes fossem virgens de tratamento prévio para, então serem incluídos neste estudo.
Pacientes que obedeceram aos critérios de elegibilidade foram incluídos em um período únicocego, de uma semana, com dieta e exercício e início com placebo3. Os pacientes foram randomizados um dos quatro braços de tratamento: ONGLYZA 5 mg + metformina1 500 mg, saxagliptina 10 mg + metformina1 500 mg, saxagliptina 10 mg + placebo3 ou metformina1 500 mg + placebo3. ONGLYZA foi administrado uma vez ao dia. Nos 3 grupos de tratamento usando metformina1, a metformina1 foi titulada em aumentos de dose, incrementos de 500 mg por dia até alcançar uma dose máxima tolerável de 2000 mg por dia, baseado no FPG. Pacientes que não obtiveram as metas de glicemia9 específicas foram tratados com pioglitazona de resgate como terapia adicional.
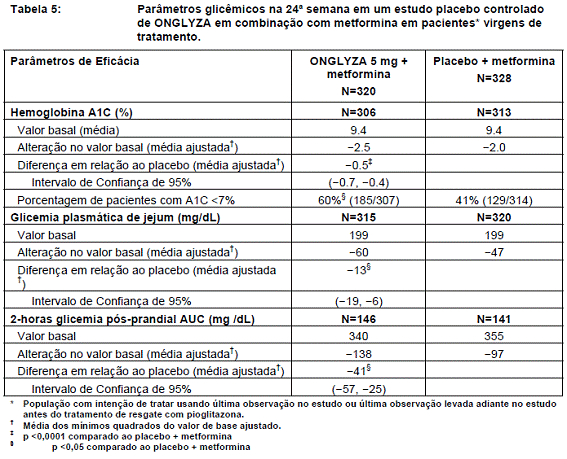
A coadministração de ONGLYZA 5 mg em combinação com a metformina1 promoveu melhorias significativas em A1C5, FPG, e PPG comparados com o grupo de placebo3 mais metformina1 (Tabela 5).
Terapia combinada16 em adição a metformina1 versus terapia combinada16 em adição de glipizida12 a metformina1
Neste estudo ativo-controlado de 52 semanas, um total de 858 pacientes com diabetes tipo 213 e controle glicêmico inadequado (A1C>6,5% e ≤10%) com metformina1 isolada foram ramdomizados em terapia duplo-cega combinada com ONGLYZA ou glipizida12. Pacientes foram requeridos a estar sob uso de dose estável de metformina1 (pelo menos 1500 mg ao dia) por pelo menos 8 semanas anteriores à inscrição.
Os pacientes que cumpriam o critério de elegibilidade foram submetidos a um período introdutório de 2 semanas, simples-cego, com placebo3, dieta e exercício, durante o qual os pacientes receberam metformina1 (1500-3000 mg com base em suas doses pré-estudo). Após o período introdutório, os pacientes eleitos foram randomizados para 5 mg de ONGLYZA ou 5 mg de glipizida12 em adição à suas atuais doses abertas de metformina1. Pacientes no grupo de glipizida12 com metformina1 receberam titulação cega da dose de glipizida12 durante as primeiras 18 semanas do estudo até uma dose máxima de glipizida12 de 20 mg/dia. A titulação objetivou a meta de FPG < 110mg/mL ou a maior dose tolerada de glipizida12. Cinquenta por cento (50%) dos pacientes tratados com glipizida12 foram titulados até a dose de 20 mg/dia; 21% dos pacientes tratados com glipizida12 tiveram uma dose final de glipizida12 de 5 mg ou menos. A dose média diária final de glipizida12 foi 15 mg.
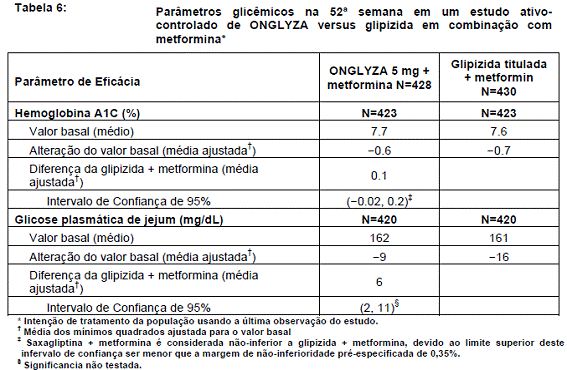
Após 52 semanas de tratamento, ONGLYZA e glipizida12 resultaram em reduções médias semelhantes do valor basal de A1C5 quando adicionada à terapia com metformina1 (Tabela 6). Esta conclusão pode se limitar a pacientes com valores basais de A1C5 comparáveis aos do estudo (91% dos pacientes tinham valores basais de A1C5 < 9%).
De um peso corporal inicial médio de 89 kg, houve uma redução média estatisticamente significativa de 1,1 kg em pacientes tratados com ONGLYZA comparado a um ganho de peso médio de 1,1 kg em pacientes tratados com glipizida12 (p <0,0001).
Insuficiência Renal14
Um total de 170 pacientes participaram de um estudo de 12 semanas, randomizado20, duplocego, controlado por placebo3 conduzido para avaliar a eficácia e segurança de ONGLYZA 2,5 mg uma vez ao dia em comparação com placebo3 em pacientes com diabetes tipo 213 e insuficiência renal14 moderada (n=90) ou grave (n=41), ou doença renal15 em estágio terminal (n=39). Neste estudo, 98% dos pacientes estavam em uso de medicamentos antidiabéticos de fundo (75% faziam uso de insulina21 e 31% faziam uso de medicamentos antidiabéticos orais22, a maioria sulfoniluréias23).
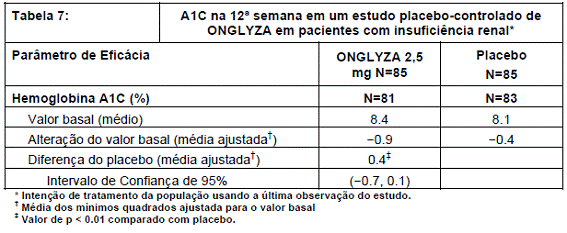
Após 12 semanas de tratamento, ONGLYZA 2,5 mg aumentou significativamente a A1C5 comparado ao placebo3 (Tabela 7). No subgrupo de pacientes com doença renal15 em estágio terminal (ESRD), ONGLYZA e placebo3 resultaram em reduções comparáveis em A1C5 dos valores basais na semana 12. Este resultado é inconclusivo, pois o estudo não foi devidamente desenhado para demonstrar a eficácia em subgrupos específicos de insuficiência renal14.
Após 12 semanas de tratamento, a alteração média na glicose24 plasmática de jejum (FPG) foi de -12 mg/dL25 com ONGLYZA 2,5 mg e -13 mg/dL25 com placebo3. Comparado com placebo3, a alteração média na FPG com ONGLYZA foi de -12 mg/dL25 no subgrupo de pacientes com insuficiência renal14 moderada, -4 mg/dL25 no subgrupo de pacientes com insuficiência renal14 grave, e +44 mg/dL25 no subgrupo de pacientes com doença renal15 em estágio terminal. Estes resultados são inconclusivos, pois o estudo não foi devidamente desenhado para demonstrar a eficácia dentro de subgrupos específicos de insuficiência renal14.
Extenção de estudo de longo prazo controlado
Os pacientes que completaram o período inicial de 12 semanas do estudo, eram elegíveis a participar de uma extenção de longo prazo do estudo controlado, por 40 semanas. Pacientes que receberam saxagliptina no período inicial de 12 semanas de estudo mantiveram a mesma dose de saxagliptina na extensão de longo prazo. A maioria dos indivíduos (76%) em ambos os grupos de tratamento recebendo insulina21 ou outros medicamentos anti-hiperglicêmicos não teve nenhuma mudança na dose ou no tipo de medicação durante o período de tratamento de 52 semanas. Para os indivíduos que tiveram uma mudança significativa no tipo e dose de insulina21 (mais de ± 20%) ou antidiabéticos de uso oral (OAD), os dados de eficácia foram posteriormente excluídos da análise.
O tratamento com saxagliptina 2,5 mg proporcionou uma melhoria sustentada em A1C5 versus placebo3 (redução média do valor basal na 52ª semana, de -1,4% para o grupo de saxagliptina e -0,5% para o grupo do placebo3).
O perfil de segurança da saxagliptina no período de tratamento a longo prazo foi consistente com o previamente observado na experiência clínica e o observado no período de tratamento de curta duração (12 semanas) deste estudo.


