
RESULTADOS DE EFICÁCIA MERITOR
Em estudo multicêntrico, duplo-cego visando avaliar a eficácia e a segurança da terapia oral combinada de glimepirida1 mais metformina2 em uma única fórmula farmacêutica em pacientes com diabetes melito3 do tipo 2 (DM2) e falha secundária na monoterapia com glibenclamida, foram incluídos 104 pacientes obesos, com DM2, os quais tinham recebido monoterapia com glibenclamida em doses máximas e terapia médica de nutrição4 durante pelo menos três meses e que apresentavam glicose5 de jejum > 140 mg/dL6 e hemoglobina glicosilada7 A1c8 (A1C8) > 8%. Os pacientes receberam durante três meses de forma titulada até 4 mg de glimepirida1, 2 mg de metformina2 ou 4 mg de glimepirida1 mais 2 mg de metformina2 em uma única apresentação. Foram considerados como critérios de eficácia a diminuição de 1% ou mais de A1C8 ou sua redução a 7% ou menos. Os resultados (média + desvio padrão) após 90 dias de seguimento mostraram uma tendência à diminuição nos pacientes que receberam a combinação de glimepirida1 mais metformina2. A diminuição da glicose5 no grupo de glimepirida1 depois dos três meses de tratamento foi de -16,7 + 57,5 mg/dL6 (IC 95%: 6,3 a -39,7), no grupo que recebeu metformina2 de 8 + 48,6 mg/dL6 (IC 95%: 29,8 a -13,8) e no da combinação de -16,8 + 58,8 mg/dL6 (IC 95%: 5,3 a -38,9).
Ao longo do estudo houve uma diminuição significativa na A1C8 no grupo que recebeu a combinação de glimepirida1 mais metformina2 e uma tendência em sua redução no grupo de glimepirida1. A diminuição da A1C8 no grupo de glimepirida1 depois dos três meses de tratamento foi de -0,9 ± 1,6% (IC 95%: -2,0 a -1,5), no grupo que recebeu metformina2 de -0,7 ± 2,1% (IC 95%: 0,2 a -1,6) e no da combinação de -1,3 ± 1,8 mg/ dL (IC 95%: -0,6 a -1,9).
A porcentagem de pacientes que conseguiram diminuir a A1C8 em 1% ou mais depois de três meses de tratamento foi de 35,1 (n = 13), 21,2 (n = 7) e 47% (n = 16) para os grupos de glimepirida1, metformina2 e combinação, respectivamente, com uma diferença estatisticamente significativa (p < 0,001) entre os grupos; que persistiu entre glimepirida1 e metformina2 (p = 0,02) e entre a combinação de metformina2 (p = 0,001), mas não entre glimepirida1 e a combinação (p = 0,08).
A porcentagem de pacientes que conseguiu diminuir a A1C8 a 7% ou menos depois de três meses de tratamento foi de 18,9 (n = 7), 9,0 (n = 3) e 23,5% (n = 8) para os grupos de glimepirida1, metformina2 e combinação, respectivamente, com uma diferença estatisticamente significativa (p = 0,01) entre os grupos; que persistiu entre glimepirida1 e metformina2 (p = 0,04) e entre a combinação e metformina2 (p = 0,004), mas não entre glimepirida1 e a combinação (p = 0,38). Os efeitos indesejáveis consistiram principalmente em moléstias gastrintestinais e foram similares (p = 0,50) nos três grupos [24,3% (n = 9) para glimepirida1, 36,3% (n = 12) para metformina2 e 26,4% (n = 9) para a combinação]. A hipoglicemia9 apresentou-se somente em 2,7% (n = 1) no grupo de glimepirida1, no 3% (n = 1) no grupo com metformina2 e no 2,9% (n = 1) no da combinação e foi considerada como leve em todos os casos. Em nenhum paciente foi necessária a suspensão do tratamento por efeitos indesejáveis.(1) Em estudo multicêntrico, randomizado10, duplo-cego, double-duumy, com grupos paralelos conduzido em pacientes diabéticos tipo 2 com idades de 35-70 anos inadequadamente controlados por monoterapia diária de 2550 mg de metformina2, por pelo menos 4 semanas que foram randomizados para metformina2, glimepirida1 ou metformina2 e glimepirida1.
O estudo consistiu de uma fase de titulação de dose por 12 semanas seguido por uma fase de manutenção de 8 semanas.
Durante a fase de titulação, o tratamento com glimepirida1 (ativa ou placebo11) foi iniciado com uma dose diária de 1 mg e aumentado de forma gradual para 2, 4 ou 6 mg uma vez ao dia, a fim de atingir uma glicemia de jejum12 dentro do critério alvo (3,9 mmol/l13 < GJ < 7,8 mmol/l13). Seguindo-se a conclusão da fase de titulação de 12 semanas, os pacientes entraram em uma fase de manutenção de 8 semanas em que as dosagens dos tratamentos de estudo tiveram que ser mantidos constantes; entretanto, no caso de sintomas14 de hipoglicemia9, a dosagem de glimepirida1 foi reduzida aos níveis anteriores.
Dos 379 pacientes randomizados para tratamento, 372 pacientes, 75 no grupo de metformina2, 150 no grupo de glimepirida1 e 147 no grupo de glimepirida1 + metformina2, receberam pelo menos uma dose do medicamento do estudo.
O tratamento combinado foi significativamente mais eficiente na redução dos níveis de HbA1c15 do que tanto apenas a glimepirida1 (diferença na alteração média de 1,04%), 95% IC 0,81-1,27%; P< 0,001) ou metformina2 apenas (diferença na alteração média de 0,92%, 95% IC 0,63-1,21%; P< 0,001).
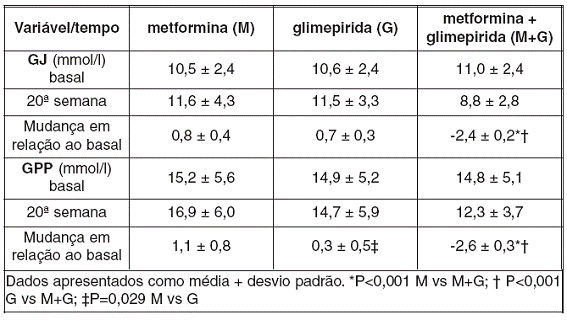
O tratamento combinado foi também significativamente mais efetivo do que qualquer monoterapia na redução de GJ (P < 0,001) e GPP (P < 0,001).
Embora não houvesse uma diferença significativa entre os dois grupos de monoterapia com respeito à alteração da glicemia de jejum12, o tratamento com glimepirida1 foi significativamente mais eficaz do que a metformina2 na redução da glicemia pós-prandial16 (P < 0,001). Os ajustes para os efeitos do centro, IMC17 e sexo não influenciaram a significância dos resultados.
Ao final do estudo, cerca de duas vezes os pacientes em qualquer grupo de monoterapia do que no grupo combinado (84% no grupo de metformina2 e 77% no grupo de glimepirida1 vs 41% no grupo combinado) foram titulados em níveis de dose mais alta de glimepirida1 (ou placebo11 equiparado).
Os eventos adversos experimentados por 105 pacientes, 22 (29%) dos pacientes no grupo de metformina2, 38 (25%) dos pacientes no grupo de glimepirida1 e 45 (31%) dos pacientes no grupo de tratamento combinado, foram considerados possivelmente relacionados ao tratamento pelo investigador.
Em grande parte o evento relacionado a tratamento mais frequentemente informado em cada grupo foi hipoglicemia9. Entretanto, a incidência18 de episódios sintomáticos foi significativamente superior no grupo de tratamento combinado do que em qualquer dos grupos em monoterapia (22% dos pacientes vs. 11% dos pacientes no grupo de metformina2 e 13% dos pacientes no grupo de glimepirida1, P = 0,039).
Em conclusão, a terapia combinada19 com glimepirida1 e metformina2 resultou em controle glicêmico significativamente superior (P < 0,001) comparado tanto com a continuação de monoterapia de metformina2 como a substituição de glimepirida1 por metformina2, sugerindo que é mais adequada a estratégia de terapia combinada19, idealmente com sulfonilureia e metformina2, em vez de trocar somente para metformina2 ou sulfonilureia, em pacientes diabéticos do Tipo 2 inadequadamente controlados por qualquer terapia.
Mais pacientes experimentaram a hipoglicemia9 sintomática20 em terapia combinada19 do que em monoterapia 22% vs. 13% no grupo de glimepirida1 e 12% no grupo de metformina2. Como o controle glicêmico melhorado é, com frequência, associado com um risco aumentado de hipoglicemia9, não é surpreendente que os pacientes tratados com a terapia combinada19 também experimentassem mais episódios.(2)


