
REAÇÕES ADVERSAS PIOGLIT
Foram realizados estudos clínicos em todo o mundo com mais de 5900 pacientes que apresentavam diabetes tipo 21 e foram tratados com pioglitazona. Nos estudos clínicos realizados nos Estados Unidos, mais de 4700 pacientes utilizaram pioglitazona, mais de 3300 foram tratados no período de 6 meses ou mais e mais de 450 pacientes receberam pioglitazona por um período de 1 ano ou mais. No quadro a seguir, apresentamos a incidência2 geral e os tipos de eventos adversos observados nos estudos clínicos placebo3-controlado que utilizaram a pioglitazona em monoterapia doses de 7,5 mg, 15 mg, 30 mg ou 45 mg uma vez ao dia:
Estudos clínicos de pioglitazona em monoterapia, controlados com placebo3: eventos adversos relatados com frequência ≥ 5% dos pacientes tratados com pioglitazona
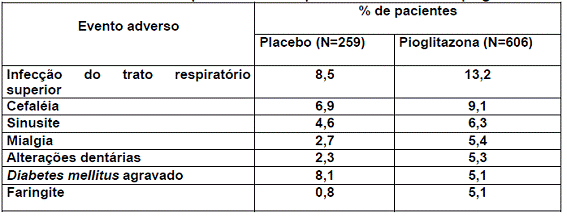
A incidência2 de grande parte dos eventos adversos observados foi similar nos grupos que receberam pioglitazona isoladamente e nos grupos que receberam pioglitazona associada com sulfoniluréia, metformina4 ou insulina5. Em relação ao edema6, foi observado um aumento da ocorrência deste evento em pacientes que receberam a associação pioglitazona e insulina5 quando comparado com pacientes que receberam apenas insulina5.
No grupo de 379 pacientes que receberam a associação pioglitazona e insulina5, 10 pacientes apresentaram dispnéia7 e também, em determinado período da terapia, alteração do peso corporal ou edema6. Desses pacientes, 7 utilizaram diuréticos8 para o tratar estes sintomas9.
Este fato não foi observado no grupo que recebeu a associação insulina5 e placebo3.
A taxa de desistência dos estudos clínicos provocada por um evento adverso com exceção da hiperglicemia10 foi semelhante no grupo que recebeu placebo3 (2,8%) e no grupo que recebeu pioglitazona (3,3%). Durante a administração da associação pioglitazona com sulfoniluréia ou insulina5, foi observada uma hipoglicemia11 leve a moderada. Nos pacientes que receberam placebo3, 1% deles apresentaram hipoglicemia11 enquanto que para os pacientes que receberam pioglitazona associada com sulfoniluréia, a incidência2 de hipoglicemia11 foi em 2% dos pacientes.
Quando a pioglitazona foi associada com uma insulina5, observou-se hipoglicemia11 em 5% dos pacientes que receberam placebo3, 8% dos pacientes que receberam 15 mg de cloridrato de pioglitazona e 15% dos pacientes que receberam 30 mg de cloridrato de pioglitazona (ver Advertências e precauções). Nos estudos duplo-cegos de monoterapia, observou-se anemia12 em < 2% dos pacientes que receberam pioglitazona e 0% dos pacientes que receberam placebo3. A associação pioglitazona e insulina5 provocou anemia12 em 1,6% dos pacientes tanto nos grupos que receberam pioglitazona quanto no que recebeu placebo3. Quando a pioglitazona foi associada com uma sulfoniluréia, observou-se anemia12 em 0,3% dos pacientes que receberam pioglitazona e 1,6% dos pacientes que receberam placebo3. Quando associada com metformina4, a anemia12 foi constatada em 1,2% dos pacientes que receberam pioglitazona e 0,0% dos pacientes que receberam placebo3.
Em estudos de monoterapia, observou-se edema6 em 4,8% dos pacientes que receberam pioglitazona e 1,2% dos pacientes que receberam placebo3. Quando associada com insulina5, foi observada uma maior frequência de edema6 em pacientes que receberam pioglitazona (15,3%) quando comparado com aqueles que receberam placebo3 (7,0%). Todos esses eventos foram classificados de intensidade leve ou moderada (ver Advertências e precauções).
Em estudos de terapia combinada13, observou-se edema6 em 7,2% dos pacientes que receberam pioglitazona e sulfoniluréia quando comparado com 2,1% dos pacientes que receberam apenas sulfoniluréia. Quando a pioglitazona foi associada com metformina4, observou-se edema6 em 6,0% dos pacientes que receberam essa associação em comparação com 2,5% dos pacientes que receberam apenas metformina4. Em estudos da associação pioglitazona e insulina5, foi constatado edema6 em 15,3% dos pacientes que receberam essa associação quando comparados com 7,0% dos pacientes que receberam apenas insulina5 (ver Advertências e precauções). A maior parte desses eventos foi classificada como de intensidade leve ou moderada.
Início ou piora do edema macular14 do paciente diabético com redução da acuidade visual15 foi constatado nos relatórios recebidos de pós-comercialização (ver Advertências e precauções).
Em um estudo clínico de 16 semanas de duração de terapia associada de insulina5 e pioglitazona, 1,1% dos pacientes que foram receberam a associação apresentaram insuficiência cardíaca congestiva16 quando comparado a 0,0% dos pacientes que receberam apenas insulina5 (ver Advertências e precauções).
Anormalidades laboratoriais
Hematológicas: pode ocorrer diminuição dos valores de hematócrito17 e hemoglobina18 devido ao uso de pioglitazona. Em todos os estudos clínicos realizados, os valores médios de hemoglobina18 sofreram redução de aproximadamente 2 a 4 % nos pacientes que receberam pioglitazona. Essa redução foi observada, geralmente, dentro das primeiras 4 a 12 semanas de terapia e manteve-se relativamente sem alteração após estas semanas. Essas alterações podem estar associadas ao aumento do volume plasmático relacionado ao tratamento com pioglitazona e não foi relacionada a nenhum efeito clinico hematológico significante.
Transaminases séricas: durantes os estudos clínicos realizados nos Estados Unidos, 0,30% (14/4780) dos pacientes que receberam pioglitazona apresentaram valores de ALT ≥ 3 vezes o limite superior da normalidade. Foram observadas elevações reversíveis de ALT em todos os pacientes que estavam sob acompanhamento. No grupo de pacientes que receberam pioglitazona, os valores médios de bilirrubina19, AST (aspartato-amino transferase), ALT, fosfatase alcalina20 e gama GT apresentavam-se diminuídos na última consulta em comparação com os respectivos valores basais. Resultados anormais da função hepática21 provocaram a saída de menos de 0,9% dos pacientes que receberam pioglitazona dos estudos americanos. Em estudos clínicos de pré-comercialização, não foram relatados casos de reações idiossincráticas pelo fármaco22 gerando insuficiência hepática23 (ver Advertências e precauções).
CPK (creatinina24 fosfoquinase): foram relatados em testes laboratoriais obrigatórios em estudos clínicos aumentos esporádicos e transitórios nas taxas de CPK. Em 9 pacientes observou-se um aumento único e isolado para taxas superiores a 10 vezes o limite superior de normalidade (valores de 2150 a 11400 UI/l); 6 destes pacientes mantiveram o tratamento com pioglitazona, 2 já tinham recebido todo o medicamento no momento do resultado do teste e 1 paciente saiu do estudo em virtude desse aumento. Esses resultados normalizaram-se sem qualquer sequela25 clínica aparente. A ligação desses eventos e a terapia com pioglitazona não é conhecida.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária - NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.


