REAÇÕES ADVERSAS XARELTO
Resumo do perfil de segurança
A segurança de Xarelto® (rivaroxabana) foi avaliada em quatro estudos de fase III que incluíram 6.097 pacientes expostos a Xarelto® (rivaroxabana) 10 mg, submetidos a uma cirurgia ortopédica de grande porte nos membros inferiores (artroplastia total do quadril ou do joelho), em 3.997 pacientes enfermos hospitalizados tratados por até 39 dias e em três estudos de fase III para tratamento de TEV com 4.556 pacientes expostos a Xarelto® (rivaroxabana) 15 mg duas vezes ao dia por três semanas seguido de 20 mg uma vez ao dia, ou a 20 mg uma vez ao dia tratados por até 21 meses.
Além disso, a segurança de Xarelto® (rivaroxabana) foi também avaliada em 7.750 pacientes com fibrilação atrial não valvular de dois estudos clínicos de fase III com, pelo menos uma dose de Xarelto® (rivaroxabana) e em 10.225 pacientes com SCA com pelo menos uma dose de Xarelto® (rivaroxabana) 2,5 mg (duas vezes ao dia) ou 5 mg (duas vezes ao dia) junto com AAS ou AAS mais clopidogrel ou ticlopidina.
Em um total aproximado de 67% de pacientes expostos a pelo menos uma dose de rivaroxabana foram relatados eventos adversos emergentes ao tratamento. Cerca de 22% dos pacientes experimentaram reações adversas consideradas relacionadas ao tratamento conforme avaliado pelos investigadores. Em pacientes tratados com Xarelto® (rivaroxabana) 10 mg submetidos à artroplastia do quadril ou joelho e em pacientes enfermos hospitalizados, ocorreram sangramentos em aproximadamente 6,8% e 12,6% dos pacientes, respectivamente, e anemia1 ocorreu em aproximadamente 5,9% e 2,1% dos pacientes, respectivamente. Em pacientes tratados tanto com Xarelto® (rivaroxabana) 15 mg duas vezes ao dia seguido de 20 mg uma vez ao dia para o tratamento de TVP ou EP, quanto com Xarelto® (rivaroxabana) 20 mg uma vez ao dia para prevenção de TVP e de EP recorrentes, eventos de sangramento ocorreram em aproximadamente 27,8% dos pacientes e anemia1 ocorreu em aproximadamente 2,2% dos pacientes. Em pacientes tratados para prevenção de AVC e embolia2 sistêmica, sangramento de qualquer tipo ou gravidade foi reportado com uma taxa de eventos de 28 por 100 pacientes ao ano, e anemia1 com uma taxa de 2,5 por 100 pacientes ao ano. Em pacientes tratados para prevenção de morte cardiovascular e infarto do miocárdio3 após síndrome4 coronariana aguda (SCA), sangramento de qualquer tipo ou gravidade foi relatado com uma taxa de evento de 22 por 100 pacientes ao ano. Anemia1 foi relatada com uma taxa de 1,4 por 100 pacientes ao ano.
Em razão do modo de ação farmacológico, Xarelto® (rivaroxabana) pode ser associado a um risco aumentado de sangramento oculto ou manifesto em qualquer tecido5 ou órgão, o que pode resultar em anemia1 pós-hemorrágica6. O risco de sangramento pode ser aumentado em certos grupos de pacientes, por exemplo, naqueles com hipertensão arterial7 grave não-controlada e/ou com medicação concomitante que afete a hemostasia8 (ver “Advertências e Precauções”). O sangramento menstrual pode ser intensificado e/ou prolongado.
Os sinais9, sintomas10 e gravidade (incluindo desfecho fatal) irão variar de acordo com a localização e o grau ou extensão do sangramento e/ou anemia1 (ver “Superdose”).
Complicações hemorrágicas11 podem se apresentar como fraqueza, palidez, tontura12, cefaleia13 ou edema14 inexplicável, dispneia15 e choque16 inexplicável. Em alguns casos, como consequência da anemia1, foram observados sintomas10 de isquemia17 cardíaca, tais como dor no peito18 ou angina19 pectoris.
Foram relatadas para Xarelto® (rivaroxabana) complicações conhecidas secundárias ao sangramento grave, como síndrome compartimental20 e falência renal21 devido à hipoperfusão. Portanto, deve-se considerar a possibilidade de uma hemorragia22 ao avaliar as condições de qualquer paciente anticoagulado.
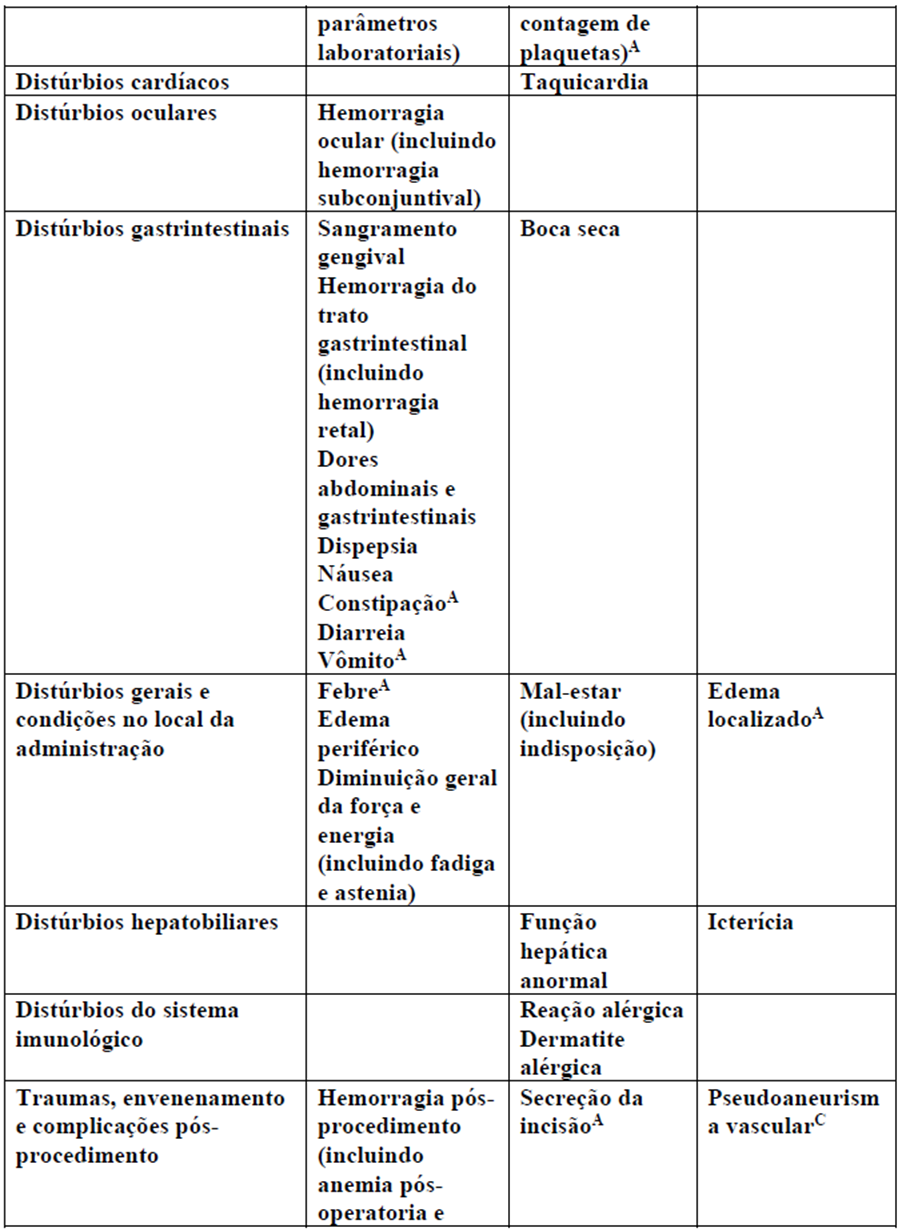
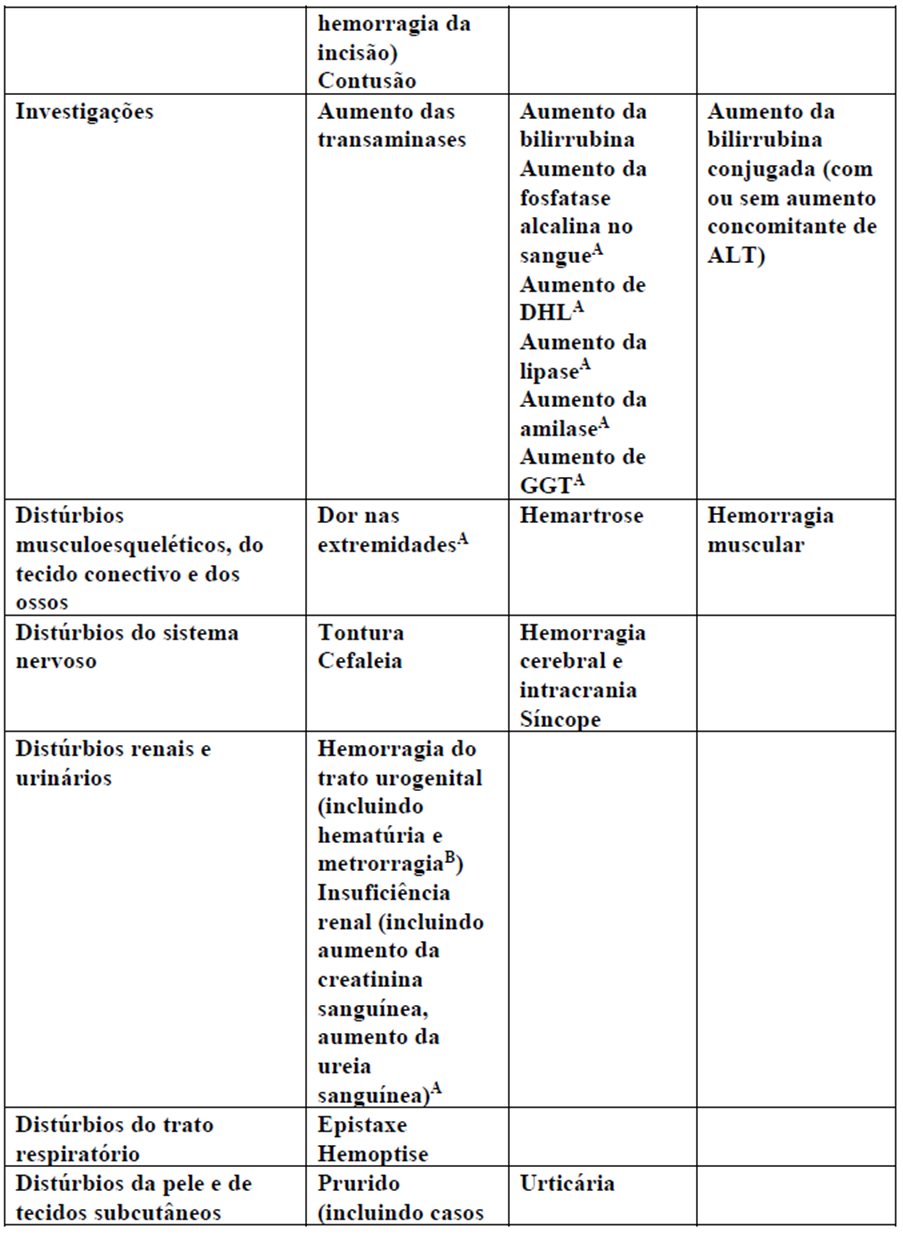
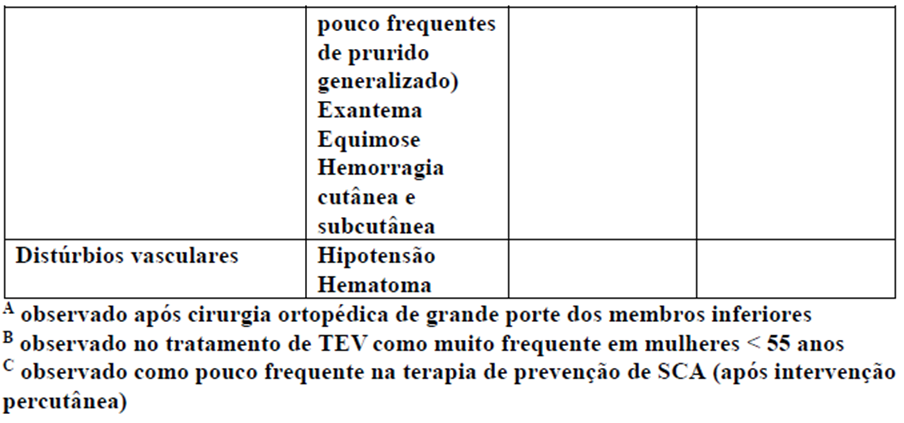
Lista tabulada de reações adversas
As frequências das reações adversas relatadas com Xarelto® (rivaroxabana) estão resumidas na tabela abaixo. As reações adversas estão apresentadas em ordem decrescente de gravidade dentro de cada grupo de frequência, que são definidas como muito frequente (≥ 1/10), frequente (≥ 1/100 a < 1/10), pouco frequente (≥ 1/1.000 a < 1/100) e rara (≥ 1/10.000 a < 1/1.000).
Observações pós-comercialização
Angioedema23 e edema14 alérgico foram relatados no período de pós-comercialização em associação temporal ao uso de Xarelto® (rivaroxabana). A frequência dessas reações adversas relatadas na experiência de pós-comercialização não pode ser estimada. Nos dados agrupados dos estudos Fase III, estes eventos foram pouco frequentes (≥ 1/1.000 a < 1/100).
“Atenção: este produto é um medicamento que possui nova concentração e nova indicação terapêutica24 no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, notifique os eventos adversos pelo Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br, ou para a Vigilância Sanitária Estadual ou Municipal.”